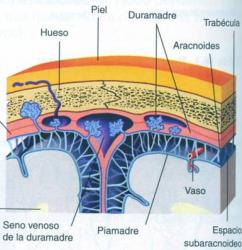
LA VACUNA DE LA TUBERCULOSIS EN CÁNCER DE VEJIGA DONDE FRACASA LA ACTUAL BCG
En modelo experimental, el grupo de la Unizar muestra que su vacuna contra la tuberculosis es superior a la BCG en cáncer de vejiga. 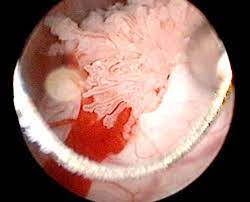
El uso de la inmunoterapia en el cáncer no es una estrategia nueva, como pueda parecer por el reciente desarrollo de los fármacos oncológicos que bloquean puntos de control inmunitario (inhibidores de checkpoint).
Entre las estrategias pioneras para espolear al sistema inmune como una potente herramienta de lucha contra el cáncer se encuentran las vacunas, estimuladoras inmunológicas por excelencia. Y, de hecho, la primera inmunoterapia contra el cáncer aprobada por la agencia del medicamento estadounidense FDA es la vacuna contra la tuberculosis BCG. Administrada por vía intravesical, es desde hace más de cuarenta años el tratamiento de primera línea en el cáncer de vejiga no músculo invasivo (Nmibc, en sus siglas inglesas) de alto riesgo.
Sin embargo, la vacuna no es eficaz en aproximadamente el 40% de los pacientes, y se estima que la mayoría de los que sufren episodios de recurrencia después del tratamiento con BCG progresan a tumor T2 (con invasión muscular); en ese punto de la enfermedad, la cistectomía radical es prácticamente la única opción terapéutica.
En un estudio coordinado por el investigador Nacho Aguiló, del Grupo de Genética de Micobacterias del Departamento de Microbiología y Medicina Preventiva que dirige Carlos Martín en la Universidad de Zaragoza, ya se ha demostrado la capacidad de la candidata vacunal contra la tuberculosis MTBVAC como agente inmunoterápico para el cáncer de vejiga en un modelo experimental.
LEn modelo experimental, el grupo de la Unizar muestra que su vacuna contra la tuberculosis es superior a la BCG en cáncer de vejiga.
El uso de la inmunoterapia en el cáncer no es una estrategia nueva, como pueda parecer por el reciente desarrollo de los fármacos oncológicos que bloquean puntos de control inmunitario (inhibidores de checkpoint).
Entre las estrategias pioneras para espolear al sistema inmune como una potente herramienta de lucha contra el cáncer se encuentran las vacunas, estimuladoras inmunológicas por excelencia. Y, de hecho, la primera inmunoterapia contra el cáncer aprobada por la agencia del medicamento estadounidense FDA es la vacuna contra la tuberculosis BCG. Administrada por vía intravesical, es desde hace más de cuarenta años el tratamiento de primera línea en el cáncer de vejiga no músculo invasivo (Nmibc, en sus siglas inglesas) de alto riesgo.
Sin embargo, la vacuna no es eficaz en aproximadamente el 40% de los pacientes, y se estima que la mayoría de los que sufren episodios de recurrencia después del tratamiento con BCG progresan a tumor T2 (con invasión muscular); en ese punto de la enfermedad, la cistectomía radical es prácticamente la única opción terapéutica.
En un estudio coordinado por el investigador Nacho Aguiló, del Grupo de Genética de Micobacterias del Departamento de Microbiología y Medicina Preventiva que dirige Carlos Martín en la Universidad de Zaragoza, ya se ha demostrado la capacidad de la candidata vacunal contra la tuberculosis MTBVAC como agente inmunoterápico para el cáncer de vejiga en un modelo experimental.
MTBVAC es la candidata vacunal para la TB construida en la Universidad de Zaragoza (Unizar) por este equipo científico y que tras más d e dos décadas de investigación se encuentra de lleno en la fase III de ensayo clínico.
e dos décadas de investigación se encuentra de lleno en la fase III de ensayo clínico.
Al igual que la centenaria BCG, utiliza una forma viva atenuada de la micobacteria causante de la enfermedad (en concreto el patógeno humano Mycobacterium tuberculosis), un hecho que podría ser clave para obtener efectos beneficiosos más allá de la prevención de la TB, y que estos científicos exploran, entre otras enfermedades, en el cáncer de vejiga.
Ahora estos investigadores dan un salto “cualitativo” con un nuevo estudio que se publica hoy lunes en Journal for ImmunoTherapy of Cancer, la revista de mayor impacto en la inmunoterapia de cáncer. Así lo considera su autor principal, Nacho Aguiló, quien destaca a DM que “vamos un paso más allá en nuestra investigación, pues nos hemos centrado en uno de los problemas reales que se producen con el tratamiento de BCG y el cáncer de vejiga: hay un grupo de pacientes, entre el 30-40%, que no responden a esta vacuna, y en la mayoría de esos casos, para evitar recidivas la opción es la cistectomía, con todo lo que ello implica de morbilidad posoperatoria y pérdida de calidad de vida”, recuerda el científico.
En 2020, un inhibidor de checkpoint, el anti PD-1 pembrolizumab recibió la aprobación por parte de la FDA para administrarse en los no respondedores a la primera línea terapéutica con BCG. El fármaco exhibe una eficacia modesta (20% de los pacientes tratados en remisión al año). En esos pacientes también se recurre al quimioterápico valrubicina, con una tasa de respuesta aún más modesta (16% sin enfermedad durante doce meses), lo que justifica la necesidad de encontrar mejores tratamientos antes de optar por la extirpación.
Con ese objetivo, los investigadores de la Unizar han puesto a punto un modelo de ratón de cáncer de vejiga resistente al tratamiento con BCG. Aquí han comprobado que la candidata vacunal MTBVAC es un estimulador del sistema inmunológico superior a BCG. En este modelo experimental de tumor de vejiga, la BCG no funcionaba en ningún caso, mientras que en MTBVAC lo hacía en un 60-70% de los animales.
“Estos datos nos hacen concluir que nuestra vacuna puede ser una alternativa viable para tratar este tipo de tumores, que no tienen cura en la actualidad más allá de la amputación de la vejiga. Además, a tenor de estos resultados no descartamos que la administración de MTBVAC en primera línea, en lugar de BCG, logre reducir el porcentaje de fracasos terapéuticos”.
MTBVAC combinado con anti PD-1
Otro hallazgo relevante del estudio es que la combinación del anticuerpo monoclonal pembrolizumab con MTBVAC consigue el rechazo del tumor en el 100% de los animales. “Repetimos el experimento tres veces, porque no nos creíamos los resultados”, comenta el científico.
Mientras MTBVAC continúa su andadura para convertirse en la sustituta de la BCG en la prevención de la TB, estos científicos exploran otros potenciales terapéuticos, además de en cáncer de vejiga, también como tratamiento en asma. Aguiló destaca el papel de Biofabri (Grupo Zendal) en el camino hacia el desarrollo clínico de estas investigaciones.
“Los cimientos están puestos: cuanto más robusto sea el desarrollo preclínico, más fácilmente se obtienen los permisos necesarios de las autoridades reguladoras para avanzar hacia el estudio clínico. Por eso ahora queremos reproducir estos hallazgos en otros modelos experimentales de cáncer de vejiga y, de forma especial, recabar más datos de seguridad de la MTBVAC en esta ruta de administración y con dosis múltiples”.
Cuentan con una gran ventaja y es toda la investigación realizada a lo largo de lustros de comparación de MTBVAC con la vacuna BCG. La investigación que este grupo lleva desplegando es una muestra de la importancia que tiene el muchas veces sordo trabajo de laboratorio.
Después de leer este artículo me he acordado de mi querido amigo Miguel un médico eminente y bondadoso qué afectado por un tumor de vejiga recibió como tratamiento la vacuna BCG intravesical.
Fue un éxito al principio, pero un par de años más tarde empieza a tener una cicatriz en toda la vejiga que le impiden a los uréteres drenar la orina a esta cavidad
Los problemas se fueron incrementando hasta conectarle unos catéteres a la vejiga que perforaban la cavidad peritoneal y se conectaban con un reservorio colocado en la espalda, ya no volvió a orinar por vías fisiológicas y periódicamente vaciaba el reservorio de la espalda terriblemente molesto pero que él con su riqueza espiritual lo soportaba perfectamente.
Con una mala calidad de vida soporto esto treintaaños, y a partir de entonces empieza tener cuadro general de afectación y le diagnostican hasta 30 metástasis en toda su biología y unos días más tarde muere con una dignidad envidiable.
Es sorprendente el ingenio de los investigadores convierten una vacuna anti microbiana nunca demasiado eficaz en un medicamento antitumoral que posiblemente no está totalmente perfeccionado pero tiene futuro.
Es admirable el ingenio de estos investigadores que siguen y siguen y van perfeccionando los beneficios de esta terapia.
Mi charla con mi amigo Miguel ya muy lesionado y con su reservorio en la espalda fueron para mí gratificantes no por el efecto médico sino por la dignidad con que soportaba sus penurias.
Nuestros tiempos que están llenos de maldades, están sin embargo conduciéndonos a un desarrollo de terapia muy eficaces sobre todo contra los malditos tumores que tanto daño nos hacen y esto se debe a la tenacidad de los investigadores que le han cogido el truco a la inmunidad.
Nacho Aguiló, Eduardo Moreo, Ana Belén Gómez, Carlos Martín, Ana Picó y Santiago Uranga, de la Universidad de Zaragoza.
Sonia Moreno. Madrid Lun, 04/07/2022 – 08:00
MTBVAC es la candidata vacunal para la TB construida en la Universidad de Zaragoza (Unizar) por este equipo científico y que tras más de dos décadas de investigación se encuentra de lleno en la fase III de ensayo clínico.
Al igual que la centenaria BCG, utiliza una forma viva atenuada de la micobacteria causante de la enfermedad (en concreto el patógeno humano Mycobacterium tuberculosis), un hecho que podría ser clave para obtener efectos beneficiosos más allá de la prevención de la TB, y que estos científicos exploran, entre otras enfermedades, en el cáncer de vejiga.
Ahora estos investigadores dan un salto “cualitativo” con un nuevo estudio que se publica hoy lunes en Journal for ImmunoTherapy of Cancer, la revista de mayor impacto en la inmunoterapia de cáncer. Así lo considera su autor principal, Nacho Aguiló, quien destaca a DM que “vamos un paso más allá en nuestra investigación, pues nos hemos centrado en uno de los problemas reales que se producen con el tratamiento de BCG y el cáncer de vejiga: hay un grupo de pacientes, entre el 30-40%, que no responden a esta vacuna, y en la mayoría de esos casos, para evitar recidivas la opción es la cistectomía, con todo lo que ello implica de morbilidad posoperatoria y pérdida de calidad de vida”, recuerda el científico.
En 2020, un inhibidor de checkpoint, el anti PD-1 pembrolizumab recibió la aprobación por parte de la FDA para administrarse en los no respondedores a la primera línea terapéutica con BCG. El fármaco exhibe una eficacia modesta (20% de los pacientes tratados en remisión al año). En esos pacientes también se recurre al quimioterápico valrubicina, con una tasa de respuesta aún más modesta (16% sin enfermedad durante doce meses), lo que justifica la necesidad de encontrar mejores tratamientos antes de optar por la extirpación.
Con ese objetivo, los investigadores de la Unizar han puesto a punto un modelo de ratón de cáncer de vejiga resistente al tratamiento con BCG. Aquí han comprobado que la candidata vacunal MTBVAC es un estimulador del sistema inmunológico superior a BCG. En este modelo experimental de tumor de vejiga, la BCG no funcionaba en ningún caso, mientras que en MTBVAC lo hacía en un 60-70% de los animales.
“Estos datos nos hacen concluir que nuestra vacuna puede ser una alternativa viable para tratar este tipo de tumores, que no tienen cura en la actualidad más allá de la amputación de la vejiga. Además, a tenor de estos resultados no descartamos que la administración de MTBVAC en primera línea, en lugar de BCG, logre reducir el porcentaje de fracasos terapéuticos”.
MTBVAC combinado con anti PD-1
Otro hallazgo relevante del estudio es que la combinación del anticuerpo monoclonal pembrolizumab con MTBVAC consigue el rechazo del tumor en el 100% de los animales. “Repetimos el experimento tres veces, porque no nos creíamos los resultados”, comenta el científico.
Mientras MTBVAC continúa su andadura para convertirse en la sustituta de la BCG en la prevención de la TB, estos científicos exploran otros potenciales terapéuticos, además de en cáncer de vejiga, también como tratamiento en asma. Aguiló destaca el papel de Biofabri (Grupo Zendal) en el camino hacia el desarrollo clínico de estas investigaciones.
“Los cimientos están puestos: cuanto más robusto sea el desarrollo preclínico, más fácilmente se obtienen los permisos necesarios de las autoridades reguladoras para avanzar hacia el estudio clínico. Por eso ahora queremos reproducir estos hallazgos en otros modelos experimentales de cáncer de vejiga y, de forma especial, recabar más datos de seguridad de la MTBVAC en esta ruta de administración y con dosis múltiples”.
Cuentan con una gran ventaja y es toda la investigación realizada a lo largo de lustros de comparación de MTBVAC con la vacuna BCG. La investigación que este grupo lleva desplegando es una muestra de la importancia que tiene el muchas veces sordo trabajo de laboratorio.
Después de leer este artículo me he acordado de mi querido amigo Miguel un médico eminente y bondadoso qué afectado por un tumor de vejiga recibió como tratamiento la vacuna BCG intravesical.
Fue un éxito al principio, pero un par de años más tarde empieza a tener una cicatriz en toda la vejiga que le impiden a los uréteres drenar la orina a esta cavidad
Los problemas se fueron incrementando hasta conectarle unos catéteres a la vejiga que perforaban la cavidad peritoneal y se conectaban con un reservorio colocado en la espalda, ya no volvió a orinar por vías fisiológicas y periódicamente vaciaba el reservorio de la espalda terriblemente molesto pero que él con su riqueza espiritual lo soportaba perfectamente.
Con una mala calidad de vida soporto esto treintaaños, y a partir de entonces empieza tener cuadro general de afectación y le diagnostican hasta 30 metástasis en toda su biología y unos días más tarde muere con una dignidad envidiable.
Es sorprendente el ingenio de los investigadores convierten una vacuna anti microbiana nunca demasiado eficaz en un medicamento antitumoral que posiblemente no está totalmente perfeccionado pero tiene futuro.
Es admirable el ingenio de estos investigadores que siguen y siguen y van perfeccionando los beneficios de esta terapia.
Mi charla con mi amigo Miguel ya muy lesionado y con su reservorio en la espalda fueron para mí gratificantes no por el efecto médico sino por la dignidad con que soportaba sus penurias.
Nuestros tiempos que están llenos de maldades, están sin embargo conduciéndonos a un desarrollo de terapia muy eficaces sobre todo contra los malditos tumores que tanto daño nos hacen y esto se debe a la tenacidad de los investigadores que le han cogido el truco a la inmunidad.
Nacho Aguiló, Eduardo Moreo, Ana Belén Gómez, Carlos Martín, Ana Picó y Santiago Uranga, de la Universidad de Zaragoza.
Sonia Moreno. Madrid Lun, 04/07/2022 – 08:00


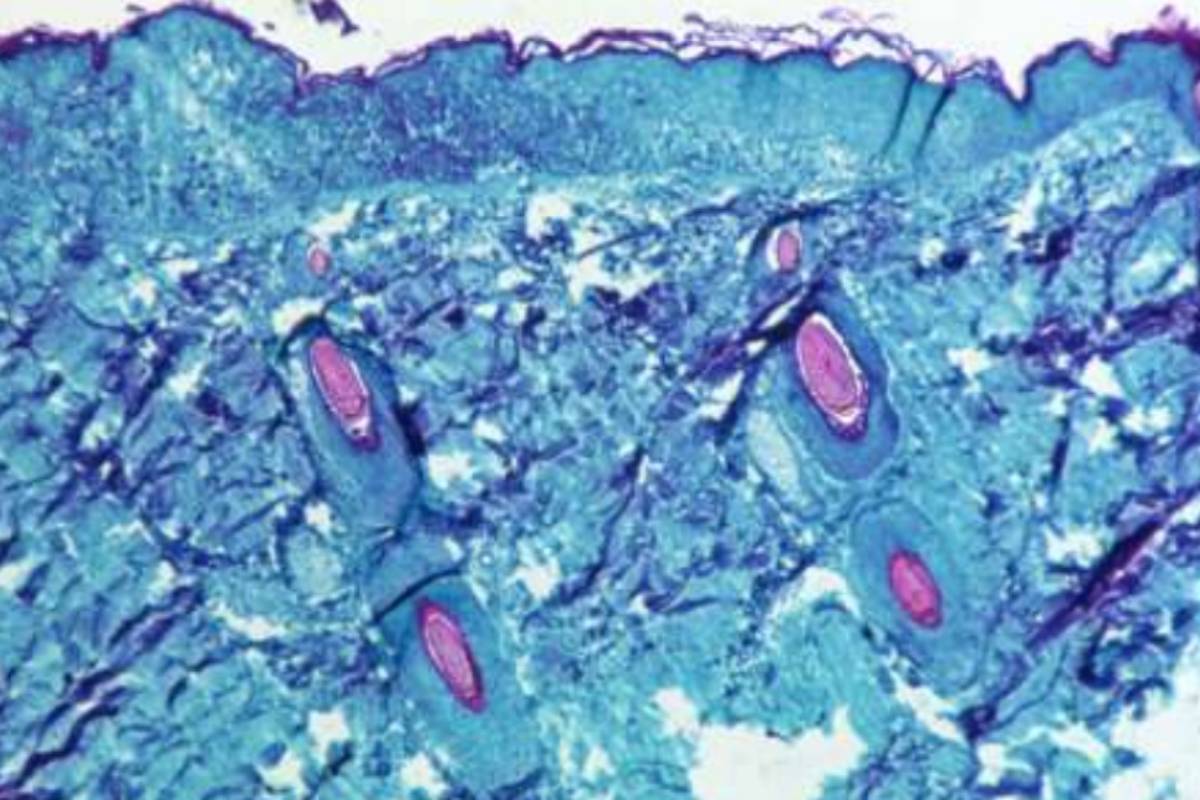 Expertos señalan la importancia de cortar las cadenas de transmisión de la viruela del mono. Foto:
Expertos señalan la importancia de cortar las cadenas de transmisión de la viruela del mono. Foto: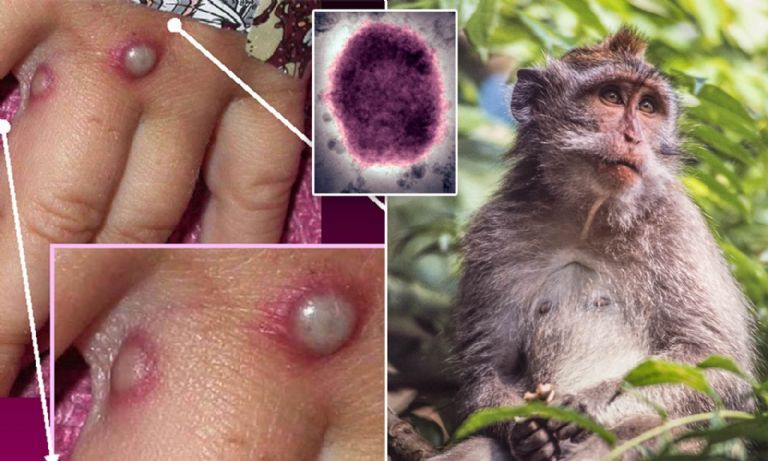 Esta semana, con la detección el 14 de mayo de dos casos en Reino Unido y 30 casos confirmados ya en España, el mayor número fuera de África, han sonado todas las alarmas y la Organización Mundial de la Salud (OMS) prevé una reunión extraordinaria para la próxima semana. ¿Hay motivos serios de preocupación?
Esta semana, con la detección el 14 de mayo de dos casos en Reino Unido y 30 casos confirmados ya en España, el mayor número fuera de África, han sonado todas las alarmas y la Organización Mundial de la Salud (OMS) prevé una reunión extraordinaria para la próxima semana. ¿Hay motivos serios de preocupación? Daniel López Acuña, epidemiólogo y ex director de Acción Sanitaria de la OMS.
Daniel López Acuña, epidemiólogo y ex director de Acción Sanitaria de la OMS.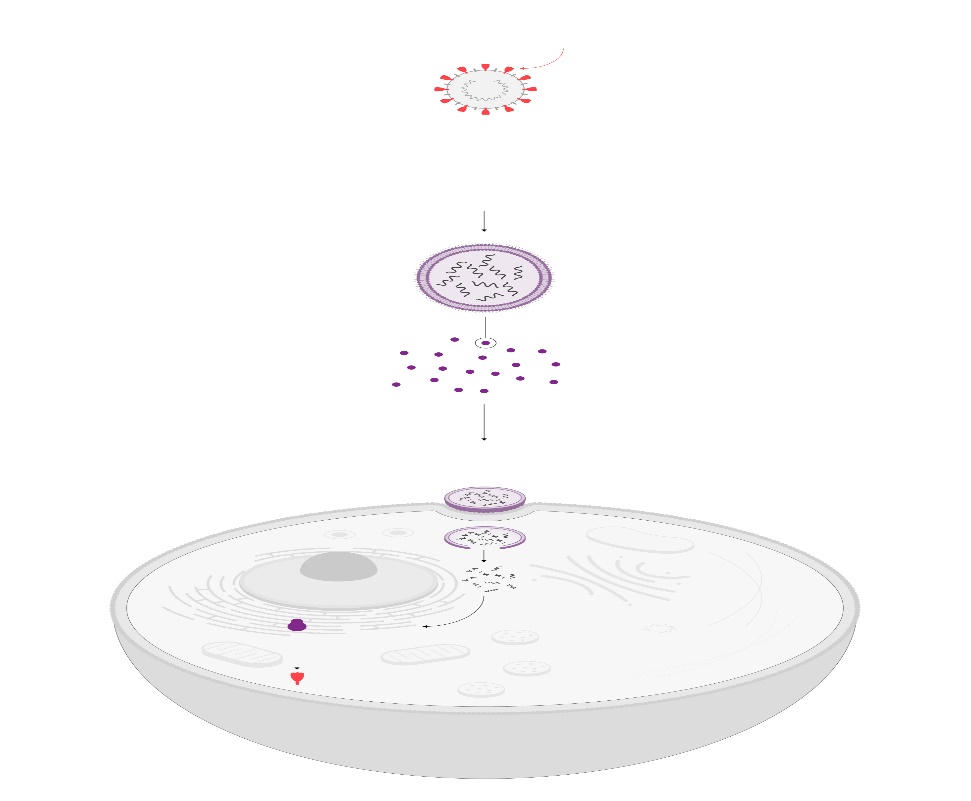
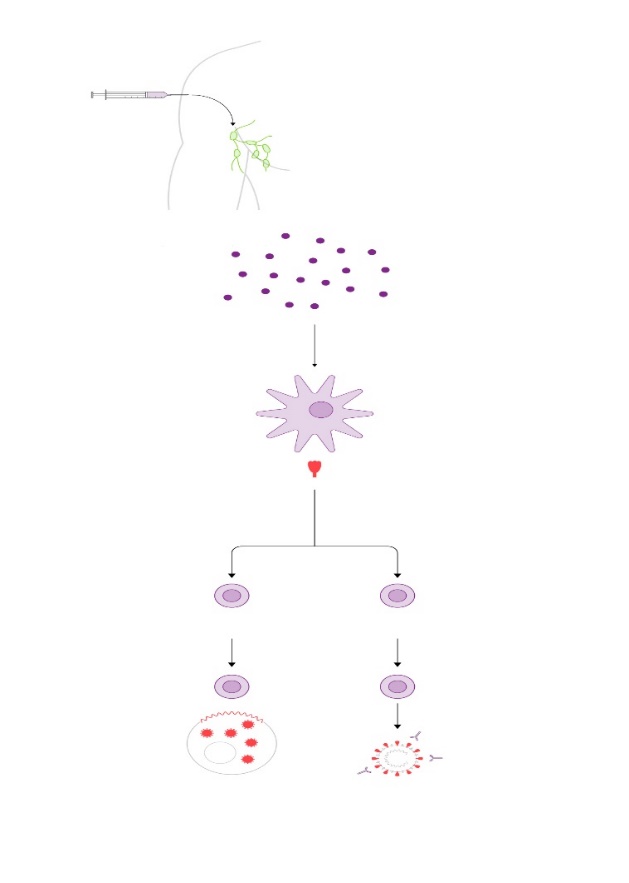
 Vacunas terapéuticas con ARN mensajero se ensayan ya frente a tumores como el melanoma, el cáncer de páncreas o el colorrectal. ILUSTRACIÓN: Gabriel Sanz
Vacunas terapéuticas con ARN mensajero se ensayan ya frente a tumores como el melanoma, el cáncer de páncreas o el colorrectal. ILUSTRACIÓN: Gabriel Sanz

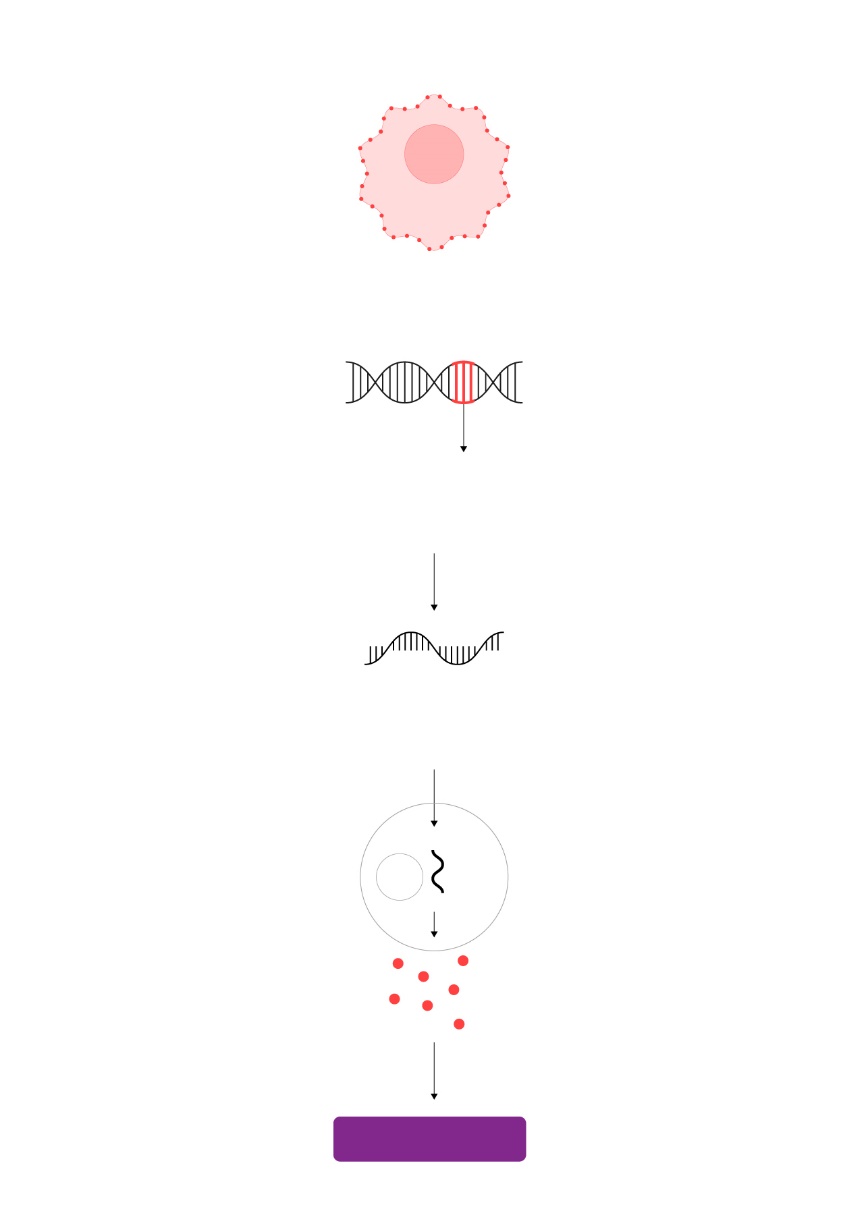
 El análisis molecular de tumores supone un antes y después en la Oncología. Ilustración: Gabriel Sanz
El análisis molecular de tumores supone un antes y después en la Oncología. Ilustración: Gabriel Sanz