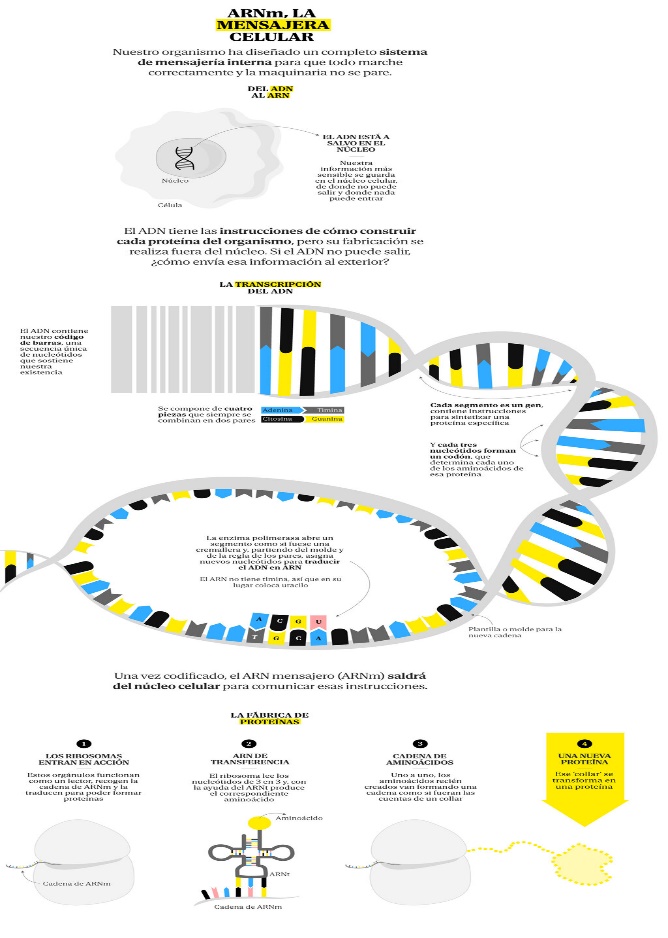
CAR-T TRATAMIENTO DEL CÁNCER CON CÉLULAS MANIPULADAS
La inmunidad celular es aquella realizada mediante el ataque directo de las células inmunes contra los agentes externos al organismo. La inmunidad humoral es el principal mecanismo de defensa contra los microorganismos extracelulares y sus toxinas, y se realiza mediante anticuerpos que atacan a los antígenos de las células extrañas al organismo.
Un CART consiste en rediseñar las células “buenas” del organismo de un paciente para combatir un cáncer. Pero no cualquier célula. No. Las seleccionadas son los linfocitos T.
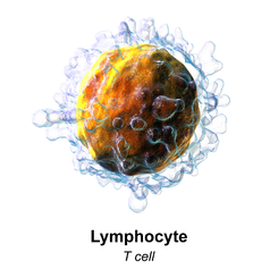
Un linfocito T es una célula de nuestro propio organismo, el de todos, pacientes y personas sanas. Los linfocitos son unidades fundamentales de nuestro cuerpo. Son creados por nuestra médula ósea, una substancia que se encuentra dentro de nuestros huesos y contiene las células madre de la sangre que, a posteriori, se convertirán en glóbulos rojos, glóbulos blancos o plaquetas.
Los glóbulos blancos (o leucocitos) son parte del sistema inmunitario de nuestro cuerpo. Nos ayudan a combatir infecciones, elementos extraños (microorganismos, células tumorales o antígenos en general), etc…. Hay 3 grandes tipos de glóbulos blancos: los granulocitos (neutrófilos, eosinófilos y basófilos), los monocitos y los linfocitos (células T y células B).
Los linfocitos T, que se desarrollan en el timo, participan en la respuesta inmunitaria celular** de nuestro organismo; y los linfocitos B, que se desarrollan en la médula ósea y luego migran a diferentes tejidos linfáticos, son los encargados de la respuesta humoral** transformándose en plasmocitos que producen anticuerpos.
Los linfocitos T tienen un receptor especial en la membrana de las células que es específico de ellos y se llama, en inglés, T cell receptor.
Cada año, más de 6.400 personas son diagnosticadas de leucemia en España, es el cáncer infantil más frecuente (un 30% de las neoplasias en niños).
Además de la leucemia, quizá el cáncer de la sangre más conocido, muchas personas también son diagnosticadas de linfomas, mieloma múltiple, síndromes mielodisplásicos, entre muchos otros
Una persona que padece un cáncer de la sangre como una leucemia o un linfoma, por ejemplo, tiene una médula ósea que no está funcionando correctamente. Por causas todavía desconocidas, las células madre de la sangre empiezan a fabricar en cantidades excesivas una línea celular, por ejemplo, los linfocitos. Estos linfocitos son inmaduros (linfoblastos), se multiplican rápidamente y desplazan a las células normales de la médula ósea, el tejido blando del centro de los huesos dónde se forman las células sanguíneas.
Lo que pretende la quimioterapia es administrar una serie de fármacos muy potentes y que estos erradiquen completamente las células cancerígenas (y, desgraciadamente, también las sanas). Cuando los tratamientos de quimioterapia no son suficientes, bien porque la enfermedad no remite, bien porque reaparece, en algunos cánceres de la sangre, los hematólogos pueden plantear un trasplante de células madre de la sangre (médula ósea, sangre periférica o sangre de cordón umbilical).
Básicamente, un trasplante de células madre de la sangre (llamado, médicamente, trasplante de progenitores hematopoyéticos) consiste en “substituir” la médula ósea dañada del paciente por una nueva. En un trasplante autólogo, se tratan las propias células madre de la sangre del paciente y se le vuelven a infundir y, en un trasplante alogénico, éstas se substituyen por las células de un donante sano. Muchos cánceres de la sangre pueden requerir un trasplante de células madre: las leucemias agudas, los linfomas, el mieloma múltiple o los síndromes mielodisplásicos, entre otros.
¿Qué ocurrió en abril de 2012?
Tenemos que remontarnos un poco más atrás. El Dr. Carl June es un inmunólogo y oncólogo americano que trabaja en la Universidad de Pensilvania (Filadelfia, Estados Unidos).
El Dr. June empezó su carrera como investigador centrándose sobre todo en el virus de inmunodeficiencia humana (VIH). Su idea era estimular el propio sistema inmunitario de estos pacientes para luchar contra el SIDA. Pero sus prioridades cambiaron cuando a su mujer le diagnosticaron un cáncer de ovario en 1996, cuando tenía 41 años. June intentó desarrollar entonces una inmunoterapia contra el cáncer, pero no logró convencer a ninguna compañía de que invirtiera en el proyecto. Cuando su mujer murió en el 2001, June decidió dedicarse a tiempo completo a la inmunoterapia del cáncer.
¿Qué es un CART?
Las células tumorales expresan unos receptores en sus membranas. En cada subtipo de la enfermedad, estas células, y, por lo tanto, los receptores, son distintos y se denominan con “nombres” diferentes. Por ejemplo, los receptores de las células de una leucemia linfoblástica aguda o de algunos linfomas no Hodgkin de tipo B como el linfoma no Hodgkin de células B grandes, se llaman CD19; los del linfoma de Hodgkin o de algunos tipos de linfomas no Hodgkin de tipo T, CD30; o los del mieloma múltiple, CD38. Estos “CD” (cúmulo de diferenciación) son antígenos celulares que se expresan en las membranas de las células tumorales y están formados por cadenas de aminoácidos.
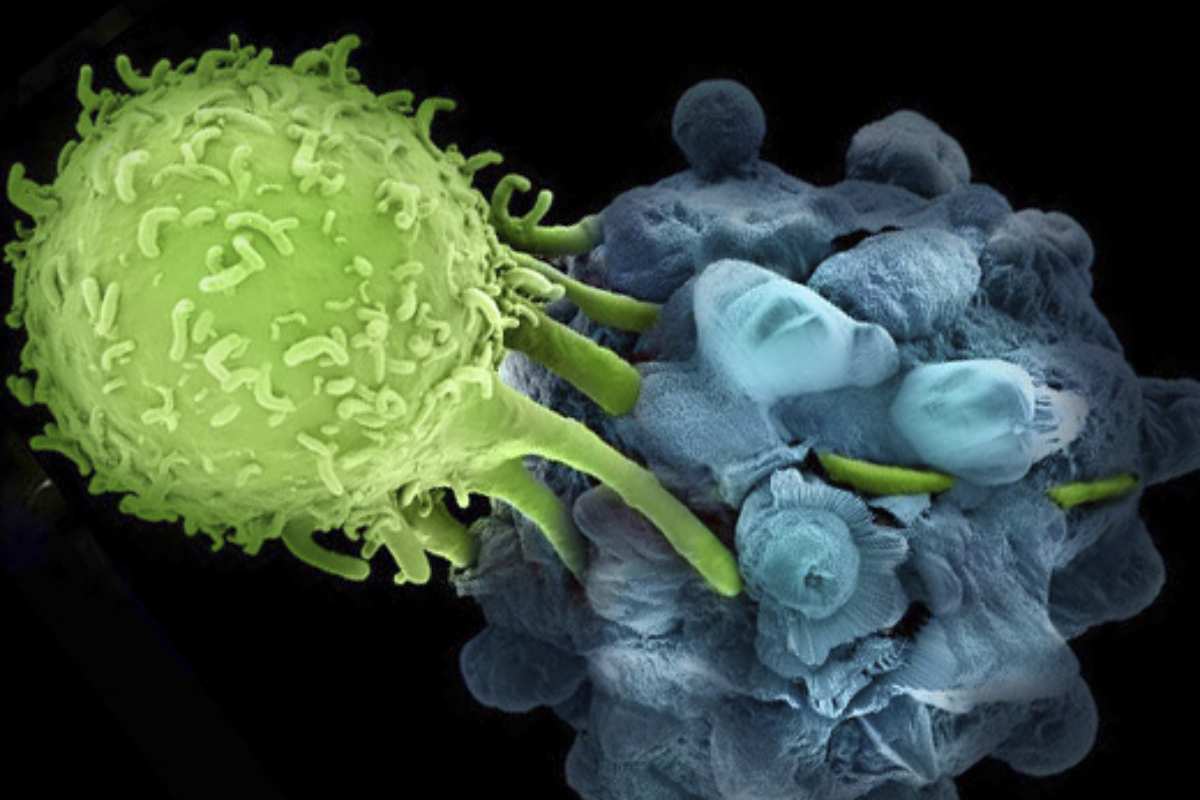
Pero, volvamos a los linfocitos T. Como ya hemos dicho anteriormente, estos están “entrenados” para matar células extrañas del organismo. Podríamos decir que son “naturalmente asesinos”. Pero, en una analogía bélica poco adecuada pero muy descriptiva, podríamos decir que están diseñados biológicamente para “matar moscas a cañonazos”. Erradican muchas células extrañas que se encuentran, pero no todas y no específicamente. Un CART podría definirse, con nuestra analogía, como un calibrado de estas células. Sería coger estos linfocitos T que ya tiene el paciente y saben destruir células, y diseñarlos concretamente para acabar con los receptores concretos de las células tumorales: CD19, CD30, CD38…. según la enfermedad que se esté tratando.
¿Cómo se administra un CART?
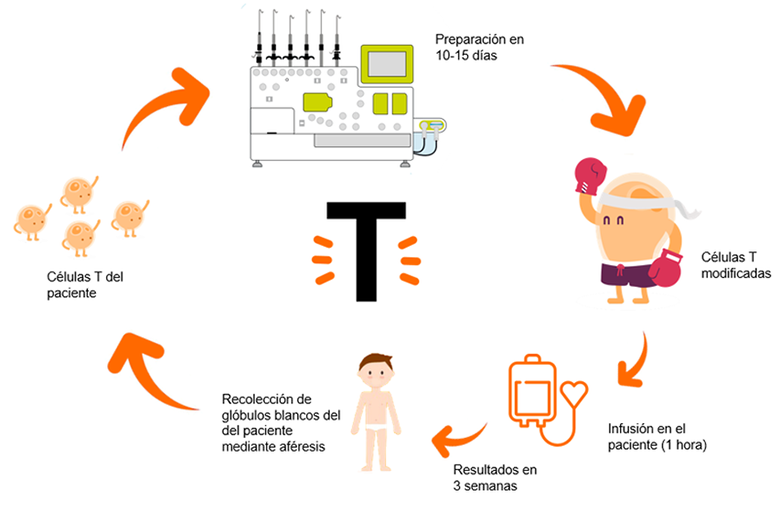
Se extraen los linfocitos T del propio paciente a tratar. Pongamos por caso que es un paciente de leucemia linfoblástica aguda de tipo B (ya hemos comentado anteriormente que las células tumorales de este paciente expresan unos antígenos llamados CD19).
Mediante un lentivirus, un virus cuyo periodo de incubación es muy largo, los inmunólogos infectaran a estos linfocitos T con un virus perpetuo anti-CD19 y los multiplicaran en el laboratorio.
Tienen los parámetros ambientales estrictamente controlados: partículas en aire, temperatura, humedad, flujo de aire, presión interior del aire, iluminación…
A posteriori, tras un ciclo de acondicionamiento con quimioterapia, se infundirán estas células anti-CD19 de nuevo en el paciente. De esta manera, en el paciente quedarán unos linfocitos T perpetuos cargados con “armamento anti-CD19” que se llamarán CART anti-CD19.
El primer CART que se llevó a cabo en Estados Unidos fue el CART anti-D19 para leucemia linfoblástica aguda de tipo B infantil, el que se administró a Emily Whitehead. Este ensayo clínico fue posible gracias a una gran farmacéutica, Novartis. Hasta 2016, los tratamientos de inmunoterapia CART que se realizaron en Estados Unidos fueron ensayos clínicos de grandes empresas farmacéuticas. En 2016, Novartis inició el primer ensayo clínico de esta inmunoterapia en algunos hospitales pediátricos de Europa. En nuestro país, los primeros CARTs se realizaron como ensayo clínico en el Hospital Sant Joan de Déu de Barcelona.
Los resultados de estos primeros ensayos clínicos fueron espectaculares y completamente sorprendentes para el mundo de la medicina en general y de la hematología en particular. El 80% de los pacientes estaban libres de la enfermedad un año después de someterse al CART. Es importante destacar que todos estos pacientes eran niños o personas muy jóvenes, todos menores de 25 años, que no habían respondido a ninguno de los tratamientos previos, incluidos trasplantes de células madre de la sangre.
A pesar de ello, la coyuntura de estos ensayos clínicos es complicada. La mayoría de tratamientos CART se suministran a través de una farmacéutica y, por lo tanto, son ensayos clínicos privados, y su coste es muy alto.
En paralelo a estos descubrimientos, algunos grupos de hematólogos e inmunólogos decidieron avanzar para crear unos CARTs llamados “académicos”. Son CARTs impulsados por un hospital universitario, en nuestro país, público, y, por lo tanto, con un coste mucho más asequible. El Hospital Clínic de Barcelona, de la mano del Dr. Álvaro Urbano-Ispizua y del inmunólogo, Dr. Manuel Juan, fueron los primeros en tener a punto un CART académico anti-CD19. Una vez logrados los permisos de la Agencia Española del Medicamento, se empezó el primer ensayo clínico con CART académico anti CD19 en el Hospital Clínic, para adultos, y en el Hospital Sant Joan de Déu para niños. Todos los receptores tenían que ser pacientes con leucemia linfoblástica aguda de tipo B y menores de 25 años. Los resultados también fueron los esperados. En paralelo, en varios hospitales también se continuaron los ensayos clínicos del CART anti-CD19 comercial de la industria farmacéutica).
A pesar de que los primeros resultados fueron apabullantes (>80% de pacientes libres de la enfermedad), los científicos pronto vieron que había que perfeccionar algunos aspectos de esta nueva terapia. En primer lugar, se dieron cuenta que la administración del CART provocaba en el paciente una reacción grave llamada “síndrome de liberación de citoquinas”. El síndrome de liberación de citocinas se presenta por una liberación masiva y rápida en la sangre de las células afectadas por la inmunoterapia. Las citocinas son sustancias que tienen muchas acciones diferentes en el cuerpo. Los signos y síntomas del síndrome de liberación de citocinas incluyen fiebre, náuseas, dolor de cabeza, sarpullidos, latidos cardíacos rápidos, presión arterial baja y dificultad para respirar. La mayoría de los pacientes tienen una reacción leve, pero, a veces, la reacción es grave o pone en peligro la vida. Por ello, se crearon equipos multidisciplinarios para tratar a estos pacientes y, hoy en día, es una complicación que se ha sabido manejar positivamente.
Por otra parte, se vio como algunos pacientes “perdían” los CARTs con el paso del tiempo, perdiendo por supuesto también la reacción inmunológica contra las células tumorales. A pesar de ello, hoy en día el 40-50% de los pacientes que se someten a un CART anti-CD19 siguen libres de la enfermedad pasado un año. Un resultado a mejorar, por supuesto, pero de momento, exitoso.
Actualmente, en nuestro país conviven los ensayos clínicos de CART comerciales y los académicos. No solamente se han desarrollado inmunoterapias CART anti-CD19 para leucemia linfoblástica aguda de tipo B sino también para linfomas no Hodgkin de tipo B como el linfoma difuso de células grandes, por ejemplo. Están ya en curso ensayos clínicos con inmunoterapia anti-CD30 para linfoma de Hodgkin y linfomas no Hodgkin de tipo T y, se están estudiando esta terapia para otras dolencias como la leucemia mieloide aguda. También hay centros españoles que han iniciado ensayos clínicos, tanto académicos como comerciales, con inmunoterapia CART para mieloma múltiple.
La inmunoterapia CART es el futuro de la curación de muchos cánceres de la sangre. En un futuro se espera poder desarrollar estrategias de tratamiento CART también para pacientes con otras neoplasias hematológicas o, incluso, tumores sólidos. El campo de aplicación de esta terapia es muy amplio.
Pero la inmunoterapia CART no es el futuro por si sola. De hecho, hoy en día se están realizando tratamientos de CART incluso a pacientes que se no consigue hacer remitir la enfermedad para conseguir erradicarla y, a posteriori, realizarles un trasplante de células madre de la sangre. La inmunoterapia CART es una nueva arma que deberá complementar y regularse junto con el arsenal terapéutico ya existente.
Carl H. June, inmunólogo y pionero en la terapia con células CAR-T confía en que este tipo de tratamientos llegue también a otras patologías no oncológicas.
En 1999, June empezó a aplicar, ya en la Universidad de Pensilvania, sus conocimientos sobre el VIH para intentar estimular al sistema inmune frente a la enfermedad. Así surgió un programa de entrenamiento para que ciertas células inmunitarias, los linfocitos T, atacaran con mayor precisión y potencia a las células tumorales. Mediante ingeniería genética modificaron linfocitos T para que expresaran un marcador, un receptor antigénico quimérico (CAR, en su acrónimo inglés). “Como sabía mucho sobre el VIH, fuimos los únicos que utilizamos este tipo de virus [modificado para que no cause enfermedad] para colocar la molécula CAR en las células T y resulta que era una buena forma. Tuve suerte. Haberme formado en diferentes disciplinas resultó ser una ventaja muy grande y algo que nunca hubiera planeado. Fue un accidente causado por la guerra”, resume con sencillez.
La terapia con células CAR-T de June cosechó resultados sorprendentes en sus primeros ensayos iniciados en 2010 con pacientes afectados por leucemia linfocítica crónica refractaria y recidivante, incluida poco después una niña de seis años que ahora es una adolescente sin rastro de la enfermedad. Hoy, hay varias compañías farmacéuticas que comercializan células CAR-T para diversas indicaciones, todas de cáncer hematológico. En España, un total de 15 hospitales están autorizados para administrarlas a los pacientes, mediante un proceso que implica extraer los linfocitos del paciente, modificarlos genéticamente en un laboratorio e introducirlos de nuevo en el enfermo para que ataquen a las células enfermas.
Deben superarse otras barreras para que esta terapia pueda funcionar en otros tumores?
Son mas difíciles que en el cáncer hematológico, porque el cáncer sólido tiene más formas de apagar el sistema inmunológico; cuenta con muros, algunos hechos con tejido cicatricial, para evitar que los invasores entren. En el cáncer de la sangre, las células CAR-T no tienen que atravesar una pared para llegar hasta la célula tumoral. Por esto estamos trabajando en diversos enfoques, como combinar las células CAR-T con un virus capaz de infectar al tumor para ayudar a los linfocitos a entrar. De hecho, esta investigación la llevamos a cabo con un equipo de Barcelona, con Ramón Alemany, quien desarrolló el virus oncolítico, y Sònia Guedan, que estuvo haciendo un posgrado en mi laboratorio de Pensilvania. Tenemos un ensayo clínico abierto en cáncer de ovario. También vamos a ensayar el cáncer de páncreas con esta estrategia combinada. Y creo que habrá muchos más estudios en esta línea. Es una forma de derribar los muros, que parece muy prometedora. Hay muchas investigaciones aquí en España y en todo el mundo para tratar de hacer que funcione en el cáncer sólido. Y está funcionando en ratones y está empezando a funcionar en algunos ensayos en humanos, por ejemplo, se han visto datos emocionantes en un reciente ensayo sobre cáncer cerebral infantil en Stanford. Hay mil ensayos ahora, sin embargo, es importante recordar que estamos en el campo de la investigación. De momento, la terapia CAR-T solo está aprobada para el cáncer de sangre.
«Las CAR-T está empezando a funcionar, en el campo de la investigación, en tumores como el de páncreas, cerebral y de ovario»
También se está trabajando en otras enfermedades diferentes al cáncer, como el lupus, .
Las células CAR-T aplicadas al cáncer activan el sistema inmunitario, pero también puede ser interesante desactivarlo, por ejemplo, en el caso de las enfermedades autoinmunes o para evitar el rechazo en un trasplante de riñón. Si se pudiera diseñar una célula que desactivara específicamente la respuesta contra el órgano trasplantado, tendríamos un tratamiento más seguro para el paciente, que no contraería ni siquiera infecciones. En esa dirección se está investigando mucho con las llamadas células T reguladoras (Tregs). Acabamos de empezar un ensayo en la Universidad de Pensilvania con este tratamiento. En el lupus que menciona, se ha tratado ya a algunos pacientes en un ensayo, en la Universidad de Erlangen, en Alemania, con resultados emocionantes.
También hemos publicado datos en ratones donde hemos tratado la fibrosis cardíaca. Y hay muchas enfermedades en las que se generan cicatrices, por ejemplo, en los pulmones.
Vamos a ver cómo se utilizan las células manipuladas para muchos tipos de enfermedades aparte del cáncer. Todavía es pronto, pero creo que podremos tratar con células modificadas incluso patologías como la esclerosis múltiple o la enfermedad de Alzheimer, donde se acumulan proteínas en el cerebro. Casi todas las enfermedades tienen algún tipo de componente de inflamación, y podemos intentar dirigir células modificadas para que actúen sobre las moléculas que causan el daño.
P. Volviendo a las actuales células CAR-T. Es cierto que están añadiendo vida a un grupo de pacientes, pero no siempre funcionan, ¿cómo mejorarlas?
R. Hay varias estrategias para aumentar su eficacia. Por un lado, están las combinaciones, como la de los virus oncolíticos que comentaba para alcanzar mejor a los tumores. También está la idea de manipular a la célula T para que sea más potente, convertirla en un especie súper célula T, mediante la modificación de sus genes.
Otra categoría de investigación, es conseguir que la célula CAR-T luche contra el microambiente del tumor, que es lo que lo protege y favorece su crecimiento.
Y también se avanza en conseguir que los linfocitos T tengan el mismo efecto que los anticuerpos que inhiben los llamados puntos de control (checkpoint), la inmunoterapia que se emplea ahora en algunos tipos de cáncer. Esta es un área muy prometedora, pues se obtendrían una célula CAR-T que de forma local, una vez en el tumor, secrete los anticuerpos. Una de mis colaboradoras, Marcela Maus, que ahora está en Harvard, trabaja con células CAR-T que segregan BiTE [del inglés, anticuerpo biespecífico de células T], un anticuerpo que tiene dos especificidades, es muy complejo. Se une a una célula T y a la célula tumoral. De esta forma, la célula CAR-T cuenta con su propio anticuerpo dirigido al tumor y aporta ese anticuerpo biespecífico que puede dirigirse al microambiente del tumor. Como ve, hay mucha investigación y muy esperanzadora en este campo.
Un potencial por explorar en las CAR: fibrosis cardíaca, lupus y hepatitis B
La Red Española de Terapias Avanzadas se hace más fuerte en España
Las CAR-T se consolidan en linfoma, leucemia y mieloma múltiple
P. Además, existe la posibilidad de utilizar otras células diferentes los linfocitos T.
R. Sí, como las células asesinas naturales (CAR-NK) y también los hay macrófagos, que llamamos CAR-Ms. Tenemos un ensayo en la Universidad de Pensilvania con macrófagos, que literalmente se comen las células tumorales. Mientras que las células T hacen agujeros en la célula tumoral provocando que muera, los macrófagos las eliminan por fagocitosis. Esperamos que, dado que acaban de forma diferente con el tumor, puedan ser dos aproximaciones sinérgicas.
Un problema de estas terapias es su alto coste, que también dificulta el acceso a todos los pacientes que lo necesiten, la logística de la fabricación es muy complicada y se necesita a profesionales altamente cualificados, pero hay ejemplos que nos indican que esto no tiene que ser siempre así. El caso de los coches, por ejemplo, con Henry Ford, se fabricaban con trabajadores en una línea de montaje y ahora el 80% o más de un coche está fabricado por robots. Tendrá que llegar la automatización de la fabricación celular, lo que reducirá su coste drásticamente.
Y otro forma de abordar el problema también será utilizar en lugar de las propias células T del paciente, células ya listas, cultivadas en grandes lotes y disponibles para cualquier enfermo. Esto también haría más accesible.
Esto es una cuestión de ingeniería, no hace falta ningún descubrimiento científico. Es como aprender a hacer teléfonos móviles mejores y más baratos. Ahora estamos en esa etapa de conseguir que la fabricación de la terapia celular se abarate y terminará haciéndose directamente en el hospital, sin esperar tantos días para su producción. Ahora ya sabe que extraen la sangre del paciente, la envían a un centro de fabricación, cuando están listas, congelan las células y las envían de vuelta, para que el médico las infunda en el paciente. Todo eso se hará en un futuro en el lugar donde está el paciente, de forma más sencillo y mucho menos costosa. ►
¿Qué hospitales administran CARTs en España y cómo lo hacen?
Para explicar qué hospitales administran CARTs y si estos son académicos o comerciales es necesario entender por qué diferentes fases para la aprobación de un ensayo clínico en nuestro país.
Fases IMPRESCINDIBLES (en la práctica y en la legalidad) para producir un tratamiento eficaz
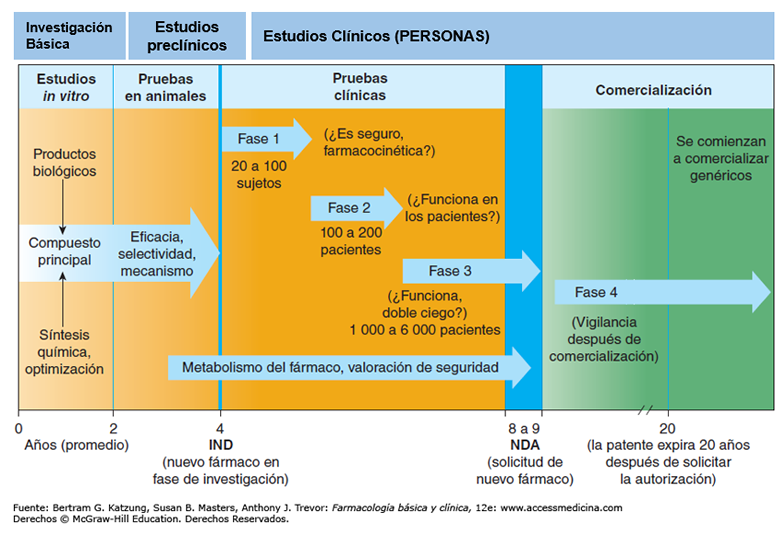
Como se puede leer en la gráfica adjunta, después de los estudios celulares y los estudios en modelos animales, un tratamiento entra en una fase de ensayo clínico denominada Fase I. Para a ello, el equipo debe haber demostrado la efectividad del nuevo tratamiento con 3 pruebas exitosas en modelos animales en condiciones GMP*, haber presentado toda la documentación a la Agencia Española del Medicamento y haber recibido su verificación y autorización. Solo entonces, se podrá llevar a cabo una prueba en unos 10-30 pacientes debidamente seleccionados.
Una vez analizados estos resultados en estos pocos pacientes, se continua o no el ensayo en Fase 2, 3, etc… Son procedimientos muy costosos y complicados.
En el caso del CART anti-CD19, se llevaron a cabo en España todas las pruebas pertinentes y, en diciembre de 2018, la Ministra de Sanidad, Consumo y Bienestar Social, María Luisa Carcedo, anunció la aprobación de la financiación de la primera terapia CART de la industria farmacéutica privada en el Sistema Nacional de Salud (SNS). Se trataba del CART anti-CD19 de Novartis (Kymriah®), indicado para tratar la leucemia linfoblástica aguda (LLA) de células B refractaria, en recaída postrasplante de médula ósea o en segunda o posterior recaída en pacientes pediátricos y adultos jóvenes de hasta 25 años de edad y para la indicación de linfoma B difuso de célula grande (LBDCG), en recaída o refractario tras dos o más líneas de tratamiento sistémico en pacientes adultos. La ministra realizó este anuncio junto a la presentación del Libro blanco de la terapia celular en España, de la Red de Terapia Celular Española del Instituto de Salud Carlos III.
¿Cuál es el criterio para la selección de pacientes para someterse a una inmunoterapia CART?
Según el Ministerio de Sanidad, en el caso de los pacientes de leucemia linfoblástica aguda B, se consideran pacientes candidatos a iniciar un tratamiento de inmunoterapia CAR-T anti CD19 los siguientes pacientes:
Pacientes pediátricos y adultos jóvenes hasta 25 años.
Pacientes de leucemia linfoblástica aguda B (LLA-B) CD19+ refractaria o en recaída:
– Segunda o posterior recaída de la enfermedad tras el tratamiento con dosis convencionales de quimioterapia/terapia de anticuerpo monoclonal.
– Cualquier recaída que ocurra tras un trasplante alogénico de progenitores hematopoyéticos (alo TPH o trasplante procedente de un donante).
– Enfermedad refractaria primaria que no logra alcanzar respuesta completa tras la segunda línea de quimioterapia estándar.
– Enfermedad refractaria secundaria definida como no lograr una respuesta completa después de 1 ciclo de quimioterapia estándar en casos de LLA en recaída.
– Pacientes en recaída que no son candidatos por criterio clínico a un aloTPH (trasplante de donante), pero que están en un estado funcional adecuado para el tratamiento con inmunoterapia CAR-T.
Según el Ministerio de Sanidad, en el caso de los pacientes de linfoma difuso de células B grandes, se consideran pacientes candidatos a iniciar un tratamiento de inmunoterapia CAR-T anti CD19 los pacientes:
Pacientes adultos (mayores de 18 años).
Pacientes de linfoma difuso de células B grandes (LDCBG), linfoma folicular transformado a LDCBG o linfoma primario del mediastino.
Pacientes con la enfermedad en recaída o refractaria tras al menos 2 líneas de tratamiento sistémico, definida por uno de los criterios que vienen a continuación, y que o bien el paciente no hubiera respondido al trasplante autólogo o bien no fuera candidato por criterios clínicos:
– Pacientes con LBDCG que ha recibido 2 o más líneas de terapia sistémica y recae después de la ultima línea o es refractario a la ultima línea de terapia sistémica.
-Pacientes con linfoma folicular transformado que ha recibido 2 o mas líneas de terapia sistémica desde el diagnóstico de transformación y recae después de la ultima línea o es refractario a la ultima línea de terapia sistémica.
Breve Bibliografia
Carl H.June es director del Centro de Inmunoterapias Celulares de la Universidad de Pensilvania.
Foto: ÁNGEL NAVARRETE.
Sonia Moreno. Madrid Vie, 09/09/2022 – 17:47
 Cifras de supervivencia de cáncer en 2023 y los factores de riesgo asociados. Infografía: SEOM.
Cifras de supervivencia de cáncer en 2023 y los factores de riesgo asociados. Infografía: SEOM.











 Elena Garralda, jefa del Grupo de Desarrollo Clínico Precoz de Fármacos del Vall d’Hebron Instituto de Oncología (VHIO). Foto: VHIO.
Elena Garralda, jefa del Grupo de Desarrollo Clínico Precoz de Fármacos del Vall d’Hebron Instituto de Oncología (VHIO). Foto: VHIO. Expertos señalan la importancia de cortar las cadenas de transmisión de la viruela del mono. Foto:
Expertos señalan la importancia de cortar las cadenas de transmisión de la viruela del mono. Foto: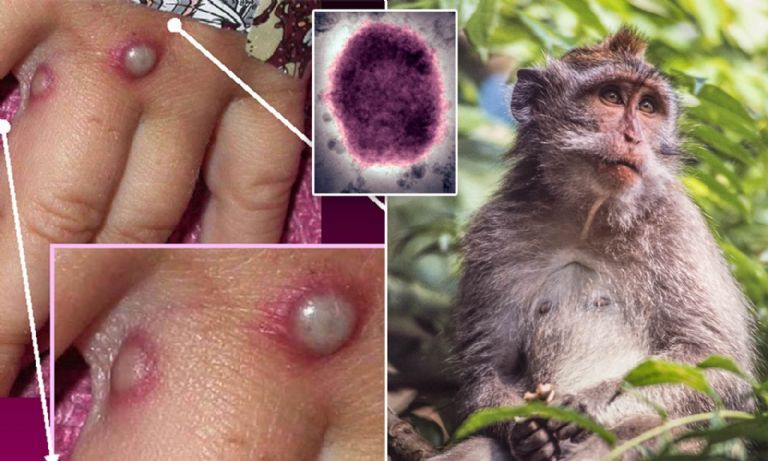 Esta semana, con la detección el 14 de mayo de dos casos en Reino Unido y 30 casos confirmados ya en España, el mayor número fuera de África, han sonado todas las alarmas y la Organización Mundial de la Salud (OMS) prevé una reunión extraordinaria para la próxima semana. ¿Hay motivos serios de preocupación?
Esta semana, con la detección el 14 de mayo de dos casos en Reino Unido y 30 casos confirmados ya en España, el mayor número fuera de África, han sonado todas las alarmas y la Organización Mundial de la Salud (OMS) prevé una reunión extraordinaria para la próxima semana. ¿Hay motivos serios de preocupación? Daniel López Acuña, epidemiólogo y ex director de Acción Sanitaria de la OMS.
Daniel López Acuña, epidemiólogo y ex director de Acción Sanitaria de la OMS.