CÉLULAS IPS,REPROGRAMACIÓN CELULAR Y EPIGENETICA:
EL CIENTÍFICO BRITÁNICO JOHN B. GURDON Y EL APONÉS SHINYA YAMANAKA HAN GANADO EL PREMIO NOBEL DE MEDICINA 2012 POR SUS INVESTIGACIONES PIONERAS EN CLONACIÓN Y CÉLULAS MADRE.
En 2006, Shinya Yamanaka hizo un descubrimiento sorprendente que le llevó a ganar el Premio Nobel en Fisiología o Medicina tan solo 6 años después: encontró una nueva manera de “reprogramar” células especializadas adultas para convertirlas en células madre. Éstas células madre de laboratorio son pluripotentes – pueden dar lugar a cualquier tipo de célula del cuerpo – y se llaman células madre pluripotentes inducidas, o células iPS. Sólo las células madre embrionarias son de naturaleza pluripotente. El descubrimiento de Yamanaka significa que cualquier célula del cuerpo en division puede ahora convertirse en una célula madre pluripotente.

Yamanaka añadió cuatro genes a células de la piel provenientes de ratón. Este hecho inició un proceso en el interior de las células llamado reprogramación y, en un periodo de 2-3 semanas, las células de las piel se transformaron en células madre pluripotentes.
La institución ha galardonado al científico británico John B. Gurdon y el japonés Shinya Yamanaka
Estos avances «han creado nuevas oportunidades para investigar enfermedades y desarrollar métodos para diagnósticos y terapias.
Gurdon, de la Universidad de Cambridge (Reino Unido), sentó las bases de la clonación en experimentos realizados en ranas en 1962. Sus investigaciones fueron claves para la clonación de la oveja Dolly y, posteriormente, de mamíferos de otras especies.
PUBLICIDAD
Yamanaka, de la Universidad de Kioto, sentó las bases de las investigaciones actuales con células madre al demostrar en 2006 cómo se pueden obtener las llamadas células madre pluripotentes a partir de células adultas. Las células pluripotentes tienen el potencial de diferenciarse en cualquier otra célula del organismo, por lo que se espera poder utilizarlas en un futuro próximo para regenerar órganos y tejidos dañados.
Según el acta del premio, Gurdon (Dippenhall, 1933) y Yamanaka (Osaka, 1962) reciben en Nobel «por el descubrimiento de que las células maduras se pueden reprogramar para convertirse en pluripotentes».
Reprogramar: este es el concepto clave que une los trabajos de Gurdon y de Yamanaka.
Gurdon reprogramó organismos enteros y Yamanaka, células individuales. A raíz de sus trabajos, destaca la Asamblea Nobel, “se han reescrito los libros de texto y se han creado nuevos campos de investigación”.
Antes de estos descubrimientos, biólogos y medicos pensaban que el desarrollo de un organismo es un viaje en sentido único. Desde la concepción hasta la muerte, las células se transforman para formar unos tejidos u otros. Una vez transformadas, se pensaba, no pueden volver atrás. Es decir, no pueden reprogramarse.
Gurdon fue el primero que cuestionó este dogma al demostrar, en 1962, que la especialización de las células es reversible. En su experimento, extrajo el núcleo de un óvulo de rana y lo sustituyó por el núcleo de una célula intestinal, también de rana.
Se pensaba entonces, la célula intestinal no hubiera podido volver atrás para ser de nuevo un óvulo. Pero Gurdon observó que, a partir del óvulo en que había introducido el núcleo de una célula intestinal, se desarrolló un renacuajo perfectamente normal. Por lo tanto, sí podía volver atrás. Había reprogamado el óvulo.
Yamanaka, por su parte, se preguntó por qué las células de un embrión tienen la capacidad de convertirse en cualquier tejido del organismo. Razonó que esta capacidad tenía que estar regulada por algunos genes y empezó a buscar genes candidatos .
Yamanaka, penso si se pudieran crear células madre a partir de células de los propios pacientes, no serían rechazadas por el sistema inmunitario. Y tampoco serían rechazadas por los sectores religiosos contrarios a utilizar células embrionarias.
Yamanaka descubrió que sólo cuatro genes eran suficientes para transformar células adultas en células como las de un embrión –a las que llamó células madre plutipotentes inducidas, más conocidas como células iPS-. A diferencia del descubrimiento de Gurdon, que había sido recibido con escepticismo, el de Yamanaka fue reconocido inmediatamente como un hito.
“Estos descubrimientos han proporcionado nuevas herramientas a científicos de todo el mundo y como ejemplo, que “se pueden obtener células de la piel de pacientes con distintas enfermedades; estas células se pueden reprogramar y examinar en el laboratorio para observar en qué difieren de las células de personas sanas. Estas células representan herramientas muy valiosas para comprender los mecanismos de las enfermedades y, por lo tanto, abren nuevas oportunidades para desarrollar tratamientos médicos”.
A partir de aquí empieza la epigenetica. Un 80m% del genoma modifica y dirige la multiplicación celular hasta donde la biología la necesita, pero su alteración conduce a graves desordenes.
La palabra epigenética significa literalmente «por encima de los genes», y eso resume perfectamente el epigenoma.
Todos tenemos nuestro ADN único, siempre y cuando no se tenga un gemelo idéntico. Y casi todas las células de nuestro cuerpo contienen todo nuestro ADN y todos los genes que nos hacen ser quienes somos. Esto se conoce como el genoma. Pero, no todas las células son iguales, por ejemplo, nuestras células cerebrales hacen cosas diferentes a las del corazón, que a su vez se comportan de manera diferente a las células de la piel.
Nuestras células tienen todas la misma información, en forma de ADN, ¿pero hacen cosas diferentes?
Aquí es donde entra en juego la epigenética. Básicamente es una capa de instrucción por encima del ADN al que le dice qué activar, cómo actuar, etc.
Esto es similar a una orquesta en la que nuestro ADN serían los músicos y el epigenoma sería el director, que les dice a las células qué deben hacer y cuándo hacerlo. La orquesta de cada persona es diferente. Por eso, aunque el epigenoma no cambia nuestro ADN, si que es el responsable de decidir qué genes se expresarán y cuales no. 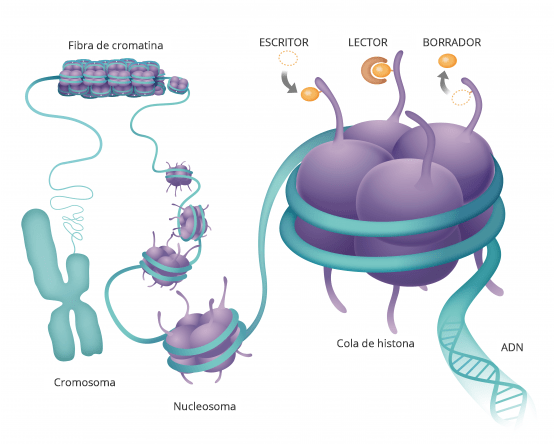
Resumiendo, cada célula con todo su ADN espera instrucciones externas, las cuales vienen en forma de un grupo METILO, un compuesto hecho de carbono e hidrógeno. Estos grupos metilo se unen a los genes, haciéndoles saber cuándo expresarse y cuándo permanecer inactivos, y se unen de manera diferente dependiendo de en qué parte del cuerpo se encuentra el ADN. Además hay otras moléculas que son las HISTONAS que también juegan un papel muy importante en cómo se expresan los genes, pues las histonas son las proteínas alrededor de las cuales se enrolla el ADN. La forma en que este el ADN empaquetado alrededor de la histona juega un papel importante en la fuerza con que se expresa un gen.
Genotipia
Investigadores del Hospital Monte Sinaí han realizado el mayor análisis de variaciones epigenéticas en el genoma humano hasta la fecha, que proporciona una herramienta que podría mejorar el diagnóstico genético de algunas enfermedades.
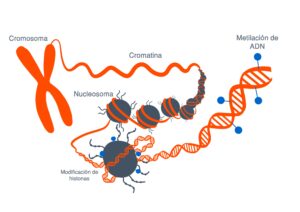 Los mecanismos epigenéticos, que regulan la expresión de los genes sin modificar la secuencia de ADN también pueden contribuir al desarrollo de enfermedades. Imagen: Rosario García, Genotipia.
Los mecanismos epigenéticos, que regulan la expresión de los genes sin modificar la secuencia de ADN también pueden contribuir al desarrollo de enfermedades. Imagen: Rosario García, Genotipia.
“Debido a que las variantes epigenéticas que identificamos no serían detectadas por la secuenciación genómica a pesar de poder conducir a la desregulación y silenciamiento de genes relacionados con enfermedades hereditarias, nuestro trabajo muestra que algunos tipos de mutaciones causantes de enfermedades serán omitidos por las pruebas genéticas estándar que solo analizan la secuencia de ADN”, señala Andrew Sharp, profesor de genética y genómica en la Facultad de Medicina de la Universidad Monte Sinaí y director del trabajo.
En las últimas décadas, numerosos estudios han abordado el análisis del ADN a la búsqueda de aquellos cambios que influyen en las características humanas y tienen un papel relevante en la salud. Además de la secuencia del ADN existen otros mecanismos de regulación de la expresión que también pueden repercutir en mayor o menor grado en el desarrollo de enfermedades, los denominados mecanismos epigenéticos.
En el estudio, los investigadores han analizado de forma extensa uno de estos mecanismos, la metilación del ADN, con el objetivo de determinar hasta qué punto son frecuentes y cuál es la distribución de las variaciones epigenéticas (epivariaciones) en el genoma humano. Además, el equipo ha combinado la información obtenida con datos de expresión génica, lo que ha permitido identificar cómo afectan las epivariaciones a la actividad de los genes.
Tras analizar la metilación del genoma en más de 23 000 personas, los investigadores han detectado 4452 epivariaciones en los cromosomas no sexuales. Este resultado implica que las epivariaciones son un suceso frecuente en el genoma humano. Dentro de los cambios epigenéticos identificados se incluyen 384 localizados en regiones reguladoras de genes relacionados con enfermedades humanas que podrían influir negativamente en su expresión. De hecho, a partir de los datos de expresión, los investigadores han estimado que muchas de las epivariaciones identificadas están relacionadas con cambios de expresión fuera de lo habitual.
No obstante, al igual que ocurre con los cambios en la secuencia del ADN, no todas las epivariaciones tienen un efecto negativo. Por ejemplo, la segunda epivariación más común, presente en aproximadamente 1 de cada 325 personas, es una hipermetilación del promotor del gen FRA10AC1 producida por una expansión CGG que se considera una variante benigna. De hecho, los investigadores señalan que las epivariaciones que pueden causar enfermedades, como por ejemplo, una hipermetilación en el gen BRCA1, son muy poco frecuentes.
A partir de estudios con gemelos, el equipo también ha analizado algunas de las causas y mecanismos por los que se producen las epivariaciones. Los gemelos idénticos, tienen la misma composición genética de origen de forma que es posible detectar si un cambio concreto se ha producido tras la formación de los dos embriones. En este caso, los investigadores han podido estimar que dos tercios de las epivariaciones se producen como consecuencia de cambios en la secuencia que afectan a elementos reguladores (y por lo tanto probablemente son hereditarios) y un tercio se produce por cambios somáticos.
El estudio proporciona un catálogo de cambios epigenéticos poco frecuentes en el genoma humano que podría representar una herramienta de interés para el diagnóstico en algunas ocasiones en las que la secuenciación del genoma de un paciente no ha obtenido resultados definitivos. “En una era en la que la secuenciación del genoma está siendo aplicada a millones de personas, nuestros resultados muestran que el estudio de la variación epigenética pueden proporcionar perspectivas de la función del genoma”, concluyen los autores.
EPIGENÉTICA
Cancer y gen metilado
La epigenética es un campo de la ciencia, todavía incipiente, que tendrá implicaciones muy importantes sobre cómo abordamos nuestra salud y la de las generaciones futuras.
La palabra epigenética significa literalmente «por encima de los genes», y eso resume perfectamente el epigenoma.
Todos tenemos nuestro ADN único, siempre y cuando no se tenga un gemelo idéntico. Y casi todas las células de nuestro cuerpo contienen todo nuestro ADN y todos los genes que nos hacen ser quienes somos. Esto se conoce como el genoma. Pero, no todas las células son iguales, por ejemplo, nuestras células cerebrales hacen cosas diferentes a las del corazón, que a su vez se comportan de manera diferente a las células de la piel.
Nuestras células tienen todas la misma información, en forma de ADN, ¿pero hacen cosas diferentes?
Aquí es donde entra en juego la epigenética. Básicamente es una capa de instrucción por encima del ADN al que le dice qué activar, cómo actuar, etc.
Esto es similar a una orquesta en la que nuestro ADN serían los músicos y el epigenoma sería el director, que les dice a las células qué deben hacer y cuándo hacerlo. La orquesta de cada persona es diferente. Por eso, aunque el epigenoma no cambia nuestro ADN, si que es el responsable de decidir qué genes se expresarán y cuales no. 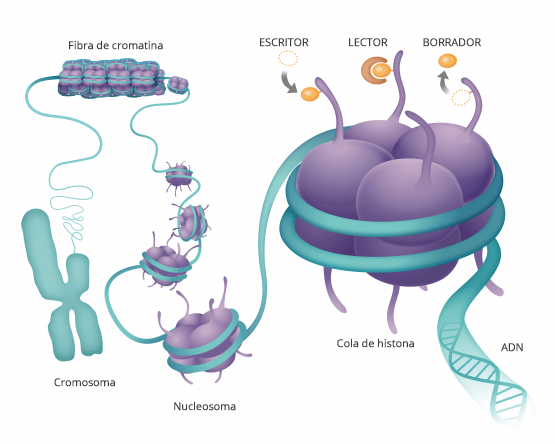
Resumiendo, cada célula con todo su ADN espera instrucciones externas, las cuales vienen en forma de un grupo METILO, un compuesto hecho de carbono e hidrógeno. Estos grupos metilo se unen a los genes, haciéndoles saber cuándo expresarse y cuándo permanecer inactivos, y se unen de manera diferente dependiendo de en qué parte del cuerpo se encuentra el ADN. Además hay otras moléculas que son las HISTONAS que también juegan un papel muy importante en cómo se expresan los genes, pues las histonas son las proteínas alrededor de las cuales se enrolla el ADN. La forma en que este el ADN empaquetado alrededor de la histona juega un papel importante en la fuerza con que se expresa un gen.
Referencias
Shinya Yamanaka 2006, John B. Gurdon reprogramación celular
Amparo Tolosa
Garg P, et al. A Survey of Rare Epigenetic Variation in 23,116 Human Genomes Identifies Disease-Relevant Epivariations and CGG Expansions. Am J Hum Gen. 2020. DOI: https://doi.org/10.1016/j.ajhg.2020.08.019
Mount Sinai study shows widespread epigenetic defects in the human genome. https://www.eurekalert.org/pub_releases/2020-09/tmsh-mss090920.php