EISNTEINS LA VIDA TRAS LA MUERTE
Qué le pasa a nuestra esencia cuando nuestro corazón deja de latir? ¿A dónde va todo lo que sentimos, pensamos y soñamos? ¿Se apagará todo como una luz que se apaga para siempre? ¿O hay algo que continúa invisible a los ojos, pero eterno por naturaleza? Mucha gente vive ignorando estas preguntas. Trabajan, pagan cuentas, enfrentan problemas y olvidan que la vida un día les exigirá enfrentarse al misterio más profundo de todos, la muerte. Pero, ¿qué pasaría si os dijera que uno de los mayores genios de la historia de la humanidad creía que el alma no desaparece? Que permanezca como una forma de energía viva, presente, pulsando en otra dimensión. Albert Einstein, conocido por desentrañar las leyes del universo, hizo sorprendentes declaraciones sobre algo que la ciencia tradicional tiende a evitar, la existencia del alma. Creía que todo es energía y que la energía no se puede destruir. Entonces, ¿qué dice eso sobre ti? ¿Sobre qué pasa después del último aliento? Este vídeo le mostrará algo que quizás nunca antes haya escuchado. Un lado oculto de Einstein, donde se encuentran la física, la conciencia y la eternidad. Prepárate para repensar lo que entiendes por muerte y por vida. Lo que descubras hoy podría cambiar para siempre la forma en que ves tu propia existencia. Si este tema tocó algo dentro de ti, aprovecha y suscríbete al canal ahora. Aquí tenemos nuevos vídeos todos los días, siempre trayendo reflexiones profundas y transformadoras que sacan lo mejor de ti. Y quiero invitaros a interactuar en los comentarios. Decime desde donde estáis viendo este vídeo. Construyamos juntos una comunidad que busque significado, conciencia y crecimiento real. La pregunta que la ciencia evita, ¿a dónde va el alma? A menudo pasamos por la vida sin afrontar una pregunta inevitable. ¿Qué pasa después de morir? La mayoría de las personas evitan este pensamiento como alguien que cierra una puerta incómoda, ocupándose de las tareas diarias, las facturas, los teléfonos móviles y las distracciones. Pero tarde o temprano todos nos enfrentamos a esta pregunta. Cuando perdemos a alguien, cuando enfrentamos una enfermedad, cuando sentimos ese vacío en el pecho, cuando nos damos cuenta de lo frágil que es la existencia, todo desaparecerá. Desaparece para siempre lo que sentimos como yo o hay algo en nosotros que continúa silenciosamente más allá de la materia. Durante mucho tiempo, la ciencia prefirió no ocuparse de esto. Todo lo que no se puede pesar, medir o aislar en un laboratorio, se considera irrelevante o fantasioso. Pero, ¿es esto realmente honestidad científica o simplemente miedo a lo que no podemos controlar? Grandes mentes de la humanidad, desde los filósofos hasta los físicos, se han atrevido a afrontar esta pregunta con valentía. Y entre ellos estaba Albert Einstein. Él, que tanto habló del universo, no ignoraba lo que existe dentro de nosotros. El alma para él no era una creencia ciega, sino una posibilidad real conectada con la esencia de todo. Cuando nos detenemos a pensar más profundamente, nos damos cuenta, no es una cuestión de religión o doctrina. Se trata de identidad sobre lo que somos cuando nadie nos mira. Cuando cerramos los ojos por la noche sentimos que hay algo en nosotros que va más allá del cuerpo físico. Esta pregunta, ¿a dónde va el alma? No es solo filosófico, cambia la forma en que vivimos en el ahora. Porque si el alma continúa, entonces cada elección, cada gesto, cada pensamiento tiene un peso que va mucho más allá de este momento. Y quizá la respuesta que buscamos no esté afuera, sino dentro de nosotros todo el tiempo. Einstein y la visión de que todo es energía. Albert Einstein revolucionó la forma en que entendemos el universo. Demostró que la materia y la energía son en realidad dos caras de la misma moneda y más. Todo lo que existe, incluido lo que llamamos sólido, está compuesto de energía en diferentes niveles de vibración. Esto lo cambia todo. Porque si estás hecho de energía y la energía nunca se destruye, ¿qué dice eso sobre el final de la vida? Quizás no sea un final. sino una transformación. Y si el alma es exactamente eso, un campo energético que se reorganiza, que pasa a otra dimensión cuando el cuerpo ya no la sostiene. Einstein no era un hombre religioso en el sentido tradicional, pero tenía un profundo respeto por el misterio del universo. Creía que Dios no juega a los dados con el mundo, sugiriendo que hay un orden, una inteligencia, una conexión detrás de todo. Cuando dijo que todo es energía, nos estaba abriendo una puerta para que entendiéramos que el alma, la conciencia, el yo más profundo, no pueden desaparecer, simplemente cambian de forma, como el vapor que surge del agua o la semilla que muere para convertirse en árbol.
.La vida continúa, solo que en otro estado. Esta visión nos invita a pensar de manera diferente, dejar de tratar la vida como algo mecánico y fugaz y empezar a verla como un proceso de expansión. Si todo es energía y la energía se transforma, entonces quizás solo estemos experimentando una de las muchas fases de nuestra existencia. nos da coraje, da propósito, porque lo que sientes, amas, piensas, construyes, todo eso deja huellas que no se pierden en el tiempo. No eres una oportunidad, eres parte de una energía viva e inteligente que pulsa a través de todas las cosas. La frase de Einstein sobre la imposibilidad de destruir la energía. Una de las leyes más poderosas de la física dice que la energía no se puede crear ni destruir, solo transformar. Y esta idea, que ya sería impresionante en sí misma, se vuelve aún más fascinante cuando se aplica al alma. Si somos energía, como creía Einstein, entonces no dejamos de existir. Cambiamos, evolucionamos, trascendemos. Esta sencilla frase de la física se convierte en un poema sobre la eternidad. No es una promesa religiosa, es un principio universal. Lo que somos en esencia nunca desaparece y esto cambia por completo la forma en que vemos la vida y la muerte. Piense en una vela encendida. Cuando la llama se apaga, ¿a dónde va la luz? No deja de existir, simplemente se dispersa. De la misma manera, cuando una persona muere, quizás su esencia, su energía, continúa vibrando en otro plano de otra manera. El cuerpo es solo el contenedor. Lo que nos mueve por dentro, el amor, la conciencia, el propósito. Todo eso puede continuar incluso cuando el cuerpo físico ya no responde. Esta es la belleza de la visión de Einstein. No niega la ciencia, pero tampoco cierra los ojos al misterio. ¿Cuántas veces has sentido la presencia de alguien que ya no está? ¿O tuviste una intuición tan fuerte que parecía venir de otro lugar? Y esas extrañas coincidencias que parecen señales. La idea de que la energía no muere nos ayuda a comprender que hay un hilo invisible que todo lo conecta. Einstein no nos dio respuestas definitivas sobre el alma, pero nos dejó pistas. Y a nosotros nos corresponde seguirlos con el corazón abierto, porque quizás al comprender que la esencia no se puede borrar, podamos vivir con más coraje, más dedicación y más sentido. La diferencia entre el Einstein de la ciencia y el Einstein de la conciencia. Mucha gente conoce a Einstein solo como el científico de fórmulas complicadas, pelo despeinado e ideas que cambiaron la física. Pero hay otro lado de el que pocos exploran. El hombre que miraba el universo con asombro espiritual, que creía en un orden invisible, en algo más grande de lo que los seres humanos pueden comprender. Dijo que el sentimiento más hermoso que podemos experimentar es el misterio. Es la fuente de todo verdadero
arte y ciencia. Esta frase revela a un Einstein que no solo quería descifrar ecuaciones, sino comprender el significado de la existencia. Este lado más humano y reflexivo del genio no tiene cabida en los libros de física. Surgen sus cartas, entrevistas, conversaciones íntimas. Un hombre que hablaba del alma, la intuición, la emoción y que veía la espiritualidad como una dimensión profunda de la realidad, incluso si no encajaba en las religiones organizadas. Einstein creía que hay algo más grande que gobierna el universo y que vivir sin buscar esta conexión era como morir en vida. Para él, la mente racional tenía sus límites y solo el sentimiento de reverencia ante el misterio podía ampliar nuestra comprensión de la vida. Esta dualidad entre científico y buscador es lo que hace que su figura sea tan poderosa. Einstein representa el puente entre dos mundos, el de la razón y el de la conciencia. Y tal vez sea exactamente esta unidad la que nos falta hoy. Cuando miramos el alma con los ojos de la ciencia y la ciencia con el corazón del alma, descubrimos que no estamos separados del universo. Somos parte de él. La misma energía que mueve las estrellas pulsa dentro de ti. No se trata de creer ciegamente, sino de permitirse sentir lo invisible. Conexiones entre el alma, la
conciencia y la frecuencia vibratoria. Si todo es energía, como dijo Einstein, entonces todo vibra, incluidos nuestros pensamientos, sentimientos e intenciones. Esta idea, que puede parecer abstracta, está cada vez más presente en los estudios modernos de física y neurociencia. Cada emoción tiene una frecuencia. El amor, por ejemplo, vibra más alto que el miedo. La gratitud eleva más que la ira y la consciencia quizás es exactamente eso, una vibración única que nos conecta con una dimensión superior. El alma, en este contexto no sería una entidad separada, sino una frecuencia que sobrevive al cuerpo físico. Piense en una radio. Al girar la perilla, sintonizas diferentes estaciones, incluso si todas están al aire. Lo mismo puede suceder con el alma. El cuerpo sería solo el dispositivo y la consciencia, la frecuencia. Cuando el cuerpo desaparece, la frecuencia no desaparece, simplemente deja de escucharse en ese canal. Esta es una manera poderosa de entender que la muerte puede ser simplemente un cambio de tono y no un final. La energía continúa, el alma continúa y quizá incluso se expandirá de maneras que aquí no podemos comprender. Esta visión nos invita a cuidar mejor nuestro estado interno. Después de todo, si nuestra alma vibra, entonces todo lo que sentimos y pensamos interfiere con nuestra frecuencia. Cargar con dolor, vivir con miedo, negar lo que sentimos. Todo esto nos desconecta de quiénes somos realmente. El amor, la presencia, la búsqueda de un propósito elevan nuestra vibración y cuanto más nos alineamos con esto, más cerca estamos de nuestra esencia. El alma, como creía Einstein, no es un concepto místico. Es una realidad que late dentro y fuera de nosotros y que responde a la frecuencia que elegimos emitir. Testimonios y teorías ignoradas por la ciencia tradicional. A pesar de tanta evidencia, historias y experiencias, la ciencia tradicional todavía se resiste a reconocer aquello que no se puede poner bajo el microscopio. Pero hay miles de informes de todo el mundo de personas que han tenido experiencias cercanas a la muerte y han quedado con una clara sensación de conciencia continua. Describen sentimientos de paz, lucidez, encuentros con seres queridos. Todo ello en momentos en los que el cerebro teóricamente ya no funcionaba. ¿Cómo explicar esto? Ignorar es fácil. Investigar requiere coraje. Además, muchos investigadores y científicos ya han intentado explorar esta frontera entre materia y conciencia. El neurocirujano Dr. Even Alexander tuvo una experiencia cercana a la muerte que desafió todo en lo que creía como médico. Regresó convencido de que la conciencia no se limita al cerebro. Rupertraque, físico y biólogo, habla sobre campos morfogenéticos y conexiones invisibles entre los seres vivos. Estas son ideas que desafían los modelos rígidos, pero quizás estén mucho más cerca de la verdad de lo que imaginamos. Y aunque no estén en los libros escolares, estas voces resuenan cada vez más fuerte. La propia historia demuestra que las grandes verdades al principio siempre fueron ridiculizadas. Galileo fue condenado por afirmar que la Tierra giraba alrededor del Sol. Paster fue ignorado por hablar de microorganismos. ¿Qué pasa si hoy ignoramos otra verdad fundamental? Que el alma existe, que la conciencia continúa y que hay algo más allá de lo que podemos tocar. Einstein no ignoró lo invisible. creía que hay más misterios entre el cielo y la tierra de los que la lógica puede comprender y tal vez al dejar espacio a lo inexplicable podamos acercarnos a quiénes somos realmente. ¿Por qué se evitaron o silenciaron estas ideas? A menudo, aquello que no se puede medir con precision es descartado inmediatamente por la ciencia tradicional. Existe un miedo antiguo, casi inconsciente, a todo aquello que escapa al control y a la lógica. Hablar del alma, la eternidad y el propósito es incómodo porque obliga a la humanidad a salir de su zona de confort. Y cuando una idea amenaza con sacudir estructuras muy antiguas, ya sean religiosas, científicas o sociales, la reacción es casi siempre la misma, negarla, ridiculizarla o ocultarla. No porque sea mentira, sino porque es demasiado peligroso para aquellos que quieren mantener todo como está. Einstein lo sabía, fue reconocido por sus fórmulas y descubrimientos, comprendió que algunas verdades no podían decirse abiertamente. En cartas personales y conversaciones íntimas habló sobre Dios, el alma, el propósito y el misterio, pero en público era cuidadoso, porque hasta un genio puede ser desacreditado si se atreve a tocar temas que confrontan paradigmas. La historia está llena de pensadores que fueron silenciados no porque estuvieran equivocados, sino porque se adelantaron a su tiempo. Y tal vez las ideas de Einstein sobre el alma fueron solo susurradas, esperando a alguien con el coraje de escucharlas. Vivimos en una era donde todo necesita tener una explicación inmediata, un gráfico, una estadística. Pero, ¿qué pasa si las verdades más importantes se sienten, no se miden? Y si lo que realmente transforma al ser humano no es lo que se prueba en el laboratorio, sino lo que resuena en el alma. Cuando la ciencia se cierra a estas cuestiones se limita, pero cuando se abre al misterio se expande. Einstein entendió esto. Sabía que el verdadero conocimiento no es el que nos hace dueños de la verdad, sino el que nos hace humildes ante lo desconocido. La búsqueda del sentido de la vida según Víctor Frankl. Mientras Einstein exploraba leyes del universo, Víctor Franti profundizaba en el alma humana. Sobrevivió a los campos de concentración nazis, incluso en medio del dolor extremo descubrió algo esencial. Los seres humanos son capaces de soportar cualquier sufrimiento siempre que encuentren en él un significado. Y cuando combinamos esta visión con la idea de que el alma continúa más allá de la muerte, todo se conecta. No estamos aquí por casualidad. Nuestra existencia tiene un propósito mayor y entender esto es como encender
una luz en medio del caos. Frankl decía que la verdadera libertad del hombre reside en elegir su actitud ante lo que sucede. Creía que el sufrimiento, lejos de ser un mero dolor sin sentido, puede transformarse en crecimiento, en profundidad, en misión. Si el alma es eterna, como sugirió Einstein, entonces cada experiencia que vivimos, por difícil que sea, tiene un valor que trasciende esta vida. Somos más que eventos, estamos evolucionando procesos y buscar el significado es la manera más elevada de honrar ese viaje. ¿Cuántas veces has sentido que tu dolor tenía algo que enseñar? que ese momento difícil te moldeó por dentro de una manera que nada más podría haberlo hecho. Frany llamó a esto logoterapia, la terapia del significado. Y cuando combinamos esta visión con la idea de que el alma no muere, nos damos cuenta cada elección, cada gesto, cada caída tiene un peso eterno. No estás aquí solo para sobrevivir. Estás aquí para transformarte. Y todo lo que te pase puede ser materia prima para eso. Y si Einstein tuviera razón, ¿cómo cambia esto tu vida hoy? Imaginemos por un momento que todo esto es cierto, que el alma realmente existe. Esa conciencia continúa. Que la energía que te mueve no se desvanezca, simplemente se transforme. ¿Cómo cambiaría esto la manera en que vives tu día? Quizás perdonarías más rápido. Gracias más a menudo. Cuida mejor tus pensamientos, tus palabras, tu tiempo. Porque entender que la vida no termina con la muerte es también entender que todo lo que hacemos deja una huella, una vibración que sigue resonando. ¿Qué pasaría si supieras que cada acto de amor, cada elección intencionada, cada momento de presencia permanece en la esencia de tu alma? ¿Perdarías tanto tiempo en luchas vacías? Pequeños miedos o exigencias sin sentido. La visión de Einstein, al sugerir que el alma no se pierde, nos da una enorme responsabilidad, vivir con conciencia para nutrir lo eterno que hay en nosotros. Porque al final del día nada material se va con nosotros. Pero lo que somos continúa. No estás aquí por casualidad. Tu alma no es un accidente. Hay un movimiento mayor, una danza cósmica de la que eres parte. Y si Einstein tenía razón, si su energía realmente no se apaga, entonces todo cambia. Vivir se convierte en un acto sagrado. Respirar, un privilegio. El amor una misión. Y cada nuevo día, una oportunidad para hacer tu alma más ligera, más vibrante, más conectada con lo que realmente importa. Llegado a este punto, quizás ya te hayas dado cuenta, este vídeo no trata solo de Einstein ni solo del alma. Se trata de ti, de lo que llevas dentro, de lo que te mueve incluso en los días más difíciles, de lo que queda cuando todo a tu alrededor parece desmoronarse. Si la energía del alma no se desvanece, como creía Einstein, entonces su existencia es mucho más que una casualidad pasajera. Eres parte de algo más grande, un fragmento del universo único e irreemplazable. Y todo lo que experimentas, sientes y construyes tiene un significado que va mucho más allá de lo que los ojos pueden ver. Esta visión nos hace libres. Nos recuerda que no estamos limitados a nuestros cuerpos, nuestro tiempo, nuestras circunstancias. Tu historia tiene valor. Tu dolor tiene un propósito. Tu búsqueda de significado es en realidad una señal de que el alma está viva y quiere evolucionar. La muerte ya no debe temerse como un final, sino entenderse como una transición. Y aunque ese momento no llegue, depende de ti vivirlo con valentía, con dedicación, con amor. Porque cada pensamiento, cada elección, cada gesto tiene eco aquí y más allá.
El alma no muere. Ella simplemente continúa lo que vino a comenzar. Si este mensaje te resonó, suscríbete al canal ahora. Aquí todos los días te traemos reflexiones que fortalecen tu alma y amplían tu conciencia. Y aprovecha para dejar una palabra en los comentarios que represente lo que crees que continúa después de la muerte. Vayamos juntos en este viaje de transformación.
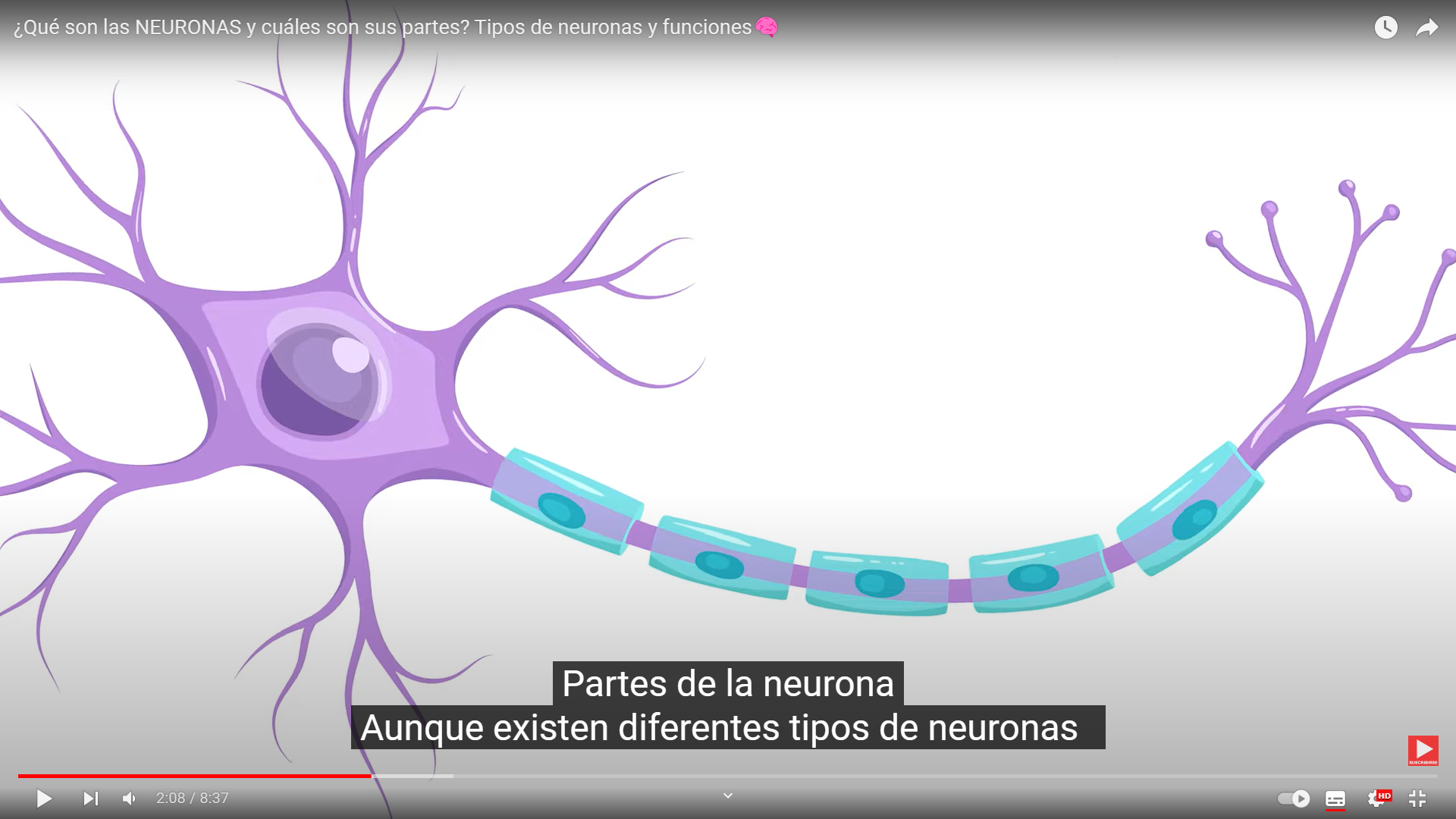

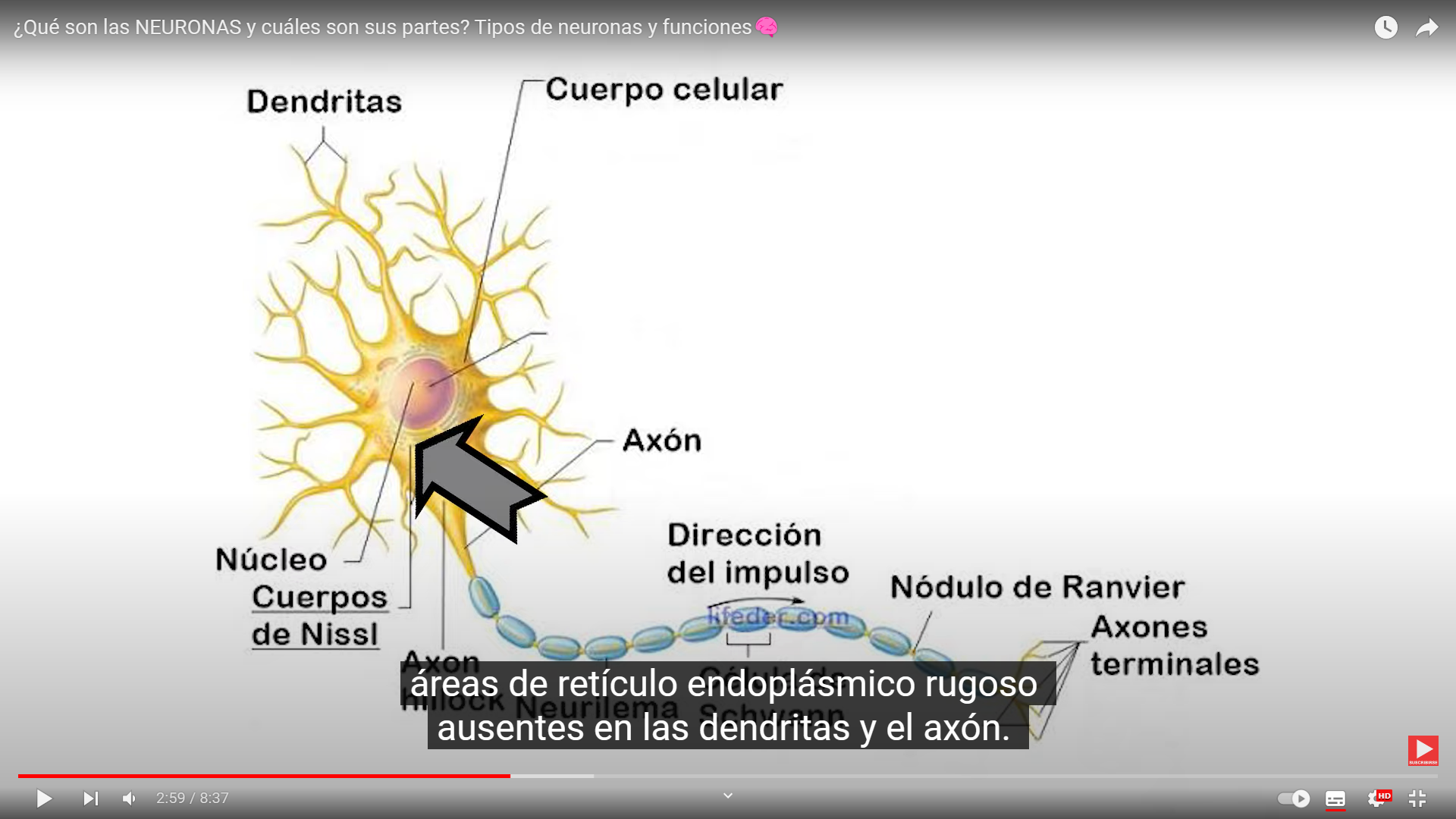
 Estos activan enzimas y las enzimas activadas, se mueven en torno a la célula provocando con la ayuda de otras enzimas una reacción en cadena las enzimas actúan como una especie de equipo de construcción cambiando la estructura de los receptor.
Estos activan enzimas y las enzimas activadas, se mueven en torno a la célula provocando con la ayuda de otras enzimas una reacción en cadena las enzimas actúan como una especie de equipo de construcción cambiando la estructura de los receptor.