 Terapia con linfocitos T-CAR:
Terapia con linfocitos T-CAR:
Representación de cómo el linfocito Tarmado con un receptor de antígeno quimérico (CAR) se une a la célula tumoral.
Terapia con linfocitos T-CAR:
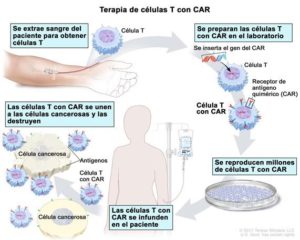
Terapia de células T con CAR es el tipo de tratamiento en el que las células T del paciente se modifican en el laboratorio para que ataquen células cancerosas. Las células T se extraen de la sangre del paciente, y en el laboratorio, se les añade el gen para un receptor especial que se une a cierta proteína de las células cancerosas del paciente. Este receptor especial se llama receptor de antígeno quimérico (CAR, del inglés «chimeric antigen receptor»). Grandes cantidades de células T con CAR se producen en el laboratorio y se administran al paciente mediante infusión. La terapia de células T con CAR está en estudio para el tratamiento de algunos tipos de cáncer. También se llama terapia de células T con receptor de antígeno quimérico.
Con la terapia de células T con CAR. se cambian las células T (un tipo de célula inmunitaria) de un paciente en el laboratorio a fin de que se unan a las células cancerosas y las destruyan. La sangre de una vena del brazo del paciente pasa por un tubo hasta una máquina de aféresis que extrae los glóbulos blancos, incluso las células T, y devuelve el resto de la sangre al paciente. Luego, en el laboratorio, se inserta en estas células T el gen que produce un receptor especial, que se llama receptor de antígeno quimérico (CAR). Se reproducen millones de células T con CAR en el laboratorio y después el paciente las recibe mediante infusión. Las células T con CAR se unen a un antígeno de las células cancerosas y las destruyen.
La infusión de células T con receptores de antígeno quimérico es hoy un exponente de la medicina de precisión y de vanguardia. La investigación, académica y de la industria, abre nuevas indicaciones para esta terapia.
Representación de cómo el linfocito Tarmado con un receptor de antígeno quimérico (CAR) se une a la célula tumoral. El
LaTerapia con linfocitos T-CAR
consiste en modificar genéticamente los linfocitos T del propio enfermo para que expresen receptores quiméricos (CAR) que, una vez reinfundidos en el paciente, se unan a las células tumorales, proliferen y las destruyan.
La terapia con T-CAR es una medicina personalizada y aúna elementos de terapia génica, celular y de inmunoterapia.
Más de 80 pacientes en España han recibido ya terapia con células T-CAR, un tratamiento que por el momento se extiende a tumores hemtologicos, pero tiene un amplio porvenir en tumores solidos.
El cáncer hematológico concentra, en la actualidad sus indicaciones. En concreto, el tratamiento se administra en la leucemia linfoblástica aguda y en el linfoma no hodgkiniano difuso de célula B grande y primario de mediastino, después de que hayan fracasado varias líneas de tratamiento. Es en estas hematopatías donde pueden ofrecer perspectivas de supervivencia a pacientes cuyo pronóstico, sin recibir el tratamiento, no rebasa las semanas. El Grupo Español CAR de la Sociedad Española de Hematología y Hemoterapia (SEHH), Álvaro Urbano Ispizúa, recuerda que las células T-CAR no son la panacea ni curarán todos los cánceres, si bien, vista su rápida evolución en los el gen últimos años, es de esperar que se consoliden y amplíen sus indicaciones.
Tanto la industria como los generados en los hospitales (académicos), con los que Ispizúa-Urbano ha sido pionero en el Hospital Clínico de Barcelona. Este grupo de médicos ha puesto en marcha el ensayo clínico público ARI, en el que han participado 26 pacientes con leucemia linfoblástica aguda, obteniendo excelentes resultados. Este ensayo se ha ampliado a otros centros españoles con el fin de consolidar los resultados obtenidos en la fase I.
Según la SEHH, también se preparan otros tres ensayos clínicos públicos: un estudio multicéntrico en el Hospital Clínico sobre mieloma múltiple; uno sobre linfoma de Hodgkin y no Hodgkin en el Hospital de la Santa Cruz y San Pablo, y otro en el Hospital Universitario de La Paz para diferentes cánceres hematológicos y sarcoma. Por otra parte, están abiertos 19 ensayos clínicos comerciales, en los que participan doce centros españoles de Madrid, Barcelona, Salamanca y Sevilla. Asimismo, varios centros españoles han puesto en marcha investigaciones en fase preclínica con terapia T-CAR.
Los investigadores se preguntan cuánto tiempo va a durar el beneficio de esta terapia y si es extendible este beneficio a los tumores solido e incluso en otras enfermedades
Los buenos resultados obtenidos en la patología hematológica despertaron el interés de las T-CAR en los tumores sólidos.
En nuestro país ya hay abiertos ensayos en glioblastoma y cáncer de pulmón, y a nivel internacional, se está empezando a explorar, además de en esos tumores, en el cáncer pancreático, en mesotelioma y en el cáncer de mama, entre otros.
Los principales obstáculos para que estas terapias funcionen en la enfermedad oncológica, sino un Lincoln el mundo por un gol uno el con un poco el mundo un genio la donde se resumen en un microambiente hostil, la heterogeneidad intratumoral y dar con la vía efectiva de administración. Las células T-CAR se mueven en los fluídos con más libertad que en el tumor sólido, que está parapetado en entornos acidificados, hipóxicos e inmunosupresores.
Todas esas barreras dificultan a los linfocitos que puedan infiltrarse y perdurar. Además, la heterogeneidad de los tumores sólidos cuestiona que un mismo tipo de linfocito T-CAR, diseñado para dirigirse a un antígeno concreto, sea suficiente para unirse a todas y cada una de las células de un tumor. La selección de esta molécula es crítica, pues además de poder actuar frente al cáncer tiene que resultar inocua para las células del tejido sano. En ello investiga ahora el equipo que ideó esta terapia, el grupo de Carl June en la Universidad de Pensilvania -donde se trató al primer paciente con T-CAR en 2010-. Estos científicos están desarrollando un tipo de T-CAR que en lugar de hacia el antígeno CD19, presente en las células B, actúe frente al receptor del factor de crecimiento epidérmico (EGFR), en concreto a una parte que solo está presente en las células del glioblastoma.
Por otra parte, la fácil infusión de células en la enfermedad hematológica se convierte en una difícil decisión en el cáncer: ¿vía sistémica o intratumoral? Al margen de que no basta una sola dosis, se requieren múltiples sesiones de administración de las células.
A pesar de todos estos obstáculos, hay ejemplos de tentativas esperanzadoras, como la administración intraventricular de estas células en pacientes con glioblastoma, iniciada hace cuatro años en el Hospital City of Hope, en Los Ángeles, o, sin dejar Estados Unidos, la infusión sistémica de T-CAR dirigida a pacientes con sarcoma en la Universidad Baylor de Houston, y el tratamiento de enfermos con mesotelioma, mediante la introducción local de las células, en un ensayo llevado a cabo en el Centro del Cáncer Memorial Sloan Kettering, en Nueva York.
CAR alogénicas, NK-CAR e indicaciones en otras enfermedades
La terapia con linfocitos T a los que se añade un receptor quimérico CAR –de ahí, por cierto, “CAR-T”– es el inicio de una estrategia que está en plena evolución. De hecho, los linfocitos T no serán el único tipo al que se añada el receptor. Se está investigando en el empleo de la célula citolítica natural NK (NK-CAR),que ofrecería como principal ventaja frente a los linfocitos T la posibilidad de almacenarlos congelados y utilizarlos en cualquier paciente.
El primer ensayo con células NK-CAR se llevó a cabo en 2016 en China en pacientes con diferentes tipos de cáncer; de momento, los resultados indican que la terapia es segura. Años más tarde, el Centro del Cáncer MD Anderson, en Houston, inició otro ensayo con estas células en linfoma y leucemia. Los médicos implicados en estos estudios destacan que con las células NK se evita la necesidad de extraerlas del paciente, si bien reconocen como principal objeción que el periodo en el que estas células resultan útiles frente a las tumorales es más limitado que el de los linfocitos T.
También la posibilidad de que las células T-CAR sean alogénicas se está explorando, al igual que la opción de combinarlas con agentes inmunopotenciadores. Ya ha llegado al ensayo clínico la suma de la terapia con T-CAR e inhibidores de punto de control (checkpoint) en tumores sólidos.
El ámbito no oncológico, y en concreto la autoinmunidad, es otra de las paradas que se aventuran para estas terapias de vanguardia. Un equipo en la Universidad de Tennessee, en Memphis, ha demostrado, en modelos experimentales, que los linfocitos T-CAR podrían reducir los síntomas más graves del lupus.
Es impresionante el número de fármacos que se están investigando para tratar los tumores, pero en la vers elatilidad y capacidad de cambio de las células de los t elumores sigue el siendo un desafio