OMOMYC TIENE EFECTO ANTI-TUMORAL EN TODOS LOS MODELOS DE CÁNCER
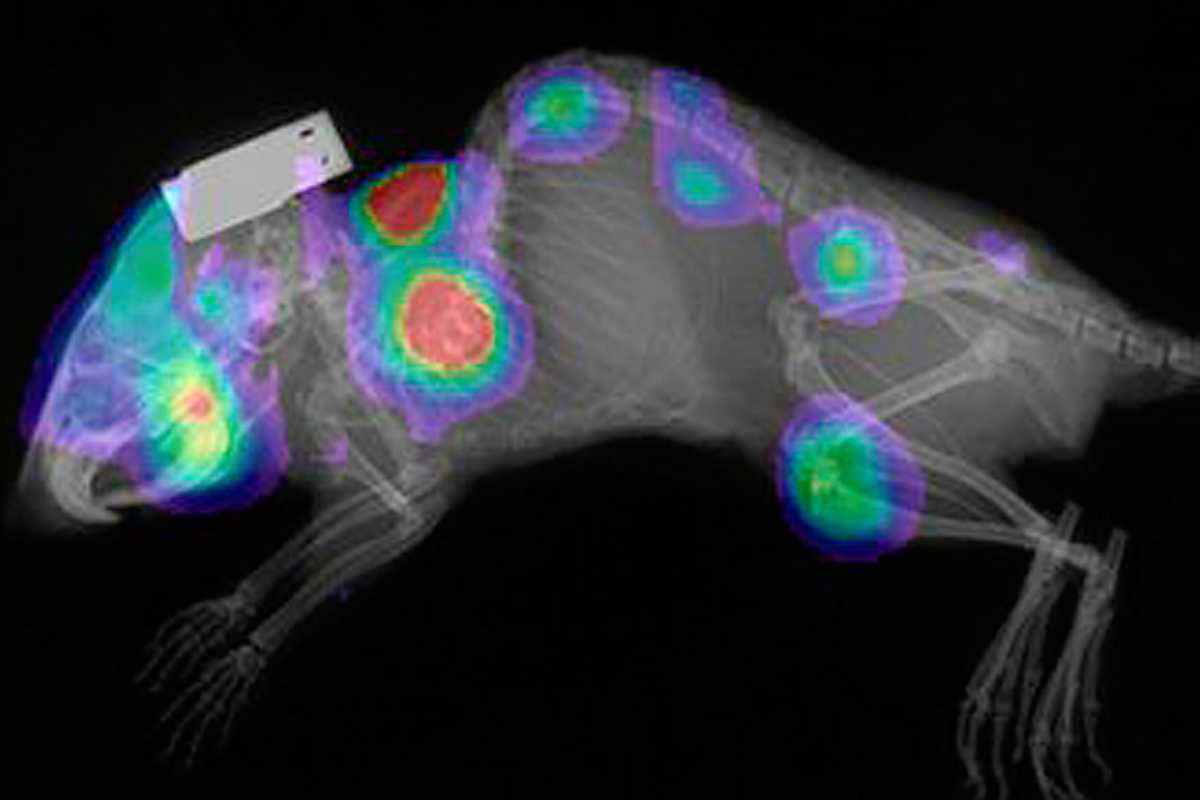
Ratón con cáncer de mama y metástasis, similar al modelo usado por el VHIO. 
El gen MYC “se encuentra implicado en el crecimiento de muchos tipos de tumores, pero había que demostrar que inhibir a MYC mediante Omomyc tiene un efecto anti-tumoral en todos los modelos de cáncer que hemos utilizado hasta ahora, principalmente células tumorales humanas en cultivo y modelos de ratón”, y esto parece demostrarse por
Daniel Massó, investigador de la spin-off Peptomyc del Vall d’Hebron Instituto de Oncología (VHIO) y primer autor de un nuevo artículo sobre esta potencial terapia oncológica publicado en Cancer Research Communications, que confirma la utilidad de esta proteína terapéutica también en metástasis en cáncer de mama.
MYC es una proteína que está implicada en varios procesos del cáncer: proliferación celular, metabolismo, bloqueo de la respuesta inmune contra el tumor, etc. Pero también está implicada en las distintas fases del proceso metastático .
El Omomyc bloquea todos los procesos en los que MYC esta involucrado e incide tanto en tumores primarios como en metástasis.
MYC desempeña una función importante en el desarrollo de muchos tipos de tumores, pero no está claro si puede afectar al desarrollo de las metástasis y algunos estudios sugieren incluso que inhibir a MYC podría potenciar la metástasis.
El nuevo trabajo del VHIO aporta, por primera vez, evidencia sobre esta cuestión: Omomyc, proteína inhibidora de MYC, ofrece resultados “muy positivos” ante la progresión del cáncer de mama metastásico.
El VHIO ha informado de que ha realizado diferentes experimentos tanto in vitro como in vivo para conocer de qué manera Omomyc impactaba en las metástasis del cáncer de mama. “La respuesta ha sido muy positiva y en todos los casos se ha podido comprobar que Omomyc tiene una importante actividad antimetastásica, en contra de lo que se había especulado”,.
Se había demostrado que Omomyc era eficaz controlando muchos tumores primarios. Ahora, además, se demuestra que también es un fármaco eficaz al bloquear la invasión, el establecimiento y el crecimiento de las metástasis en el cáncer de mama”,
El VHIO recuerda que hace décadas que la investigación oncológica puso de manifiesto que el gen MYC tiene una importante función en el desarrollo de la práctica totalidad de los tumores sólidos pero que la creencia generalizada era que se trataba de una diana inalcanzable. “Todo cambió hace más de 20 años, cuando Laura Soucek se planteó que esto no tenía por qué ser así. Fruto de su esfuerzo y trabajo nació Omomyc, una miniproteína capaz de inhibir a MYC, que, tras múltiples estudios preclínicos cuyos resultados han dado la vuelta al mundo, ya se está probando en pacientes, en un ensayo clínico iniciado en mayo del año pasado en VHIO”,. Previo al ensayo, Omomyc ya había demostrado una potente actividad antitumoral en múltiples líneas de células tumorales y modelos de cáncer en ratón, independientemente de su tejido de origen y de sus mutaciones.
Laura Soucek, artífice del ‘Omomyc’: “En ciencia, no debería haber ideas preconcebidas”
Arranca el primer ensayo clínico en España con una innovadora terapia celular para cáncer
Centros europeos desarrollan una plataforma virtual para seleccionar terapias oncológicas
Todos los trabajos de investigación realizados hasta ahora con este fármaco se han centrado en tumores primarios y nunca se había probado su eficacia contra la enfermedad metastásica. “Algunos estudios sugerían que MYC podía desempeñar una función antimetastásica, por lo que su inhibición podría ser perjudicial. Pero los datos que hemos obtenido en nuestra investigación muestran todo lo contrario”, apunta Massó, quien ha añadido que, aun así, existían algunas cuestiones que invitaban a ser optimistas sobre la posible eficacia de Omomyc para controlar las metástasis.
“Las metástasis son genéticamente inestables, lo que significa que la información del tumor primario de un paciente puede no reflejar con precisión las metástasis, que además pueden variar de unas a otras. Esto supone una importante barrera para las terapias dirigidas. El hecho de que la inhibición de MYC sea eficaz independientemente del perfil mutacional del tumor hizo que los investigadores del VHIO se plantearan que el uso de este enfoque podría superar la barrera de la heterogeneidad de las metástasis. Además, MYC promueve dos aspectos clave de la metástasis, la transición epitelio-mesenquimal y la desdiferenciación, lo que sugiere que su inhibición podría revertir estas características e inhibir las metástasis cuando estas se empiezan a formar”, asegura el centro.
Para poder demostrar estas hipótesis, se plantearon una gran multitud de experimentos. Se realizaron pruebas tanto en modelos in vitro como en modelos de ratón. En los primeros se probó la eficacia en todos los tipos de tumores, mientras que en los segundos el trabajo se centró en el cáncer de mama triple negativo, una enfermedad que necesita urgentemente mejores opciones terapéuticas.
Para comprobar los resultados de la terapia se emplearon diferentes modelos y técnicas de imagen que permitían medir el desarrollo de los tumores. “ En ratones modificados genéticamente, Omomyc era capaz de hacer que el tumor primario creciera menos pero también observamos que impactaba en el crecimiento de las metástasis y en algunos casos las hacía desaparecer. Cuando administramos Omomyc por vía intravenosa, los resultados también fueron positivos ya que vimos que se producía una disminución del crecimiento del tumor y que se alargaba significativamente la supervivencia de los ratones”, dice Massó.
Todavía no se ha llevado a cabo con pacientes, el trabajo realizado por VHIO ha querido analizar también la posible repercusión de la aplicación de Omomyc. Para ello se analizaron bases de datos de pacientes, en las que se pudo comprobar que aquellas pacientes de cáncer de mama que presentaban sobreexpresión de los genes que bloquea Omomyc tenían una supervivencia más baja. “Esto nos hace ser optimistas y pensar que, si estas pacientes se tratasen con nuestro fármaco, quizá podríamos mejorar su supervivencia”, concluye Massó.
Bibliografia
Daniel Massó, investigador de la spin-off Peptomyc del Vall d’Hebron Instituto de Oncología (VHIO) Cancer Research CommunicationsDaniel Massó, investigador de la spin-off Peptomyc del Vall d’Hebron Instituto de Oncología (VHIO)
Life Sciences, Healthequity, CDTI, Aurora Science y Business Angels
Carmen Fernández. Barcelona
Mar, 22/02/2022 – 12:44
Laura Soucek, codirectora de Investigación Traslacional y Preclínica y jefa del Grupo de Modelización de Terapias Antitumorales del VHIO y Violeta Serra y Joaquín Arribas. del VHIO