MEJORAR LA EFICACIA DE LA RADIOTERAPIA EN METÁSTASIS CEREBRALES
Un estudio del CNIO desvela que con un análisis de sangre se puede conocer qué pacientes se van a beneficiar de la radioterapia cerebral.
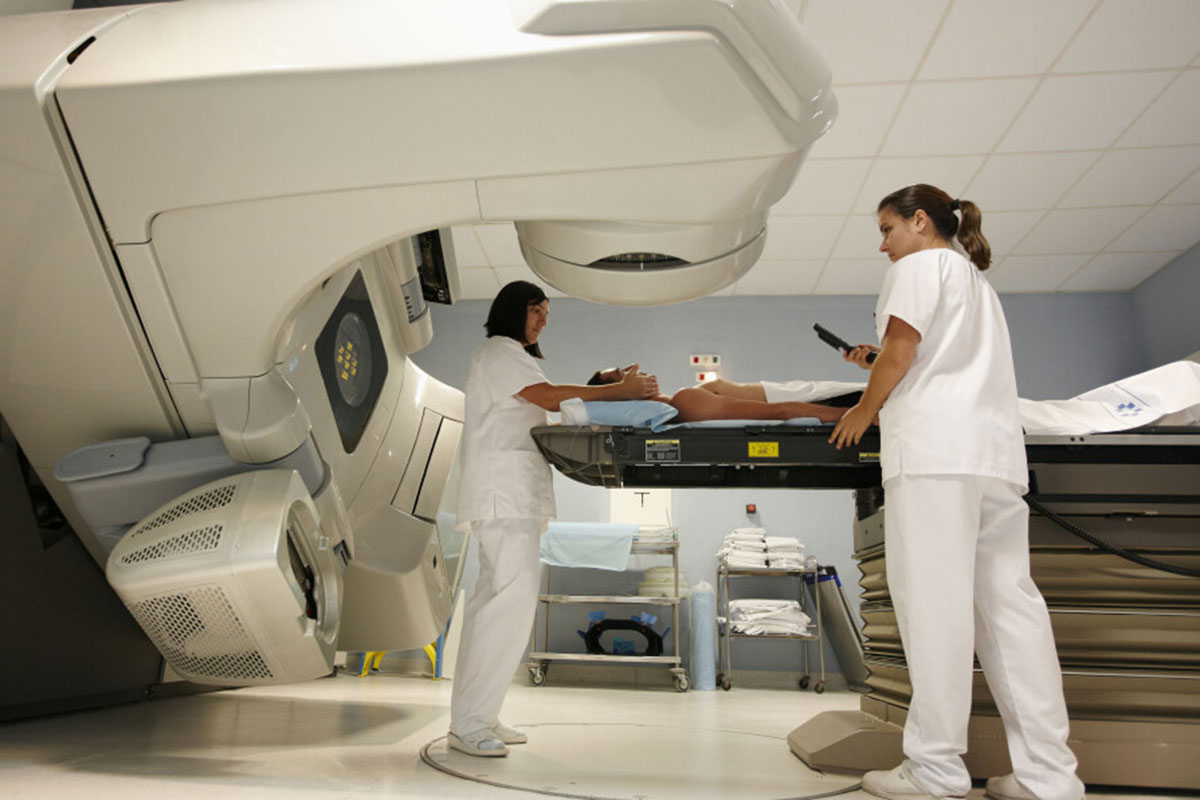 La radioterapia es una opción habitual en el tratamiento de las metástasis cerebrales. Foto: AGEFOTOSTOCK.
La radioterapia es una opción habitual en el tratamiento de las metástasis cerebrales. Foto: AGEFOTOSTOCK.
Entre el 20% y el 40% de los pacientes con cáncer (tumores de pulmón, mama y melanoma, entre otros) desarrollan una metástasis cerebral, para la que uno de los abordajes más empleados es la radioterapia.
Un equipo de investigadores del Centro Nacional de Investigaciones Oncológicas (CNIO) ha identificado una nueva estrategia que, a través de una sencilla prueba, puede mejorar la eficacia del tratamiento radioterápico.
Los autores del trabajo han descubierto que basta un análisis de sangre para identificar a pacientes resistentes a radioterapia, antes de recibirla, y han encontrado un fármaco que podría revertir esa situación. Ya han comenzado un ensayo clínico multicéntrico para validar el biomarcador a través de la Red Nacional de Metástasis Cerebral (Renacer).
Manuel Valiente, jefe del Grupo de Metástasis Cerebral del CNIO y autor principal de esta investigación que se publica hoy en Nature Medicine, sintetiza a DM el hallazgo: “Hemos encontrado un mecanismo de resistencia en la radioterapia, uno de los tratamientos habituales de la metástasis cerebral. Gracias a ello, entendemos mejor los procesos moleculares que subyacen a ese proceso; estratificamos a los pacientes, atendiendo a si responderán o no a la radioterapia y, además, hemos encontrado un fármaco que podría hacer más sensible la metástasis a la radioterapia”.
El trabajo que dirige Manuel Valiente, cuyo laboratorio en el CNIO es todo un referente en la investigación en metástasis cerebrales, ha servido para identificar una vía molecular implicada en la aparición de resistencia, en concreto la proteína S100A9, que funciona como indicador de la sensibilidad a la radioterapia: a mayor presencia de S100A9, más resistencia a la radioterapia.
La sorpresa positiva ha sido el comprobar que dicha proteína puede detectarse en sangre: “No esperaba que fuera tan sencillo −afirma Valiente−, la cantidad de S100A9 en sangre correlaciona con la resistencia a la radioterapia”.

Grupo de Metástasis Cerebral del CNIO. Foto: Laura M. Lombardía/CNIO.
Y siguiendo esa línea hacia la translación clínica de los hallazgos, el estudio también desvela que el receptor al que se une la proteína (denominado RAGE) cuenta con un inhibidor, un tipo de fármaco que ya se está ensayando en diversas patologías, entre ellas la enfermedad de Alzheimer.
“No hemos empleado exactamente el inhibidor de RAGE utilizado en estudios actuales de la enfermedad de Alzheimer, pero al usar uno similar, vimos que llega bien el cerebro”. El científico recuerda que una de las dificultades de los tratamientos que se dirigen al sistema nervioso central es que tienen dificultades para superar la barrera hematoencefálica. “Además, hemos comprobado en modelo animal que este inhibidor combinado con radioterapia no tiene un efecto negativo sobre la función cerebral, lo que supone otra gran ventaja para su empleo”.
Así, en modelos animales y en cultivos realizados a partir de muestras de pacientes, mediante el uso de METPlatform, han demostrado que este fármaco puede emplearse para lograr que los pacientes resistentes respondan a la radioterapia.
“Nuestros hallazgos presentan un nuevo enfoque para personalizar la radioterapia”, escriben los autores en la revista científica. Sobre su estrategia apuntan que “no sólo identifica a los pacientes que podrían beneficiarse de la radioterapia holocraneal [denominada así porque se aplica sobre todo el tejido cerebral, a diferencia de la radioterapia estereotáctica o radiocirugía, que se focalizan solo en el tumor], sino que también proporciona una terapia combinada para superar la radiorresistencia”.
Los siguientes pasos de esta línea de investigación, expone Valiente, incluyen “validar el biomarcador en sangre en una cohorte prospectiva de pacientes» para confirmar que, efectivamente, aquellos con niveles más elevados responden peor que los que tienen niveles bajos. Más adelante, una vez validado, podrán iniciar el ensayo con el fármaco.
“Contar con un biomarcador tiene implicaciones importantes, pues abre la puerta a realizar estudios clínicos para mejorar la administración de la radioterapia”, añade, con todo lo que ello supone para un grupo de pacientes que no cuentan con muchas opciones terapéuticas. Los inhibidores de la PI3K, eficaces en cáncer de mama
El grupo de investigación clínica en cáncer de mama Solti presentó en su cuarto encuentro, el pasado 16 de noviembre, nuevas posibilidades en el tratamiento del cáncer de mama metastásico. Eva Ciruelos, oncóloga médica de la Unidad de Cáncer de Mama del Departamento de Oncología y coordinadora de ensayos clínicos de esta patología en el Hospital Universitario 12 de Octubre de Madrid, fue la encargada precisamente de presentar los últimos agentes en desarrollo y las combinaciones más novedosas en este campo.
Así, Ciruelos explicó a GM que las presentaciones más novedosas de la jornada correspondieron a los inhibidores de la activación de la vía PI3K, que aparece alterada en “hasta un 30 por ciento de los casos de cáncer de mama”. Estos inhibidores, explica Ciruelos, podrían darse en monoterapia, en combinación con quimioterapia o incluso en combinación con tratamientos hormonales. Una noticia importante de la que José Baselga, presidente del Instituto de Oncología del Vall d’Hebron (VHIO) y director adjunto del Centro de Cáncer del Hospital General de Massachusetts, ya habló en la 7º Conferencia Europea sobre Cáncer de Mama, celebrada en marzo de 2010. En aquel momento, Baselga se refirió a esta vía como algo prometedor, pero todavía “en fase I en tumores hormonodependientes”. Ahora, dos años después, se empieza a ver que, efectivamente, inhibir esta ruta de señalización podría dar resultados.
HER2
Las últimas novedades en cáncer de mama de tipo HER2+ también fueron protagonistas del Encuentro, sobre todo gracias a los últimos resultados de los estudios Emilia (T-DM1, el conjugado trastuzumab y emtansina, ofrece una mejora significativa de la SLP y la SG en pacientes en segunda línea de tratamiento) y Cleopatra (la combinación de trastuzumab, pertuzumab y una quimioterapia mejora la SLP), ya presentados en el último Congreso de la Sociedad Americana de Oncología Médica (ASCO). La novedad ahora es la presentación de una actualización de este último estudio, Cleopatra, en el próximo Simposio de cáncer de mama que se celebrará en San Antonio, Texas, entre el 4 y el 8 de diciembre. Ciruelos espera que se presenten aquí datos en SG, unos resultados muy esperados por la comunidad científica. Además, actualmente también se investiga el valor de esta combinación en “pacientes operados sin metástasis, como tratamiento preventivo”, asegura Ciruelos.
Asimismo, también son muy esperados los resultados del estudio Marianne, del que Ciruelos espera tener los primeros resultados para finales de 2013. El estudio, en pacientes con cáncer de mama metastásico HER2+, ha dividido a las mujeres en trastuzumab con quimioterapia (brazo control), T-DM1 (brazo ganador del Emilia) y T-DM1 con pertuzumab (una combinación de los estudios Emilia y Cleopatra) con el objetivo de averiguar “si dar lo mejor que tenemos, pertuzumab y T-DM1 juntos, es mucho mejor que las otras dos opciones”, explica Ciruelos. De momento, la FDA acaba de aprobar la revisión prioritaria a T-DM1, y la EMA, por su parte, ha aceptado revisar su autorización de comercialización.
También los tumores HER2-, que afectan al 60 por ciento de la población, tuvieron su espacio en esta reunión. En este tipo de pacientes, la combinación de exemestano y everolimus, un fármaco inhibidor de las m-TOR cinasas, consigue mejoras significativas en pacientes que no habían respondido al tratamiento convencional con un inhibidor de la aromatasa como letrozol o anastrozol. De momento, en España, la única manera de conseguir tanto everolimus como pertuzumab es a través de un uso expandido.
Los inhibidores de PI3K podrían administrarse incluso en combinación con terapia hormonal
El estudio Marianne investiga la conveniencia de administrar T-DM1y pertuzumab juntos
Diagnóstico de mutaciones: cambio de paradigma en cáncer de mama
La medicina de precisión ya es un hecho. Detectar mutaciones genéticas no sólo ofrece terapias individuales. Refuerza el seguimiento y el control de las respuestas y resistencias a tratamientos.
 La detección temprana de lesiones mamarias favorece la supervivencia de las afectadas. Foto: AGEFOTOSTOCK.
La detección temprana de lesiones mamarias favorece la supervivencia de las afectadas. Foto: AGEFOTOSTOCK.
Raquel Serrano. Madrid Lun, 11/04/2022 – 13:00
El cáncer de mama, con ciertas variaciones geográficas, es el tipo de tumor más frecuente en mujeres de todo el mundo. Los últimos datos de la Sociedad Española de Oncología Médica (SEOM) señalan que en España se diagnosticaron alrededor de 34.088 nuevos cánceres de mama en el año 2020, lo que representa el 30% de los cánceres diagnosticados en mujeres.
No obstante, han sido muchos los factores que, a pesar de las notables tasas de incidencia, han permitido que las de supervivencia hayan mejorado progresivamente. Detecciones más precoces con herramientas diagnósticas que aportan mayor información, un mejor conocimiento molecular de los tumores y el aumento en la disponibilidad de terapias dirigidas han contribuido a plantar cara a este tumor, que cuenta con la participación, cada vez más sólida, de equipos multidisciplinares de especialistas, y absolutamente necesaria en la actual medicina de precisión.
El cribado ha sido uno de los grandes cambios en el control de esta enfermedad: permite un incremento del diagnóstico en estadios más iniciales, lo que facilita el inicio de estrategias de tratamiento de forma temprana que permiten abordajes quirúrgicos menos agresivos, por ejemplo.
En el caso concreto del cáncer de mama luminal, un estadio no avanzado es subsidiario, en muchos casos, de evitar el tratamiento quimioterápico, recurriendo exclusivamente al tratamiento hormonal.
Pero, además de los cribados -esenciales en cualquier proceso neoplásico-, las características genómicas y los subtipos histológicos-moleculares de los cánceres de mama han permitido seleccionar estrategias terapéuticas ‘a medida’; un fenómeno en el que se basa la medicina de precisión y en la que el análisis de la expresión de genes es decisivo para prevenir, diagnosticar y tratar de manera personalizada.
Los ejemplos de este abordaje genómico ya son una realidad en muchos tumores de mama con el descubrimiento de genes –BRCA o HER2, entre otros-, y de sus dianas terapéuticas específicas.
En el tipo luminal es donde con mayor frecuencia aparecen mutaciones en el gen PIK3CA. De hecho, es el gen mutado con más frecuencia en el cáncer de mama HR positivo/HER2 negativo. Aunque no suelen observarse en lesiones primarias, sí son bastante frecuentes en tumores metastásicos resistentes a la terapia endocrina de primera línea y de peor pronóstico. Por tanto, el análisis mutacional aparece, en estos casos, como una herramienta esencial para ofrecer más opciones a las pacientes.
Esta proteína pertenece a la familia de las PI3K (fosfoinositol 3-cinasas), cinasas lipídicas que promueven diversos procesos biológicos, incluyendo la división celular y la supervivencia, algunos de los cuales están directamente relacionados con la resistencia a las terapias endocrinas.
«Las mutaciones en PKI3CA son esenciales en el abordaje del cáncer de mama en estadio avanzado, ya que se ha observado que las afectadas tienen peor pronóstico, tanto por la alteración en sí misma –que origina recaídas tumorales más tempranas-, así como por el hecho de que mutación podría ser un mecanismo de resistencia terapéutica. Precisamente es en este ámbito donde existe indicación para los inhibidores de PIK3CA»,
, PIK3CA es una de las mutaciones más frecuentes en cáncer de mama, pues aparece en entre el 40-45% de las lesiones, según las series, con una distribución fundamental en los tumores luminales, los conocidos como hormono-dependientes, aunque también aparece en otros subtipos tumorales. Se sabe, además, que es una mutación que suele asociarse a un curso más agresivo de la enfermedad, por lo que su determinación «abre la oportunidad de emplear inhibidores selectivos, en este caso de unas subunidades de 3cinasa, como es el alpelisib, que han demostrado ser muy activas en cáncer de mama con esta mutación».
En este sentido, el oncólogo del INCLIVA alude a los datos del estudio Solar 1 en el que se evaluó la administración de un segundo fármaco de terapia endocrina, el fulvestrant, junto con un inhibidor de PIK3CA, el alpelisib, exclusivamente en pacientes con mutaciones en esta proteína.
«La combinación mostró un claro aumento de la supervivencia frente a la rama de pacientes a las que solo se administraba fulvestrant. De hecho, la FDA estadounidense y la EMA europea han aprobado alpelisib para pacientes PIK3CA mutadas con perfil luminal HER2 negativo», indica Pérez Fidalgo, quien detalla que «el actual esquema terapéutico para este subgrupo de cáncer de mama se basaría -una vez que ha progresado para una o dos líneas de terapia endocrina de primera línea-, en la estrategia de combinación de Fulvestrant con Alpelisib».
Diagnóstico precoz y específico
Sin embargo, otro de los hechos más relevantes se centra en las cada vez mayores posibilidades de llevar a cabo un diagnóstico molecular en cánceres de mama metastásico, y más concretamente en aquellos que presentan mutaciones en PIK3CA. «En el terreno del diagnóstico supone un cambio de aproximación y de paradigma», sostiene Rojo.
Durante más de 100 años, indica el patólogo, «el diagnóstico se ha basado, y se sigue basando, en el análisis de las características morfológicas del tumor. Pero, actualmente, la detección debe completarse con la caracterización de algunas alteraciones en la célula tumoral que o bien aportan información pronóstica o abren la oportunidad de utilizar terapias dirigidas».
Afortunadamente, la determinación de la mutación en este gen se lleva a cabo de forma sistemática mediante herramientas de secuenciación masiva de genes. Desde hace unos años, y para la caracterización de las mutaciones en tumores sólidos, se emplean técnicas de alto rendimiento conocidas como secuenciación masiva o NGS.
«En el caso de PIK3CA, gen muy relevante en tumores sólidos y del que además conocemos que puede asociar la indicación de un tratamiento específico, se incluye en todos los paneles de secuenciación masiva. Además, en las pacientes metastásicas es muy habitual que se empleen paneles de NGS no sólo para la detección sino también para buscar oportunidades de tratamiento».
No obstante, y como la herramienta NGS es compleja y podría no ser accesible en hospitales medianos, existen otras opciones. Es posible estudiar específicamente las mutaciones en este gen con técnicas basadas en PCR, rápidas y relativamente sencillas, que a partir del ADN del tumor buscan en este gen las mutaciones que son relevantes. Esta opción abre, según Rojo, «la posibilidad de que cualquier paciente con cáncer de mama hormonodependiente en situación metastásica se beneficie de la búsqueda de mutaciones en PIK3CA».
Las técnicas actuales de análisis masivo de genes han variado la forma de detectar e incluso de tratar el cáncer.
Las técnicas actuales de análisis masivo de genes han variado la forma de detectar e incluso de tratar el cáncer.
Para los oncólogos médicos y, por supuesto, para las pacientes, conocer la existencia de esta mutación específica permite un hecho básico: «introducir una nueva estrategia de tratamiento basada en la medicina de precisión. Hoy por hoy, avanzamos hacia la selección de las pacientes en función de las dianas terapéuticas y proponerles una terapia dirigida», indica el oncólogo.
A su juicio, el cáncer de mama es el ejemplo básico y clásico de este tipo de terapia porque los receptores hormonales fueron el primer receptor de una terapia dirigida. Posteriormente apareció el HER2, que ha seguido el mismo camino con los tratamientos anti-HER2, y actualmente están apareciendo una nueva tercera generación de biomarcadores selectivos como la PIK3CA». Actualmente, ya se están detectando pacientes con dobles biomarcadores a través de los que se está realizando «terapia doble dirigida e incluso terapias triples dirigidas, en función de las mutaciones y los biomarcadores selectivos detectados”, indica
Rojo coincide en esta nueva ‘vuelta de tuerca’, señalando que PIK3CA es un primer escalón en el ámbito de los biomarcadores, además del HER2 y de los estrógenos, porque en cáncer de mama ya están identificadas otras dianas; alteraciones moleculares que son más o menos frecuentes y sobre las cuales también se está investigando con fármacos dirigidos.
«En los próximos años se van a consolidar otros biomarcadores, actualmente en investigación, y la exigencia diagnóstica va a ser todavía mayor, lo que enlaza con la necesidad de disponer de técnicas de alto rendimiento para caracterizar adecuadamente los tumores y las pacientes».
El avance de la biopsia líquida
Los profesionales remarcan además una nueva ventana de oportunidad con el desarrollo y aplicación de la biopsia líquida que ofrece la posibilidad de evaluar la presencia de esta mutación en sangre periférica. Según Rojo, los ensayos tanto sobre PCR como en NGS se pueden hacer sobre ADN tumoral circulante (CTDNA).
La biopsia líquida parece detectar mutaciones en PIK3CA, lo que abre la puerta a la monitorización de la enfermedad
«Es una de las variantes que conocemos de biopsia líquida y que, en aquellas pacientes en las que no dispongamos de una muestra disponible de tumor para biopsia tradicional, se puede estudiar tanto el gen como las mutaciones a partir de biopsia líquida, con un rendimiento que, clínicamente, ha demostrado ser útil para indicar el tratamiento y, con el beneficio añadido de ser un método no invasivo”.
Según Pérez Fidalgo, a veces, la mutación está presente en el tumor de inicio, pero en otras ocasiones, se trata de una mutación adquirida. «En el curso de la enfermedad, después de haber sido sometida a diferentes tratamientos, puede emerger una mutación. Una de las estrategias que se plantea en la clínica es si es necesario re-biopsiar, con las consecuencias que ello contrae para la paciente, o si se podría intentar determinar con CTDNA o análisis del ADN tumoral circulante en sangre periférica».
Señala que, precisamente, en el estudio Solar 1, se identificaron mutaciones en CTDNA en sangre periférica, por lo que la FDA estadounidense ha hecho una aprobación para alpelisib en pacientes con mutación PIK3CA tanto en tumor como en CTDNA».
Rojo adelanta otra utilidad de la biopsia líquida, actualmente en investigación, que es la monitorización de la enfermedad en presencia de PIK3CA para predecir, en cierta medida, la respuesta al tratamiento.
«En estas pacientes, se ha demostrado que esta cuantificación o monitorización en sangre se asocia con el beneficio al tratamiento y puede anticipar, por ejemplo, una progresión a la enfermedad. Actualmente, este hecho se encuadra en el contexto de la investigación, pero en los próximos años tendremos un cuerpo de evidencia como para hacer recomendaciones. Será una herramienta muy importante para el manejo de las pacientes con cáncer de mama».
Sin duda, todos los avances en diagnóstico de mutaciones que se están afianzando en PIK3CA se traducen clínicamente en mejoras significativas de la supervivencia de las mujeres con cáncer de mama, y muy especialmente, en las que presentan enfermedad avanzada.
«Hay un beneficio claro en la supervivencia y los datos del estudio Solar 1 son el mejor ejemplo. Con PIK3CA tenemos un ‘target’ tal y como ocurrió con HER2, que también se puede beneficiar de una terapia específica», señala Pérez Fidalgo, quien considera que una gran parte de los éxitos cosechados en Oncología en los últimos años están asociados a biomedicina de precisión con identificación de un biomarcador válido.
«En el caso del PIK3CA es válido pero, además, podría determinarse en biopsia líquida, lo que evitaría re-biopsiar a las pacientes. Se trata de un ‘target’ que se está explorando en muchos otros tumores y situaciones». 
El oncólogo explica que uno de los puntos futuros más esperanzadores es el de la investigación de inhibidores de PIK3CA en combinación con inhibidores del PARP para cáncer de ovario, aproximación que se está explorando en España. «Parece también que la combinación de inhibidores de PIK3CA con inmunoterapia puede tener un efecto positivo, ya que la vía PIK3CA/m-TOR es una especie de cruce y parece que interacciona con otras muchas vías de señal».
El papel del patólogo en el manejo de múltiples enfermedades, y más concretamente, en cáncer, es cada día más evidente e importante. El abordaje tumoral es cada vez más complejo y requiere una visión multidisciplinar con expertos en la diferentes áreas de conocimiento.
«Tenemos que movernos desde estructuras estancas o de gestión vertical a una más transversal que permite que todos los especialistas participen en la decisión empoderada del paciente. El patólogo tiene que ser parte activa de los comités multidisciplinares que adoptan decisiones; ya no es suficiente con que el patólogo emita un diagnóstico y no participe más», considera Federico Rojo, responsable de Anatomía Patológica de la Fundación Jiménez Díaz de Madrid.
A su juicio, hay dos tareas en la que esta especialidad, y dentro de un grupo multidisciplinar, debería jugar un papel fundamental.
Primero, en la interpretación de la mutaciones. «El patólogo debe aprender y formarse en biología molecular y debe ofrecer una adecuada interpretación de lo que encuentra en el ámbito genómico. Cuando trabajamos, sobre todo, con secuenciación masiva es relativamente frecuente observar hallazgos no esperados o no previamente descritos. Y el patólogo es uno de los expertos, junto con biólogos moleculares, entre otros, que debe ofrecer la interpretación clínica de ese hallazgo molecular, por ejemplo para una recomendación de tratamiento, para que el comité tenga toda la información para considerar en cada caso».
El segundo aspecto en el que, según Rojo, esta especialidad ha de tener un papel muy activo es el relacionado con la decisión, junto al equipo, de cuál es la fuente de información más apropiada en cada caso, refiriéndose a qué muestra o biopsia es la más acertada en cada caso.
«Si en una paciente tenemos el tumor primario y además una biopsia de su lesión metastásica, por ejemplo, el patólogo debe valorar cuál de las dos ofrece la información más adecuada. De la misma forma, debe plantear si una biopsia líquida es capaz de aportar, en un momento dado, una información complementaria o adicional a la muestra de tejido que está disponible».
Para acometer estos retos, considera que se debe transmitir a los patólogos que deben ser actores más activos en el comité multidisciplinar, así como que han de actualizar su forma de diagnosticar. «Ya hemos dicho que el diagnóstico morfológico lo llevamos haciendo muchos años, y es una parte esencial, pero hay que complementarlo con el estudio molecular de mutaciones. Echamos de menos que el itinerario formativo de los patólogos no esté adecuadamente actualizado y, posiblemente, necesitamos que el periodo de formación de nuestros residentes se amplíe y se actualice para adquirir estas competencias. Cuando acabas la formación como especialista encuentras otra realidad asistencial que exige algo más que el diagnóstico clásico».
Autores

Nos ofrece a los médicos una rápida y variada información de las innovaciones medicas Muchas gracias por esta ayuda
Oncología-Radioterápica – En ‘Nature Medicine’
Sonia Moreno. Madrid Lun, 11/04/2022 – 17:00
Federico Rojo, jefe del Servicio de Anatomía Patológica de la Fundación Jiménez Díaz de Madrid
Alejandro Pérez Fidalgo, del Servicio de Oncología y Hematología del Instituto de Investigación Sanitaria Clínico Valencia (INCLIVA), del Hospital Clínico Universitario de Valencia.
Federico Rojo, jefe del Servicio de Anatomía Patológica de la Fundación Jiménez Díaz de Madrid
Eva Ciruelos, oncóloga médica de la Unidad de Cáncer de Mama del Departamento de Oncología y coordinadora de ensayos clínicos de esta patología en el Hospital Universitario 12 de Octubre de Madrid