DOSTARLIMAB, EN CANCERES SÓLIDOS CON DMMR DE COLON Y ENDOMETRIO
La eficacia de la medicación DOSTARLIMAB,, se ha mostrado muy eficaz en canceres de colon y menos en los de endometrio.
Ambos tumores sólidos con dMMR parecen responder bien a este tipo de tratamiento.
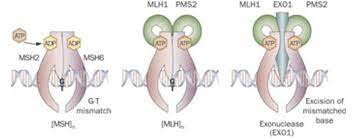
La dMMR es el sello distintivo del síndrome de Lynch (antes conocido como cáncer colorrectal hereditario sin poliposis), un trastorno de cáncer hereditario que aumenta el riesgo de cáncer colorrectal y de otros tipos de cáncer de por vida en los pacientes y tiene implicaciones para los parientes de estos.
Los descubrimientos del estudio también confirmaron la importancia de detectar dMMR en pacientes con cáncer rectal. Un cáncer hereditario que aumenta el riesgo de cáncer colorrectal y de otros tipos de cáncer de por vida en los pacientes y tiene implicaciones para los parientes de estos. El síndrome de Lynch es causado por defectos en los genes de reparación de desajustes, incluidos MLH1, MSH2, MSH6 y PMS2. La mayoría de los pacientes del estudio tenían el síndrome de Lynch, y la mayoría de los pacientes con ese síndrome además tenían mutaciones de línea germinal patogénicas en los genes MSH2 o MSH6. Los defectos en los genes MSH2 y MSH6 pueden predisponer a los pacientes al cáncer colorrectal, pero también se asocian con otros cánceres. Cerca de un quinto de los pacientes con cáncer rectal con dMMR del estudio tenían antecedentes de al menos un cáncer no colorrectal antes de su diagnóstico, y otro quinto desarrolló al menos un cáncer no colorrectal durante el período de seguimiento.
“Esos pacientes necesitan vigilancia de por vida de otros cánceres en otros órganos
Dada la gravedad de este síndrome, la aparición de una medicación eficaz es enormemente gratificante. Microsatellite Instability – Defective DNA Mismatch Repair
Luis A. Diaz, responsable del estudio, publicó los resultados en la revista New England Journal of Medicine, dijo que no conocía ningún otro estudio en el que un tratamiento lograra eliminar por completo un cáncer en todos los pacientes. “Creo que es la primera vez que esto sucede en la historia del cáncer”, dijo Díaz en “The New York Times”. Alan P. Venook, especialista en cáncer colorrectal de la Universidad de California en San Francisco, calificó el resultado de “inaudito”.
Por otra parte y de manera menos afortunada, el Dostarlimab para ha sido empleado en el CÁNCER DE ENDOMETRIO con deficiencia en la reparación de errores de emparejamiento recurrente o avanzado
Un ensayo clínico de fase 1 no aleatorizado
Ana Oaknin, MD, PhD1; Anna V. Tinker, MD2; Lucy Gilbert, MD3; et alVanessa Samouëlian, MD4; Cara Mathews, MD5; Jubileo Brown, MD6; María-Pilar Barretina-Ginesta, MD7,8; Víctor Moreno, MD9; Adriano Gravina, MD10; Cirilo Abdeddaim, MD11; Susana Banerjee, MD12; Wei Guo, PhD13; Hadi Danaee, ScD14; Ellie Im, MD15; Renaud Sabatier, MD16
Autor Afiliaciones Información del artículo
JAMA Oncol. 2020;6(11):1766-1772. doi:10.1001/jamaoncol.2020.4515
Hallazgos En este ensayo clínico de fase 1 no aleatorizado, la tasa de respuesta objetiva confirmada fue del 42 %; El 13 % de los pacientes tuvo una respuesta completa confirmada y el 30 % de los pacientes tuvo una respuesta parcial confirmada. La anemia (3 %), la colitis (2 %) y la diarrea (2 %) fueron los eventos adversos relacionados con el tratamiento de grado 3 o superior más comunes.
Lo que significa que Dostarlimab se asoció con una actividad antitumoral clínicamente significativa y duradera con un perfil de seguridad aceptable para pacientes con cánceres de endometrio con reparación deficiente de errores de emparejamiento que han progresado después de una quimioterapia previa basada en platino.
Los mecanismos de reparación de mutaciones de desajustes deficientes pueden sensibilizar a los cánceres de endometrio a las terapias contra la muerte programada 1 (PD-1). Dostarlimab (TSR-042) es un anticuerpo anti-PD-1 en investigación que se une con alta afinidad al receptor PD-1.
Diseño, entorno y participantes Este estudio multicéntrico, abierto, de un solo grupo y en curso comenzó la parte 1 el 7 de marzo de 2016 y comenzó a inscribir a pacientes con cáncer de endometrio con reparación de mutaciones deficientes el 8 de mayo de 2017. La mediana de seguimiento fue 11,2 meses (rango, 0,03 [en curso] a 22,11 [en curso] meses; según evaluaciones radiológicas). El análisis estadístico se realizó del 8 de julio al 9 de agosto de 2019.
Los pacientes recibieron 500 mg de dostarlimab por vía intravenosa cada 3 semanas durante 4 dosis, luego 1000 mg cada 6 semanas hasta la progresión de la enfermedad, la interrupción del tratamiento o el retiro.
Principales resultados y medidas El criterio principal de valoración fue la tasa de respuesta objetiva y la duración de la respuesta mediante una revisión central independiente ciega utilizando los Criterios de evaluación de respuesta en tumores sólidos, versión 1.1.
Resultados A partir del corte de datos, 104 mujeres (mediana de edad, 64,0 años [rango, 38-80 años]) con cánceres de endometrio con reparación de mutación deficiente de coincidencia fueron inscritas y tratadas con dostarlimab. De estos, 71 tenían enfermedad medible al inicio y a los 6 meses o más de seguimiento y se incluyeron en el análisis. Hubo una respuesta confirmada en 30 pacientes (tasa de respuesta objetiva, 42,3 %; IC del 95 %, 30,6 %-54,6 %); 9 pacientes (12,7 %) tuvieron una respuesta completa confirmada y 21 pacientes (29,6 %) tuvieron una respuesta parcial confirmada. Las respuestas fueron duraderas; no se alcanzó la mediana de duración de la respuesta (la mediana de seguimiento fue de 11,2 meses). La probabilidad estimada de mantener una respuesta fue del 96,4% a los 6 meses y del 76,8% a los 12 meses. La anemia (3 de 104 [2,9 %]), la colitis (2 de 104 [1,9 %]) y la diarrea (2 de 104 [1,9 %]) fueron los eventos adversos relacionados con el tratamiento de grado 3 o superior más comunes.
En este ensayo no aleatorizado, dostarlimab se asoció con una actividad antitumoral clínicamente significativa y duradera con un perfil de seguridad aceptable para pacientes con cánceres de endometrio con reparación de mutaciones deficientes después de quimioterapia previa basada en platino.
Aproximadamente 15000 pacientes en los Estados Unidos y 11000 pacientes en la Unión Europea son diagnosticadas anualmente con cáncer de endometrio (EC) avanzado o recurrente.1 La EC en etapa temprana puede tratarse con éxito mediante cirugía sola o cirugía con radioterapia o quimioterapia adyuvante ( generalmente quimioterapia doble basada en platino). El pronóstico para los pacientes con un diagnóstico de EC avanzada o recurrente es malo y, hasta donde sabemos, no existen pautas aceptadas basadas en consenso para el estándar de atención después de que la enfermedad progresa durante o después del tratamiento con un régimen que contiene platino. Los pacientes en este entorno generalmente reciben atención de rescate con quimioterapia de agente único o terapia hormonal, con actividad clínica limitada; las tasas de respuesta oscilan entre el 7 % y el 14 %, y la mediana de supervivencia general (SG) es inferior a 1 año.2-6
El cáncer de endometrio es un tipo de tumor asociado con altas tasas de inestabilidad de microsatélites-condición alta y reparación de desajustes de ADN-deficiencia (MSI-H/dMMR). Un informe de 2017 de Le et al7 evaluó 12019 muestras de tumores, que representan 32 tipos de tumores distintos para MSI-H/dMMR, e identificó EC como uno de los c
EL DOSTARLIMAB, ha logrado la remisión del cáncer de recto en un ensayo
Células de cáncer de colon@[luismmolina de Getty Images] via canva.com
El dostarlimab ha sido noticia recientemente después de que se publicasen los resultados de un ensayo clínico de fase II para su uso en el cáncer de colon. En dicha investigación, publicada en el medio The New England Journal of Medicine, el fármaco logró la remisión completa de los tumores en todos los participantes.
El objetivo: cáncer con reparación de desajuste deficiente
El medicamento en cuestión pertenece a una rama relativamente joven de las terapias contra el cáncer, pero que en los últimos años ha crecido enormemente: la inmunoterapia. Concretamente, el dostarlimab es un anticuerpo monoclonal anti-PD-1.
Para entender lo que esto significa, debemos repasar algunos de los mecanismos causantes del cáncer.
Normalmente, y tal como indica la Sociedad Americana del Cáncer, es normal que por el envejecimiento o por otros motivos (como el contacto con determinadas sustancias) las células sufran daño en el ADN. Nuestro organismo cuenta con varios sistemas para acabar con estas células y evitar que, al reproducirse, el daño se propague; por desgracia, estos métodos a veces fallan, y las células dañadas comienzan a reproducirse sin control.
Un fármaco logra remitir por completo el cáncer en todos los pacientes de un estudio
Más en concreto, existe cierto tipo de cánceres (como muchos colorrectales, señala el estadounidense Instituto Nacional del Cáncer) en los que ciertos genes implicados en la corrección de fallos cuando la célula copia fragmentos de ADN (proceso necesario para ‘enviar’ la información de ese fragmento a los ribosomas, que después expresan el gen en forma de proteína) no funcionan correctamente. Esto se llama reparación de desajuste deficiente (dMMR, por sus siglas en inglés), y es el tipo de cáncer frente al que, al menos por ahora, el dostarlimab parece excepcionalmente eficaz.
El mecanismo de acción: inhibir los ‘puestos de control’
Como decíamos, las células cancerosas son uno de los elementos nocivos que nuestro sistema inmune debería detectar y eliminar. En condiciones normales, para hacer esto se sirve, entre otras cosas, de lo que se conoce como ‘puestos de control’: una serie de proteínas presentes en las células inmunes (a esta clase pertenece la proteína PD-1) que, al entrar en contacto con una proteína complementaria (en el caso de la PD-1, la proteína PD-L1) presente en otras células del cuerpo, funcionan como ‘interruptores’ que evitan una respuesta inmune.
Thank you for watching
Con todo, algunos tumores (que, no olvidemos, provienen de células del propio organismo que han sido dañadas) aún expresan la proteína PD-L1 (incluso, en cantidades mayores a lo normal, lo que efectivamente los protege de la acción del sistema inmune).
Un nuevo tratamiento contra el cáncer de pulmón multiplica por seis la erradicación de los tumores
En este principio se basan ciertas inmunoterapias contra el cáncer, según desarrolla la Sociedad Americana del Cáncer, que buscan interferir en este sistema para ‘guiar’ al sistema inmune a atacar esas células que no reconoce como enemigas. Para lograr tal cosa, se emplean anticuerpos (una molécula que se une a otra de una sustancia extraña, llamada antígeno) monoclonales (siempre idénticos, ya que son producidos por un único tipo de célula inmune) producidos artificialmente para que se unan a una de las dos proteínas (la PD-1 o la PD-L1) de forma que el propio sistema inmune la reconozca como antígeno y la ataque, inhibiendo la función de los puestos de control.
Por este complejo método, se elimina la cobertura de las células tumorales frente al sistema inmune, que ahora sí que las ataca y acaba con ellas.
Muchos tumores sólidos con dMMR parecen responder bien a este tipo de tratamiento.
El resultado: muy prometedor, pero aún no definitivo
Recapitulando, el dostarlimab es uno de los medicamentos empleados en este tipo de inmunoterapia, indicado hasta ahora en tumores de endometrio con dMMR. La novedad del ensayo clínico citado es que se estaba probando la eficacia y seguridad de su uso en pacientes con adenocarcinoma de colon con dMMR de estadios II y III, ya que este tipo de tumores parece ser sensible a la inmunoterapia
anti-PD-1.
Los resultados han sido tremendamente positivos. Tanto que han sorprendido a los propios autores del trabajo: originalmente, pensaban administrar quimioterapia a aquellos pacientes que no lograsen la remisión completa tras la administración de dostarlimab, a fin de estudiar la eficacia de la terapia coadyuvante, pero esto no ha hecho falta debido a que la remisión se ha dado en el 100% de los 12 pacientes.
La noticia es por ello muy esperanzadora.
Autores del trabajo
Luis A. Diaz, New England Journal of Medicine
Ana Oaknin, MD, PhD1; Anna V. Tinker, MD2; Lucy Gilbert, MD3; et alVanessa Samouëlian, MD4; Cara Mathews, MD5; Jubileo Brown, MD6; María-Pilar Barretina-Ginesta, MD7,8; Víctor Moreno, MD9; Adriano Gravina, MD10; Cirilo Abdeddaim, MD11; Susana Banerjee, MD12; Wei Guo, PhD13; Hadi Danaee, ScD14; Ellie Im, MD15; Renaud Sabatier, MD16
Autor Afiliaciones Información del artículo
JAMA Oncol. 2020;6(11):1766-1772. doi:10.1001/jamaoncol.2020.4515
D