 La angiogénesis consiste en la formación de vasos sanguíneos a partir de otros preexistentes.
La angiogénesis consiste en la formación de vasos sanguíneos a partir de otros preexistentes.
Es un proceso fundamental en la aparición de múltiples procesos y necesario para la inflamación y sobre todos para la producción demetástasis.
Es imprescindible el conocimiento de este desarrollo patológico de los vasos para entender la inflamación.
Cualquier tejido inflamado crea nueva circulación, de forma que es imprescindible para reconocer la fisiopatología de la inflamación y para tenerla en cuenta a la hora de inhibir su evolución.
Es un proceso fundamental durante el desarrollo del embrión mientas que en los adultos, normalmente, sólo se produce en procesos como cicatrización de heridas. El gran interés que la angiogénesis ha despertado entre la comunidad científica en los últimos años se debe a la constatación de que la angiogénesis está anormalmente activada en un gran número de enfermedades, desde cáncer a dolencias inflamatorias crónicas como artritis reumatoide o psoriasis. El estudio de las bases moleculares de la angiogénesis durante la inflamación, como medio para avanzar en el conocimiento de dichas enfermedades e identificar posibles moduladores que atenúen sus procesos inflamatorios
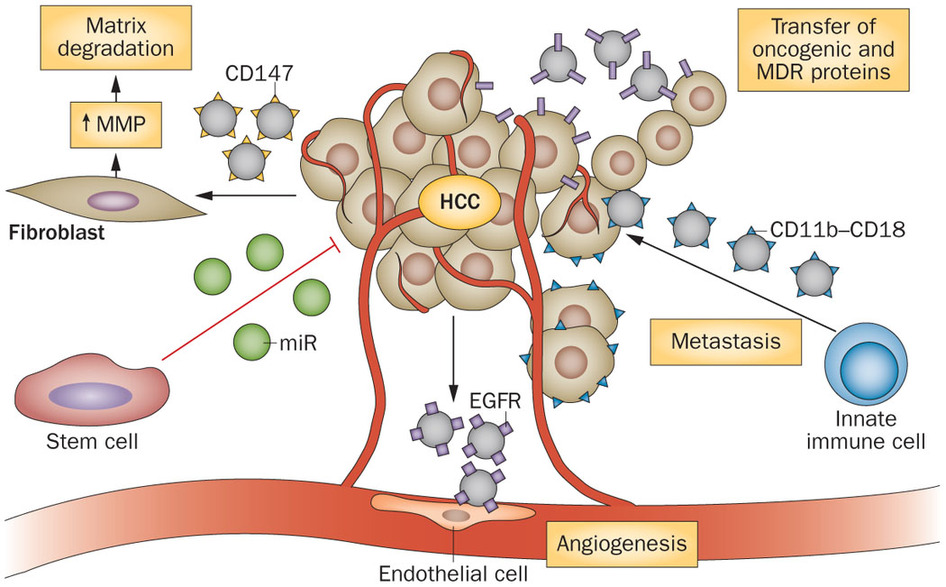
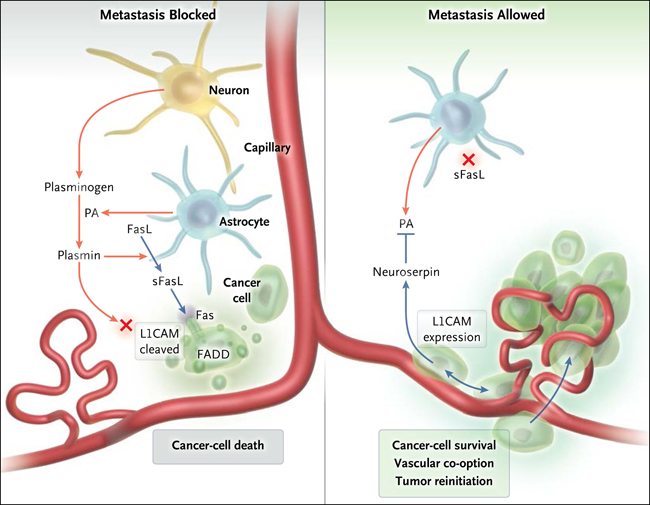
La angiogénesis (angios: vasos; génesis: formación) es la formación de nuevos vasos sanguíneos a partir de otros preexistentes. En el organismo, este proceso está controlado mediante la producción de sustancias que promueven el crecimiento vascular (factores pro-angiogénicos) y sustancias que lo inhiben (factores anti-angiogénicos), que se mantienen en equilibrio en condiciones fisiológicas normales. Cuando este equilibrio se altera debido a un aumento de factores pro-angiogénicos, se produce un crecimiento anormal de los vasos sanguíneos, lo que puede llevar a producir una hipervascularización en ciertos tejidos. La angiogénesis aparece en un elevado número de patologías, más de 70 descritas hasta la fecha. Entre ellas se encuentran el cáncer, la degeneración macular asociada a la edad, y enfermedades inflamatorias autoinmunes como la psoriasis o la artritis reumatoide.
En los primeros pasos del proceso de formación de vasos sanguíneos o angiogénesis, las células que forman el vaso sanguíneo (células endoteliales) responden ante la presencia de factores pro-angiogénicos cambiando su morfología y función. Estas células aparecen muy polarizadas (es decir, elongadas, con un polo hacia el exterior del vaso) y con numerosos filopodios (pequeños tentáculos), y se conocen como células líder o ‘tip’ (Figura 1). Las células endoteliales ‘tip’ se encargan de la invasión del tejido circundante, abriendo paso para permitir la formación del nuevo vaso. Para degradar, entre otras muchas cosas, las proteínas que forman este tejido circundante, estas células ‘tip’ expresan proteasas (proteínas que degradan otras proteínas). Entre ellas, el grupo de investigación al que pertenezco, se centra en un tipo específico, las metaloproteinasas de matriz, y en concreto MT1-MMP (Membrane Type 1- Matrix MetalloProteinase). Trabajos previos de mi laboratorio demostraron que la presencia de MT1-MMP es esencial en la formación de capilares inducida por ciertos factores inflamatorios, por lo que podría ser relevante en contextos inflamatorios específicos.
Con estos antecedentes y dado el desconocimiento acerca de los mecanismos moleculares que regulan la formación de nuevos capilares durante el proceso inflamatorio, nos propusimos ahondar en este tema estudiando las bases moleculares de la angiogénesis ante distintos estímulos inflamatorios (factores que desencadenan la inflamación: TNFα, MCP-1, SDF-1 y MIP-2) en comparación con el estímulo angiogénico clásico VEGF (Vascular Endothelial Growth Factor).
Para ello, extrajimos células de los vasos sanguíneos pulmonares de ratones (MLEC, Mouse Lung Endothelial Cell) y las hicimos crecer. Para conseguir un mayor número de células y poder realizar todos los ensayos en paralelo, las incubamos con un virus (en concreto el antígeno-T de polioma virus) haciéndolas inmortales, aumentando su proliferación y crecimiento celular.
Estas células se pusieron en contacto con los factores que desencadenan la inflamación, a distintos tiempos. De esta manera pudimos ver qué tipo de cambios se producían en las células endoteliales inmortales, es decir, si producían marcadores, o lo que es lo mismo, proteínas específicas (VEGFR2, Jag1, Dll4, MT1-MMP, integrina αVβ3 y CXCR4) que indicasen que se habían convertido en células ‘tip’.
Mediante el uso de técnicas utilizadas en biología molecular (citometría de flujo) analizamos la expresión de estos marcadores en la membrana de las célulasy observamos su localización dentro de la célula (mediante imágenes de inmunofluorescencia en microscopía confocal en dos y tres dimensiones, Figura 2).
Estos ensayos nos permitieron identificar distintos mecanismos moleculares que hacen que las células endoteliales se conviertan en células ‘tip’, dependiendo del factor inflamatorio empleado. Para analizar la implicación de MT1-MMP en estos procesos, se realizaron los mismos ensayos en células endoteliales procedentes de ratones transgénicos que no eran capaces de producir esta proteasa (MT1-MMP), lo que se conoce como ensayos de pérdida de función. Tras estos modelos celulares, nuestro laboratorio profundizará en estos estudios mediante el análisis de modelos ex vivo (explantes de retina) e in vivo (inyección intraocular) en ratón.
En este proyecto podemos ver cómo evolucionan las investigaciones biomédicas, en las que el uso de modelos celulares y animales son pasos previos necesarios para entender qué ocurre a nivel humano. Este es un ejemplo más de lo que hoy en día se conoce como From the bench to the bedside, es decir, la necesidad de una investigación básica que nos permita avanzar en el conocimiento de la patogenia de enfermedades, trasladándola “del laboratorio a la clínica; de la investigación a la salud”. La descripción de mecanismos característicos de estímulos inflamatorios específicos podría ser relevante en el desarrollo de nuevas técnicas diagnósticas como la identificación de biomarcadores (indicadores de un proceso biológico normal, estado patogénico o de respuesta a un tratamiento farmacológico) así como de dianas terapéuticas (hacia lo que dirigir el fármaco para atajar el problema) específicas en enfermedades inflamatorias que cursan con hipervascularización, lo que redundará positivamente en el Sistema Nacional de Salud.
Alba Mota, Premio Arquímedes 2011.
Enhorabuena por la insistencia en el tema: es muy conveniente
para llegar al triunfo.
Sin embargo, hace medio siglo se dejó de hablar, en mis medios,
de patología
del sistema vago y simpático
por un posible abuso clínico
sin un soporte de pruebas diagnósticas suficientes.
¿Habría algo mas que la frecuencia cardiaca, aunque sea
anotada no por el pulso o la auscultacion, sino
por el ECG?