De todos es conocida la evolución de la inmunidad para mantener la homeostasis de los seres vivientes. Seguro que el sistema inmunitario del homo sapiens de nuestros días es diferente al del hombre de Neandertal. Y también seguro que los agentes patógenos infecciosos y no infecciosos intervinieron en la modulación de la inmunidad.
Esto explica muy bien Andersson y Tracey en su artículo Neural Reflexes in inflamtion and immunity.
La inmunidad es el mecanismo por el cual el sistema nervioso controla las funciones globales del organismo. En un principio este control del sistema nervioso se relegaba exclusivamente al sistema cardiovascular, músculo esquelético y gastrointestinal, recientemente se ha conocido que también controla el sistema inmunológico para mantener la homeostasis. De forma que este reflejo ha evolucionado desde los antiguos gusanos hasta nuestro homo sapiens y fue este mecanismo de regulación de los mamíferos el que contribuyo de una manera sorprendente controlar la inflamación y ahora creemos saber que el equilibrio del sistema vegetativo controla la desmedida y persistente inflamación, posiblemente causante de la mayoría de enfermedades crónicas de nuestros tiempos.
El conocimiento de la acción de los corticoides en el control de la inflamación fue una llamada al orden sobre la necesidad que tenemos los mamíferos de controlar la inflamación más allá del exterminio del agente causal.
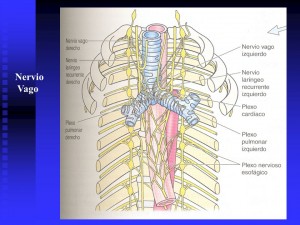
El mejor conocimiento de la anatomía del sistema vegetativo y los estudios sobre la estimulación del vago han hecho ver que este inerva prácticamente toda nuestra biología incluido el bazo, el timo, los ganglios linfáticos y a menudo la bolsa de Fabricio. Los estudios, con microscopio electrónico han mostrado la terminación de las fibras nerviosas en los linfocitos B y T y en los macrófagos.
Las neuronas que inervan las estructuras inmunológicas se localizan en el tronco del encéfalo, y su estímulo conduce a la producción por el simpático y el parasimpático de neurotransmisores adrenérgicos y colinérgicos entre otros. Tracey afirma que el reflejo neural es imprescindible para entender la inmunidad y que las señales emitidas por el N. vago modulan la respuesta inmune.
La respuesta inflamatoria no resuelta conduce a la inflamación crónica. De ello se deduce la necesidad de una homeostasis inmunitaria. El mantenimiento crónico de la inflamación conduce a la sepsis, arteriosclerosis, obesidad, cáncer, enfermedades pulmonares, inflamación en la vejiga, enfermedades neurodegenerativas, esclerosis múltiples y artritis reumatoide (Nathan and Ding 2010).
La respuesta humoral, celular y neural evitan la no resolución de la inflamación (Nathan and Ding 2010).
Las deficiencias en los glucocorticoides o hormonas pituitarias que normalmente regulan su producción confieren sensibilidad a la inflamación y la infección (Besedovsky y del Rey, 2.000; Sternberg, 2.006). Los niveles de glucocorticoides aumentan precozmente desde el principio en la inflamación, proporcionando señales de retroalimentación importantes para suprimir la respuesta inmune y proteger al huésped de la lesión y la toxicidad causada por la inflamación excesiva. El factor de necrosis tumoral TGF-β interviene de forma manifiesta en la inflamación y su exceso de reponsable del dolor y esta se segregado por los macrófagos punto estuvo abierto un nuevo campo en el conocimiento y manejo de la inflamación por medios solubles de retroalimentación negativos producidos por el sistema inmune. (Tsunawaki et al., 1988). La IL-10 fue más tarde implicada como mediador humoral en la inflamación y está producida por monocitos (Mosser y Zhang, 2008).
El sistema nervioso, que recibe información desde el sistema inmunológico en forma de mediadores solubles y por las neuronas sensoriales, también suprime la inflamación(Watkins et al, 1995b.; Tracey, 2007).
El sistema nervioso autónomo regula principalmente la homeostasis de órganos a través de los reflejos que se componen de las neuronas aferentes y eferentes.
En el reflejo inflamatorio se desencadena en forma de señales eferentes que viajan desde el núcleo ambiguo y el núcleo motor dorsal por el nervio vago, y terminan en el ganglio celiaco (Berthoud y Powley, 1996; Borovikova et al, 2000b.). La estimulación del nervio vago activa las neuronas esplénica adrenérgicas que residen en el ganglio celiaco, que a su vez viajan al bazo y terminan en sinapsis con las células T (Rosas-Ballina et al., 2011). La norepinefrina liberada por las neuronas esplénicas se une a los receptores adrenérgicos ß2 expresado en un subconjunto de células T que expresa la colina acetiltransferasa, la enzima limitante de la velocidad en la síntesis de acetilcolina.
En pacientes con enfermedad autoinmunes, la inflamación, no controlada estimula de manera desproporcionada la señalización del nervio vago, lo que acelera la progresión de la inflamación y evita su resolución (Tracey, 2007). La medición de los niveles basales de la actividad del nervio vago en la enfermedad humana se ha convertido en un análisis de gran interés potencial. Por analogía con la influencia inhibitoria tónica de la actividad del nervio vago en el ritmo cardíaco, la actividad del nervio vago deprimida causa un aumento de la frecuencia cardíaca. Variabilidad de la frecuencia cardiaca (VFC), un método utilizado para cuantificar la fuerza de la señalización del nervio vago, se ha estandarizado y aplicado en numerosos estudios(Sloan et al., 2007a). Estos resultados clínicos revelan una correlación entre la actividad deprimida del nervio vago y el aumento de la morbilidad y la mortalidad en las enfermedades inflamatorias, no resuelta. Por ejemplo, la tasa de mortalidad en la sepsis grave fue de 60% en aquellos pacientes con actividad del nervio vago deprimida a su de ingreso en el hospital, en comparación con la mortalidad del 0% en los sujetos con una mayor actividad del nervio vago (Pontet et al., 2003). En pacientes con vagotomía por trauma, habían aumentado significativamente la mortalidad y la septicemia en comparación con una cohorte de pacientes de control emparejados por edad, sexo, comorbilidades, esplenectomía concurrente y otros factores (Peterson et al., 2012).
Numerosos estudios de la VFC en la artritis reumatoide reveló reducción significativa en la actividad del nervio vago en los pacientes en comparación con los controles (Evrengül et al., 2004; Goldstein et al., 2007).
Parece objetivo que la ciencia moderna está demostrando como los circuitos neurales modulan la inmunidad, pero que nadie se engañe necesitamos múltiples estudios para dar una realidad a destrucción.
Reflejos neuronales en la inflamación y la inmunidad 1
1. Ulf Andersson 1 y Kevin J. Tracey 2