La inflamación puede afectar a todos los aspectos del desarrollo y progresión tumoral, así como la respuesta a la terapia. En los últimos 10 años, hemos aprendido mucho acerca de los diferentes mecanismos por los que el cáncer y la inflamación se cruzan, y es el momento adecuado para traducir gran parte de los conocimientos básicos adquirida hasta la fecha y lo utilizan para agregar nuevos armamentos al arsenal de cáncer terapéutica. Sólo mediante la focalización todos los aspectos de la biología del cáncer, podemos esperar para obtener ganancias reales en la lucha contra estas enfermedades actualmente incurables. Además de una combinación de enfoques anti-inflamatorias que se dirigen al microentorno del tumor con fármacos tumoricidas más sofisticadas y selectivas, las futuras terapias también deben tomar nota de la variación genética natural que afecta a la inflamación y la inmunidad. Tales consideraciones son extremadamente importantes en el diseño de nuevos enfoques preventivos a la reducción del riesgo de cáncer que necesita ser aplicada a grandes poblaciones compuestas por personas relativamente sanas. De hecho, una de las principales lecciones aprendidas de la investigación de las relaciones entre la inflamación y el cáncer, es que la mayoría de los cánceres se pueden prevenir.
La presencia de leucocitos dentro de los tumores, fue observada en el sigro XIX por Rudolf Virchow, la inflamación en la tumorigénesis es ahora generalmente aceptada, y se ha hecho evidente que un microambiente inflamatorio es un componente esencial de todos los tumores, incluyendo algunas en las que una relación causal directa con la inflamación todavía no se ha demostrado ( Mantovani et al., 2008 ) . Sólo una minoría de todos los cánceres son causados por mutaciones de la línea germinal, mientras que la gran mayoría (90%) están vinculados a mutaciones somáticas y factores ambientales. Muchas causas ambientales del cáncer y factores de riesgo están asociados con algún tipo de inflamación crónica. Hasta 20% de los cánceres están relacionados con infecciones crónicas, el 30% se puede atribuir al consumo de tabaco e inhalados contaminantes (tales como sílice y amianto), y 35% a los factores de la dieta (20% de carga del cáncer está vinculada a la obesidad) ( Aggarwal et al., 2009 ).
Ahora esta bien establecido que la inducción de la inflamación por infecciones bacterianas y virales aumenta el riesgo de cáncer ( de Martel y Franceschi, 2009 ), trabajos recientes han demostrado que además de ser un iniciador de tumor en virtud de su alto contenido de carcinógeno, tabaco humo es también un promotor de tumores debido a su capacidad de desencadenar la inflamación crónica ( Takahashi et al., 2010 ). Del mismo modo, la obesidad, cuya prevalencia está creciendo a un ritmo alarmante, promueve la tumorigénesis en el hígado ( Park et al., 2010 ) y el páncreas ( Khasawneh et al., 2009 ). La mayoría de los tumores malignos sólidos aparecen en las personas mayores e incluso la vejez ( Ershler y Keller, 2000 ) y la senescencia celular ( Rodier et al., 2009 ) se postulan para ser promotores tumorales que actúan a través de mecanismos inflamatorios. Además de sus efectos pro-tumorigénicos, inflamación también influye en la respuesta inmunitaria del huésped a los tumores y se puede usar en la inmunoterapia del cáncer ( Dougan y Dranoff, 2009 ) y para aumentar la respuesta a la quimioterapia ( Zitvogel et al., 2008 ). Sin embargo, en algunos casos, la inflamación puede disminuir los efectos beneficiosos de la terapia ( Ammirante et al., 2010 ). Esta opinión se centra principalmente en los efectos pro-tumorigénicas de la inflamación, pero también se refiere a la relación entre la inflamación y la inmunidad anti-tumor,
Ir:
Varios tipos de inflamación-difieren en causa, mecanismo, los resultados y de intensidad puede promover el desarrollo y progresión del cáncer
1 ). Persistent Helicobacter pylori infección se asocia con el cáncer gástrico y MALT (tejido linfoide asociado a la mucosa) linfoma. Las infecciones con hepatitis B (VHB) o C (VHC) aumentan el riesgo de carcinoma hepatocelular (HCC) y las infecciones con Schistosoma o Bacteroides especies están vinculados a la vejiga y el cáncer de colon, respectivamente ( Karin, 2006 ; Wu et al., 2009a ) . La respuesta inflamatoria desencadenada por la infección precede al desarrollo tumoral y es una parte de la defensa del huésped normal, cuyo objetivo es la eliminación de patógenos. Sin embargo, los patógenos tumorigénicas subvierten la inmunidad del huésped y establecer infecciones persistentes asociados con el bajo grado, pero la inflamación crónica. Por el contrario, la inflamación aguda inducida por ciertas preparaciones microbianas fue utilizado por Coley con cierto éxito para tratar el cáncer en la década de 1890 y uno de tales preparación se usa actualmente en el tratamiento de cáncer de vejiga ( Rakoff-Nahoum y Medzhitov, 2009 ). Lo que hace que el carcinoma de vejiga especialmente sensibles a la inflamación aguda, a pesar de que es promovido por la inflamación crónica, es actualmente desconocido. Este es un importante problema cuya solución debe revelar cómo implementar con éxito la inflamación en la terapia del cáncer. Otro tipo de inflamación crónica que precede al desarrollo tumoral es causada por la desregulación inmune y autoinmunidad. Un ejemplo es la enfermedad inflamatoria del intestino, lo que aumenta en gran medida el riesgo de cáncer colorrectal ( Waldner y Neurath, 2009 ).
Tipos de inflamación en la tumorigénesis y el cáncer.
Sin embargo, no todas las enfermedades inflamatorias crónicas aumentan el riesgo de cáncer y algunos de ellos, tales como psoriasis, pueden incluso reducirlo ( Nickoloff et al., 2005 ). No está claro qué hace que IBD o tumor hepatitis crónica promover, en comparación con las condiciones tales como la artritis reumatoide o la psoriasis, que no promueven significativamente la tumorigénesis. Una posibilidad podría estar relacionada con la exposición del tracto gastrointestinal y el hígado a carcinógenos dietéticos y ambientales, que nunca se abren paso en las articulaciones o la piel. La inflamación crónica también puede ser inducida por la exposición ambiental. El material en partículas del humo del tabaco y otros irritantes puede precipitar la enfermedad pulmonar obstructiva crónica, una afección asociada con mayor riesgo de cáncer de pulmón ( Punturieri et al., 2009 ). Mecanismos inflamatorios representan el tumor promover el efecto de la exposición al humo del tabaco en el cáncer de pulmón en ratones ( Takahashi et al., 2010 ). Partículas de amianto o de sílice inhalados también dar lugar a cáncer de pulmón, pero no tienen actividad mutagénica obvio. Dichas partículas, sin embargo, pueden desencadenar la inflamación a través de efectos sobre la pro-interluekin-1β (IL-1β) procesamiento por el inflamasoma ( Dostert et al., 2008 ) y esto puede mediar su actividad tumorigénica. Incluso la obesidad, lo que aumenta el riesgo de cáncer en 1,6 veces ( Calle, 2007 ), puede conducir a la inflamación crónica ( Tuncman et al., 2006 ) que promueve el desarrollo del carcinoma hepatocelular ( Park et al., 2010 ). La acumulación de ADN dañado y la senescencia celular también puede dar lugar a tumor promoción de la inflamación crónica ( Rodier et al., 2009 ; Zheng et al., 2007 ).
Un tipo completamente diferente de la inflamación es la que sigue el desarrollo del tumor. La mayoría, si no todos, los tumores malignos sólidos desencadenar una respuesta inflamatoria intrínseca que se acumula un microambiente pro-tumorigénico ( Mantovani et al., 2008 ). Además de la proliferación de células autónoma, ciertos oncogenes, tales como RAS y MYC miembros de la familia, inducen un programa transcripcional que conduce a la remodelación del microambiente del tumor a través del reclutamiento de leucocitos y linfocitos, la expresión de las quimioquinas y citoquinas promotores de tumores, y la inducción de un interruptor angiogénico ( Soucek et al., 2007 ; Sparmann y Bar-Sagi, 2004 ). Todos los tumores malignos sólidos, en algún momento superan su suministro de sangre y se convierten en oxígeno y nutrientes privado. Esto resulta en la muerte celular necrótica en el núcleo del tumor y la liberación de mediadores pro-inflamatorios, tales como IL-1 y HMGB1 ( Vakkila y Lotze, 2004 ). La respuesta inflamatoria subsiguiente promueve la neo-angiogénesis y proporciona células de cáncer que sobreviven con factores de crecimiento adicionales, producidos por las células inflamatorias e inmunes recientemente reclutados ( Karin, 2006 ).
Otros tumores, para el cáncer de pulmón ejemplo, pueden promover la inflamación a través de la secreción activa de moléculas, tales como el extracelular componente versicano matriz que activa los macrófagos a través del receptor Toll-like (TLR) 2 ( Kim et al., 2009 ). Basado en la renovación celular continua y la proliferación inducida por la inflamación asociada al tumor, los tumores se han referido como “heridas, que nunca curan” ( Dvorak, 1986 ). Este tipo de inflamación es en gran medida una cicatrización de heridas subvertido y respuesta regenerativa de tejido. Oncogenes Incluso dominantes tales como v-Src o K-Ras son incapaces de inducir el cáncer en animales adultos sin ir acompañado de lesión y regeneración de tejidos posterior ( Guerra et al., 2007 ; . Sieweke et al, 1990 ).
Por último, una respuesta inflamatoria asociada a tumor fuerte puede ser iniciado por la terapia del cáncer. La radiación y la quimioterapia causan la muerte necrótica masiva de las células cancerosas y los tejidos circundantes, que a su vez desencadenan una reacción inflamatoria análoga a una respuesta de cicatrización de heridas ( Zong y Thompson, 2006 ). El resultado neto de la inflamación inducida por el tratamiento es controvertido, ya que por un lado puede tener funciones promotores de tumores al igual que la necrosis que acompaña el crecimiento rápido del tumor ( Ammirante et al., 2010 ; Vakkila y Lotze, 2004 ), pero por otro mano que puede mejorar la presentación cruzada de antígenos tumorales y la posterior inducción de una respuesta inmune anti-tumor ( Zitvogel et al., 2008 ). Este último y su importancia se tratará más adelante.
Ir:
Las células inmunes en la tumorigénesis
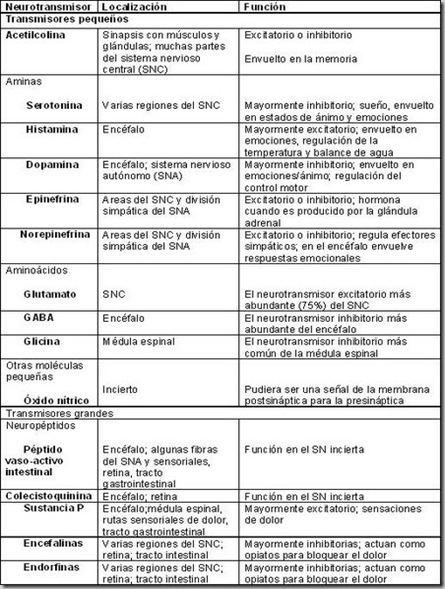
Como resultado de estas diferentes formas de inflamación, el microambiente tumoral contiene células inmunitarias innatas (incluyendo macrófagos, neutrófilos, mastocitos, células supresoras mieloides derivados, células dendríticas, y células asesinas naturales) y células inmunes adaptativas (linfocitos T y B) en Además de las células cancerosas y su estroma circundante (que consiste en fibroblastos, células endoteliales, pericitos y células mesenquimales) ( de Visser et al., 2006 ) ( Tabla 1 ). Estas células diversas comunican entre sí por medio de contacto directo o producción de citoquinas y de quimioquinas y actúan de maneras autocrinos y paracrinos para controlar y dar forma a crecimiento del tumor. Es la expresión de diversos mediadores inmunes y moduladores, así como la abundancia y estado de activación de los diferentes tipos de células en el microambiente tumoral que dictan en qué dirección se inclina el equilibrio y si la inflamación-promueve el crecimiento tumoral o la inmunidad anti-tumor se producirán ( Lin y Karin, 2007 ; . Smyth et al, 2006 ). En tumores establecidos este equilibrio está profundamente inclinado hacia la inflamación pro-tumoral, ya que sin la intervención terapéutica tumores avanzados rara vez regresan. Sin embargo, es difícil de evaluar de manera inequívoca el impacto global de la inmunidad y la inflamación en los primeros eventos tumorigénicas, porque directa en modelos in vivo para la evaluación de los efectos de estos fenómenos en el crecimiento inicial del tumor están desaparecidos. Además, nuestro conocimiento actual se basa en la medición de la carga tumoral en un punto donde las células malignas pueden ya han escapado mecanismos de vigilancia temprana. Sin embargo, es seguro suponer que tumor promoción de la inflamación y la inmunidad anti-tumor co-existen en diferentes puntos a lo largo de la ruta de progresión del tumor ( Figura 2 ) y que las condiciones ambientales y microambientales dictan el equilibrio entre los dos ( Bui y Schreiber, 2007 ; Swann et al., 2008 ).
El papel multifacético de la inflamación en el cáncer
Funciones de los diferentes subtipos de células inmunes e inflamatorias en la inmunidad anti-tumor y la inflamación promotor de tumores
Las células inmunes que se encuentran más frecuentemente en el microambiente del tumor son los macrófagos asociados a tumores (TAMs) y las células T. TAM principalmente promover el crecimiento del tumor y puede ser obligatorio para la angiogénesis, la invasión y la metástasis ( Condeelis y Pollard, 2006 ), y alto contenido de TAM en general se correlaciona con mal pronóstico ( Murdoch et al., 2008 ). Células T maduras se dividen en dos grupos principales en base a los receptores de células T (TCR) que expresan: γδ y αβ. células αβT se clasifican además según sus funciones efectoras como CD8 + células T citotóxicas (CTL) y CD4 + células T helper (Th), que incluyen Th1, Th2, Th17 y las células T reguladoras (Treg), así como natural killer T células (NKT). Es importante destacar que, las células T pueden ejercer tanto supresor del tumor y efectos promotores, como se determina por sus funciones efectoras ( DeNardo et al., 2009 ; . Langowski et al, 2007 ; . Smyth et al, 2006 ). El aumento del número de células T, CTL activados específicamente y las células Th, se correlacionan con una mejor supervivencia en algunos tipos de cáncer, incluyendo el cáncer invasivo de colon, melanoma, mieloma múltiple, y cáncer de páncreas ( Galon et al., 2006 ; Laghi et al., 2009 ; Swann y Smyth, 2007 ). Correspondientemente, la deficiencia de células T o la interrupción de mecanismos citotóxicos específicos pueden hacer que los animales de experimentación más susceptibles a la carcinogénesis espontánea o químicos ( Shankaran et al., 2001 ; Swann y Smyth, 2007 ). Sin embargo, también hay pruebas de que muchos de los subconjuntos de células T que se encuentran en los tumores sólidos están involucrados en la promoción del tumor, la progresión, o metástasis, incluyendo CD8 +células T ( Roberts et al., 2007 ), IFN-producción de células Th1 ( Hanada et al., 2006 ), las células Th2 ( Aspord et al., 2007 ; . DeNardo et al, 2009 ) y las células Th17 ( Langowski et al., 2006 ; . Wang et al, 2009 ). Las únicas células que carecen de un papel pro-tumorigénicos, hasta el momento, son las células NK. Similar a TAM, las funciones de promotores de tumores de linfocitos T están mediadas por citoquinas, mientras que ambas citocinas y mecanismos citotóxicos median las funciones anti-tumorigénicas de linfocitos T ( Lin y Karin, 2007 ; Swann y Smyth, 2007 ).
Curiosamente, las células Treg, que se presume que actúa sobre todo de una manera pro-tumorigénico través de la supresión de las respuestas inmunes anti-tumorales ( Gallimore y Simon, 2008 ), también pueden ejercer una función de anti-tumorigénico en determinadas circunstancias en virtud de su capacidad de suprimir la inflamación promotor de tumores ( Erdman et al., 2005 ). En el cáncer de mama, la presencia de linfocitos infiltrantes de tumor con alta CD4 + / CD8 + y la relación de Th2 / Th1 es indicativo de mal pronóstico ( Kohrt et al., 2005 ). Th2 CD4 + células T estimulan la progresión del cáncer de mama y metástasis mediante la educación de TAMs para producir factores pro-angiogénicos y pro-metastásico ( DeNardo et al., 2009 ). En el cáncer asociado colitis (CAC), las células T que infiltran también parecen desempeñar una función de promotor de tumores ( Waldner y Neurath, 2009 ). Lo que hace el mismo subconjunto de células T anti-tumorigénico en un cáncer y pro-tumorigénicos en otra permanece en gran parte desconocida y puede ser la clave para el desarrollo de la inmunoterapia con éxito.
El perfil de expresión de citoquinas y quimioquinas de la microambiente tumoral puede ser más relevante que su contenido específico de células inmunes. Diferentes citoquinas pueden promover o inhibir el desarrollo y progresión del tumor, independientemente de su fuente ( Lin y Karin, 2007 ). A través de la activación de diversos efectores aguas abajo, tales como NF-kB, AP-1, STAT y de transcripción SMAD factores, así como las caspasas, las citocinas controlan el medio inmune e inflamatoria a cualquiera de favorecer la inmunidad anti-tumor (IL-12, TRAIL, IFN- ) o mejorar la progresión del tumor (IL-6, IL-17, IL-23) y también tienen efectos directos sobre el crecimiento celular del cáncer y la supervivencia (TRAIL, FasL, TNF-α, los ligandos de EGFR, TGF-β, IL-6).
TAM son uno de los jugadores más importantes en el campo de la inflamación y el cáncer y una importante fuente de citoquinas ( Mantovani et al., 2008 ). En analogía con las células Th1 y Th2 T, los macrófagos se pueden clasificar en M1 y M2 tipos ( Sica et al., 2008 ). Macrófagos M1, activados por IFN y productos microbianos, expresan altos niveles de citocinas pro-inflamatorias (TNF-α, IL-1, IL-6, IL-12 o IL-23), complejos moléculas de histocompatibilidad principal (MHC) y nítrico inducible la sintasa de óxido y son capaces de matar agentes patógenos y cebado respuestas inmunes anti-tumorales. Por el contrario, M2 o macrófagos “alternativamente” activados, que son inducidos in vitro por la IL-4, IL-10 e IL-13, regular a la baja de MHC de clase II y la IL-12 expresión y muestran una mayor expresión de la citoquina antiinflamatoria IL- 10, receptor scavenger A, y la arginasa. La mayoría de TAM se considera que tienen un fenotipo M2 mientras que promueve la angiogénesis tumoral y la remodelación de tejidos ( Sica et al., 2008 ). Sin embargo, las citocinas promotoras de tumor más confirmados son “citoquinas M1”, mientras que la IL-10, una citocina M2, puede ser supresor del tumor como se muestra en en el cáncer colorrectal ( Berg et al., 1996 ; Lin y Karin, 2007 ). Además, a diferencia de las células Th1 y Th2, M1 y M2 macrófagos son de plástico y su fenotipo se define por su gen prolife expresión en lugar de por las vías de diferenciación deterministas y opciones de linaje.
Otras células inmunes también afectan a la tumorigénesis ( Tabla 1 ). Los neutrófilos pueden desempeñar ambas funciones de promoción de tumores y tumoricidas, dependiendo de su estado de diferenciación y la presencia de TGF-β ( Fridlender et al., 2009 ). Linfocitos B y mastocitos también son importantes contribuyentes a crecimiento del tumor inmunomediada ( Ammirante et al., 2010 ; de Visser et al., 2006 ; . Soucek et al, 2007 ) y los macrófagos convencionales y las células dendríticas son importantes para la presentación de antígenos y la activación de células T durante la inmunidad anti-tumor, así como para la producción de citoquinas y la inmunosupresión en tumores establecidos.
La iniciación del tumor es un proceso en el que las células normales adquieren el primer golpe mutacional que los envía en la pista tumorigénico proporcionando crecimiento y ventajas de supervivencia sobre sus vecinos. En la mayoría de casos, sin embargo, una única mutación es insuficiente y muchos tipos de cáncer requieren por lo menos 4-5 mutaciones ( Fearon y Vogelstein, 1990 ; Hanahan y Weinberg, 2000 ). También es imprescindible que cada mutación se transmite a la progenie de la célula, y en los cánceres que surgen dentro de los epitelios rápidamente renovados (cánceres intestinales y de la piel), las mutaciones oncogénicas deben ocurrir en cualquiera de las células madre vivió mucho tiempo o células amplificadoras transitorias y no dentro de las células diferenciadas , que se elimina rápidamente antes de la próxima mutación puede atacar. Alternativamente, las mutaciones oncogénicas pueden ocurrir dentro de las células epiteliales diferenciadas, tales como hepatocitos, que son capaces de proliferación y están suficientemente larga vida para permitir accesos mutacionales posteriores.
Se ha sugerido que un microambiente inflamatorio puede aumentar las tasas de mutación, además de mejorar la proliferación de las células mutadas. Células inflamatorias activadas sirven como fuentes de especies reactivas de oxígeno (ROS) y productos intermedios de nitrógeno reactivos (RNI) que son capaces de inducir daño en el ADN y la inestabilidad genómica ( Figura 3A ). Sin embargo, no está claro si ROS y RNI producidos y liberados por los neutrófilos o macrófagos (principalmente durante la inflamación aguda) están suficientemente larga vida a difundirse a través de la matriz extracelular, entrar en las células epiteliales, cruzan su citoplasma, entrar en el núcleo y reaccionan con ADN empaquetado en la cromatina. Alternativamente, las células inflamatorias pueden usar citoquinas, tales como TNF-α para estimular la acumulación de ROS en la vecina células epiteliales ( Figura 3A ). Por ello, ha sido objeto de debate si los mecanismos inmunes en contraposición a los mutágenos dietéticos y ambientales son las fuerzas de conducción críticas detrás de la iniciación del tumor ( Hussain et al., 2003 ). Sin embargo, las mutaciones de p53, presumiblemente causadas por el daño oxidativo, se encontraron tanto en las células cancerosas y en inflamado, pero no displásico, el epitelio en CAC, lo que sugiere que la inflamación crónica provoca cambios genómicos ( Kraus y Arber, 2009 ). La inflamación crónica provocada por el sulfato de colon irritante de dextrano sódico (DSS) puede inducir daño al ADN que da lugar a adenomas de colon ( Meira et al., 2008 ). Sin embargo, en su propia DSS es un carcinógeno pobres ( Okayasu et al., 1996 ).
Papel de la inflamación en la iniciación del tumor y la promoción
Mutagénesis inflamación inducida también puede resultar en la inactivación o la represión de genes de respuesta de reparación de genes y ROS también puede causar la inactivación oxidativa directa de las enzimas de reparación de genes ( Colotta et al., 2009 ; Hussain et al., 2003 ). Una vez que el sistema de reparación de genes se ha desmantelado, mutagénesis inducida por inflamación se mejora y varios supresores importantes tumorales, tales como Tgfbr2 y Bax, que albergan secuencias de microsatélites, se puede inactivar ( Colotta et al., 2009 ).
Otro mecanismo que une la inflamación a mutaciones oncogénicas es la regulación positiva de AID (inducida por activación citidina desaminasa), una enzima que promueve el cambio de clase de genes de inmunoglobulina catalizando desaminación de citosinas en el ADN ( Okazaki et al., 2007 ). Además de las células B, donde se descubrió, AID se sobreexpresa en muchos cánceres de diversos orígenes y su expresión es inducida por citoquinas inflamatorias en un modo de NF-KB dependiente o por TGF- ( Okazaki et al., 2007 ). AID induce la inestabilidad genómica y aumenta la probabilidad de mutación durante propenso a errores unión de roturas de la doble hebra de ADN, un proceso encontró para introducir mutaciones en los genes del cáncer críticos, incluyendo Tp53, c-Myc, y Bcl-6 ( Colotta et al., 2009 ) . AID contribuye a la formación de linfomas, y gástrico y los cánceres de hígado ( Okazaki et al., 2007 ; Takai et al., 2009 ). También se han sugerido otros mecanismos de mutagénesis inflamación inducida, incluyendo los efectos de la inflamación en la recombinación no homóloga y la inactivación mediada por NF-KB de vigilancia genoma dependiente de p53 ( Colotta et al., 2009 ).
En Giα2 ratones knockout, que se desarrollan inflamación colónica espontánea y el cáncer, enterocitos pierden selectivamente la expresión de los componentes implicados en la reparación desajuste, es decir, MLH1 y PMS2, debido a deacetylase- histonas y DEC-1 mediada por la represión epigenética de la Mlh1 promotor ( Edwards et al ., 2009 ). Otros hallazgos implican mecanismos epigenéticos, incluyendo silenciamiento basada en microARN y la metilación del ADN, en la inactivación de supresores de tumores, tales como INK4a y APC, y otros cambios que acompañan a la iniciación del tumor ( Cooper y Foster, 2009 ). Recientemente, la inflamación se ha conectado a la reprogramación epigenética por la proteína JmjC-dominio Jmjd3, que está codificada por un gen diana de NF-? B ( De Santa et al., 2007 ). En el cáncer intestinal asociado con la inflamación en / 2 GPx1 ratones knockout, inflamación induce metiltransferasa de ADN (DNMT) la metilación del ADN dependiente y el silenciamiento de una gran cohorte de genes diana Polycomb grupo, algunos de los cuales también son silenciados por metilación en cáncer de colon humano ( Hahn et al., 2008 ). Sin embargo, queda por demostrar que cualquiera de estos mecanismos epigenéticos inflamación inducida en realidad hace una contribución crítica a la iniciación del tumor, ya sea en un modelo de ratón adecuado o por medio de análisis prospectivo de muestras humanas.
Otro mecanismo por el que la inflamación puede mejorar la iniciación del tumor es la producción de factores de crecimiento y citoquinas que pueden conferir una de las células madre como fenotipo sobre progenitores tumorales o estimular la expansión de células madre, ampliando así la piscina célula que es reconocida por mutágenos ambientales. De hecho, STAT3 está vinculado tanto a la reprogramación de células madre y el vástago de renovación celular ( Chen et al., 2008 ), mientras que NF-KB puede mejorar la señalización de Wnt / β-catenina en criptas del colon ( Umar et al., 2009 ). La citoquina pro-inflamatoria TNF-α promueve la entrada nuclear de β-catenina durante cáncer gástrico asociado con la inflamación en ausencia de cualquier mutación en componentes de la ruta / β-catenina Wnt ( Oguma et al., 2008 ).
La conexión entre la inflamación y la iniciación del tumor no es una calle de una sola vía y también hay evidencia de que el daño del ADN puede conducir a la inflamación y promover así la tumorigénesis. Uno de los mejores ejemplos es proporcionada por el modelo de carcinoma hepatocelular inducida por la dietilnitrosamina carcinógeno (DEN) en la que el daño del ADN contribuye a la muerte celular necrótica, resultando en una reacción inflamatoria que promueve el desarrollo del tumor ( Maeda et al., 2005 ; Sakurai et al., 2008 ). Un número de oncoproteínas (RAS, Myc, RET) se puede activar vías que llevan a la producción de citoquinas pro-inflamatorias y quimiocinas (IL-6, IL-8, IL-1ß, CCL2, CCL20) de señalización ( Mantovani et al., 2008 ) . Estrés genotóxico también puede inducir la expresión de miembros de la familia de NKG2D, que sirven como ligandos para receptores de células NK y γδT ( Strid et al., 2008 ) dando como resultado o bien eliminación de células estresadas o una respuesta inflamatoria local. En la misma línea, la supresión de mosaico de la ATR gen de reparación del ADN y Tp53 en los resultados de la piel en el reclutamiento de CD11b + Gr1 + células mieloides, como parte de una respuesta inmune prototípica de “auto alterado” ( Ruzankina et al., 2009 ) . La reparación del ADN defectuoso causado por una deficiencia de la exonucleasa Fen1 también resulta en un tumor promover la respuesta inflamatoria que es impulsado por el ADN dañado, lo más probable a través de la activación de un receptor de reconocimiento de patrones ( Zheng et al., 2007 ).
Ir:
La promoción de tumores es el proceso de crecimiento del tumor de una sola célula iniciados en un tumor primario totalmente desarrollado. El crecimiento del tumor inicial depende de aumento de la proliferación celular y la reducción de la muerte celular, ambos de los cuales son estimulados por los mecanismos de la inflamación impulsada. De hecho, muchos de los efectos potenciadores de la inflamación en el cáncer se ejercen a nivel de la promoción de tumores y promotores tumorales más conocidos, por ejemplo los ésteres de forbol, son potentes inductores de la inflamación ( Karin, 2006 ). La promoción de tumores inducidos por la inflamación puede ocurrir temprano o tarde en el desarrollo del tumor y puede conducir a la activación de las lesiones pre-malignas que estaban en estado latente durante muchos años. Los mecanismos mediante los cuales la inflamación afecta a la promoción de tumores son numerosas y además de aumento de la proliferación y la supervivencia mejorada, también pueden implicar el llamado cambio angiogénico, que permite un pequeño tumor latente para recibir el suministro de sangre necesaria para la siguiente fase de crecimiento ( Lewis y Pollard, 2006 ). Mecanismos de promoción de tumores inflamación impulsada se discuten a continuación.
Producción de tumor promoción de citoquinas por las células inflamatorias / inmunológicas que activan factores de transcripción, como NF-kB, STAT3 y AP-1, en las células pre-malignas para inducir genes que estimulan la proliferación celular y la supervivencia, es una promoción de mecanismo de tumor mayor ( figura 3B ). La evidencia inicial para la promoción de tumores mediada por inflamación vino de modelos de ratón de la piel, colon, y cáncer de hígado. Aunque contrario a la intuición en el momento, se encontró TNF-α que se requiere para la carcinogénesis de la piel de dos etapas ( Moore et al., 1999 ). TNF-α activa tanto de AP-1 y NF-? B factores de transcripción, pero en la piel sus efectos promotores de tumores están mediadas por AP-1 ( Eferl y Wagner, 2003 ), que fue identificado como un factor de transcripción cuya actividad es estimulada por la promotor clásico tumor acetato de tetradecanoilforbol (TPA) ( Ángel et al., 1987 ). Por el contrario, el NF-kappa B inhibe el desarrollo del cáncer de piel ( Zhang et al., 2004 ). Así, aunque una citoquina dada puede activar varios factores de transcripción, su tumor promoción de la actividad puede ser mediada por sólo uno de ellos y antagonizada por otro. Como veremos más adelante, una situación similar se puede aplicar a cáncer de hígado. Entre los diferentes factores de transcripción que son parte de este mecanismo, NF-KB y STAT3 se activan en la mayoría de los cánceres y actúan como oncogenes no clásicos, cuya activación en las células malignas rara vez es el resultado de mutaciones directas, y en su lugar depende de señales producido por células vecinas o más raramente en la activación mutacional de componentes de señalización aguas arriba. NF-kappa B y STAT3 activan genes que controlan la supervivencia celular, la proliferación y el crecimiento, así como la angiogénesis, invasividad, la motilidad, la quimiocina, y la producción de citoquinas ( Grivennikov y Karin, 2009 ; . Yu et al, 2009 ).
Factores de transcripción oncogénicos también pueden ser activadas a través de receptores de reconocimiento de patrones por los componentes de bacterias y virus ( Rakoff-Nahoum y Medzhitov, 2009 ). Sin embargo, la contribución total de los receptores de reconocimiento de patrones en las células epiteliales frente a los expresados por las células inmunes / inflamatorias a la promoción de tumores está lejos de ser clara y requerirá el análisis de ratones knockout específica de tipo celular. Incluso los agonistas específicos que activan estos receptores en el cáncer no se definen. No obstante, el papel de las citoquinas que se producen en respuesta al daño-asociado (DAMP) o asociado a patógenos (PAMP) patrones moleculares en el desarrollo de tumores está más firmemente establecida. Por ejemplo, AP-1 de activación en el cáncer de la piel depende en gran medida de señalización de TNF-TNFR1 ( Balkwill, 2009 ), mientras que la activación de STAT3 en células de cáncer depende en gran medida de una gran cantidad de factores de crecimiento y citoquinas, incluyendo IL-6, IL-11, tirosina quinasas oncogénicas, tales como c-Met y Src IL-22, HGF y EGF, y ( . Bollrath et al, 2009 ; Grivennikov et al., 2009 ; Naugler et al., 2007 ; . Yu et al, 2009 ) .
Se obtuvo el primero evidencia genética crítica para células inflamatorias como fuente de citoquinas promotores de tumores en un modelo de ratón de CAC, en donde la inactivación de NF-KB en células mieloides redujo el crecimiento del tumor y bloqueó la producción de IL-6 y otras citoquinas en respuesta a colitis ( Greten et al., 2004 ). El trabajo posterior demostró que el efecto de las células inmunes (macrófagos, células T) en el crecimiento CAC está mediada por IL-6, IL-11, TNF-α e IL-1β ( Becker et al., 2004 ; . Bollrath et al, 2009 ; . Grivennikov et al, 2009 ; Popivanova et al., 2008 ), así como otras citoquinas, tales como IL-23. IL-11 juega un papel similar en el cáncer gástrico ( Ernst et al., 2008 ), en la que IL-1β es también un promotor tumoral ( Tu et al., 2008 ). TNF-α también promueve HCC en ratones que carecen de la Mdr2 P-glicoproteína, que se desarrollan inflamación colestática seguido por el carcinoma hepatocelular (CHC) ( Pikarsky et al., 2004 ). HCC también puede promoverse por otro miembro de la familia TNF, linfotoxina β ( Haybaeck et al., 2009 ). TNF-α junto con IL-6 contribuye a la promoción de tumores obesidad mediada en HCC ( Park et al., 2010 ). Este último efecto se correlaciona con la capacidad del TNF-α e IL-6 para promover hepatosteatosis y esteatohepatitis ( Park et al., 2010 ). Una de las citoquinas más críticos promotores de tumores en HCC es IL-6. Los ratones deficientes en IL-6 a desarrollar mucho menos HCC en respuesta a la DEN pro-carcinógeno químico y la producción sesgo de género de IL-6 cuentas para la carga HCC mucho mayor en los hombres ( Naugler et al., 2007 ). Los altos niveles circulantes de IL-6, están asociados con factores de riesgo de HCC, incluyendo hepatosteatosis, la obesidad, y la cirrosis hepática, y son los mejores predictores de la progresión rápida de la hepatitis viral a HCC en seres humanos ( Wong et al., 2009 ).
En CAC y HCC, el efecto promotor del tumor de IL-6 se ejerce principalmente a través de STAT3, cuya celda tipo específico inactivación en los hepatocitos y enterocitos inhibe el desarrollo de estos tumores malignos en ratones tratados con DEN o azoximetano (AOM) y DSS, respectivamente ( Bollrath et al., 2009 ; . Grivennikov et al, 2009 ; Park et al., 2010 ). Desarrollo de CAC en ratones depende también mediada por IKK activación de NF-KB en los enterocitos, cuya función importante en este modelo se aumenta la supervivencia de las células pre-malignas ( Greten et al., 2004 ). Se propuso un papel similar para NF-? B en el desarrollo de HCC en ratones deficientes en Mdr2 y en ratones linfotoxina-transgénico ambos de los cuales exhiben inflamación crónica del hígado ( Haybaeck et al., 2009 ). Sin embargo, en el modelo DEN de HCC y Helicobacter cáncer gástrico impulsada, NF-kB promueve hepatocitos y la supervivencia de las células epiteliales y actúa como un inhibidor del desarrollo de tumores ( Maeda et al., 2005 ; . Shibata et al, 2009 ). Lo más probable, los diversos efectos de NF-KB en diferentes modelos se determinan por el mecanismo de inducción de tumor y el tipo de respuesta inflamatoria involucrado en la promoción de tumores. Mdr2 knockout y los ratones linfotoxina-transgénicos exhiben un nivel muy bajo de la muerte de hepatocitos normal, que no se ve reforzada por la ausencia de NF-kappa B ( Haybaeck et al., 2009 ; Pikarsky et al., 2004 ). En estos ratones, NF-kappa B en hepatocitos es principalmente responsable de la propagación de la inflamación a través de la inducción de quimiocinas, que reclutan células inmunes / inflamatorias en el hígado. Por el contrario, los ratones tratados DEN exhiben una respuesta inflamatoria aguda desencadenada por la liberación de IL-1α de hepatocitos necróticos ( Sakurai et al., 2008 ). IL-1α induce la producción de IL-6 por las células de Kupffer y esta respuesta impulsa la proliferación compensatoria de los hepatocitos sobrevivientes (un tipo de una respuesta de curación de heridas); cuanto mayor sea la cantidad de muerte celular – cuanto mayor es la respuesta regenerativa. Al suprimir la acumulación de ROS y prevención de la necrosis de los hepatocitos, NF-kappa B inhibe la inducción de HCC en los ratones tratados DEN ( Maeda et al., 2005 ).
Otra citoquina promotora de tumores es IL-23 ( Langowski et al., 2006 ). IL-23 se expresa en su mayoría por TAMs de una manera dependiente de STAT3 y NF-kappa B ( Kortylewski et al., 2009 ). IL-23 bloqueo con anticuerpos neutralizantes o inactivación genética del gen de IL-23p19 disminuir dramáticamente el número de tumores y el crecimiento en el modelo de dos etapas de la carcinogénesis de piel ( Langowski et al., 2006 ). En parte, los efectos pro-tumorigénicas de IL-23 pueden ser mediados por IL-17 e IL-22 por las células Th17, pero otros efectos de las células mieloides IL-23 en los CTL, células T reguladoras, y no deben ser descontados. Un pariente cercano de IL-23 es IL-12, que comparte con la IL-23 de la subunidad IL-12p40 y está implicado en la diferenciación de Th1, la producción de IFN, y la activación de la inmunidad anti-tumor ( Trinchieri et al., 2003 ). La secreción de IL-23 y IL-12 de secreción son recíprocamente regulado y el interruptor de IL-12 para la producción de IL-23 puede ser un importante evento promotor de tumores. La activación de STAT3, PGE 2 , ATP, y aumentar el ácido láctico producción de IL-23 por TAM ( Kortylewski et al., 2009 ; . Shime et al, 2008 ). Las dos últimas agonistas enlazan necrosis cáncer de células (inducida por la hipoxia o la terapia) y el efecto Warburg (el interruptor de la fosforilación oxidativa de la glucólisis) para la producción de IL-23, desplazando de este modo la inmunidad anti-tumor a la promoción de tumores.
Un circuito similar puede ser ejecutado por células de origen mieloide supresores (MDSC) que produzcan arginase1 y indolamina-2,3-dioxigenasa, que son enzimas que amortiguan la inmunidad anti-tumor a través de la interferencia con la activación de células T ( Gabrilovich y Nagaraj, 2009 ). Tomados en conjunto, la inflamación crecimiento unidades de tumor asociado a un tumor, la angiogénesis y pueden perpetuarse mediante una extensa red de citocinas y quimiocinas, que son producidos por el sistema inmunitario, estromales y células malignas en respuesta a diversas señales ( Figura 3B ).
Teniendo en cuenta que varias citocinas (IL-1, TNF, IL-6, IL-23) y los factores de transcripción (AP-1, NF-kappa B, STAT3) son críticos tanto para la inflamación y el crecimiento tumoral, controlan centros de señalización pro-tumorigénico que pueden ser dirigidos a reducir tanto asociado a tumor inflamación y el crecimiento tumoral (véase abajo). Interferencia farmacológica con la señalización de citoquinas disminuye la tumorigénesis, así como el crecimiento del cáncer ( Becker et al., 2004 ; . Grivennikov et al, 2009 ; Hedvat et al., 2009 y por lo tanto puede servir como base para los enfoques preventivos y terapéuticos). En total, la producción de citoquinas por las células inmunes e inflamatorias es un importante mecanismo de promoción de tumor que proporciona las células malignas con un suministro continuo de las señales de crecimiento y la supervivencia en un microambiente inicialmente hostil. En la mayoría de los casos, las citoquinas promotores de tumores actúan de una manera paracrina, sin embargo, varios tipos de células cancerosas producen sus propias citoquinas, incluyendo IL-6, para lograr el mismo efecto ( Gao et al., 2007 ).
Ir:
La inflamación y la angiogénesis
El crecimiento de tumores grandes requiere un mayor suministro de sangre intratumoral. Esto es provocado por la hipoxia del tumor, que promueve la angiogénesis y aumenta la probabilidad de metástasis. Además de la hipoxia, la angiogénesis tumoral depende de reclutamiento de TAM, que detectan señales de hipoxia y a su vez producen quimiocinas y factores pro-angiogénicos. El reclutamiento de precursores de TAM depende en gran medida de los mediadores angiogénicos tales como angiopoyetina 2 y factor de crecimiento endotelial vascular (VEGF). Importantes genes pro-angiogénicos, tales como IL-8, CXCL1, CXCL8, VEGF y la hipoxia inducible factor 1 alfa (HIF1a), están regulados directamente por NF-KB, STAT3 y AP-1 en TAMs, MDSCs, y otros tipos de células ( . Kujawski et al, 2008 ; Rius et al., 2008 ).
Bajo condiciones de hipoxia, HIF-1α estimula la expresión de CXCL12, que activa y recluta células endoteliales de una manera dependiente de CXCR4 ( Sica et al., 2008 ). La formación de nuevos vasos linfáticos está regulada por VEGF-C y VEGF-D, mientras que VEGF-A facilita el reclutamiento de monocitos, que activan lymphoangiogenesis ( Murdoch et al., 2008 ). VEGF-A producida por células mieloides también inhibe la maduración de pericitos y la cobertura endotelial de los vasos sanguíneos recién formados, y su ablación condicional acelera la tumorigénesis ( Stockmann et al., 2008 ). El reclutamiento de Gr1 + células mieloides (presumiblemente MDSC y TAM precursores) en los tumores, restringe los efectos de la terapia anti-VEGF, presumiblemente sin pasar por el requisito para la producción de VEGF locales por las células cancerosas para el reclutamiento de precursores de TAM ( Shojaei et al., 2007 ) . Como la mayoría de tumores de crecimiento contienen algunas áreas de la hipoxia, no es claro si la hipoxia es el conductor directa de la angiogénesis del tumor o si los estímulos hipóxicos generar señales inflamatorias que conducen a la angiogénesis. La inactivación de NF-kappa B o STAT3, la neutralización de CCL2 o CXCL12, o el agotamiento TAM inequívocamente como resultado en la angiogénesis alterada y disminuyó el crecimiento del tumor, lo que subraya el papel crítico de mediadores inflamatorios en la angiogénesis tumoral ( Joyce y Pollard, 2009 ; . Kujawski et al, 2008 ).
Ir:
Los genes diana que median en la promoción de tumores
La mayoría de los genes que median el tumor promover las funciones de NF-KB, STAT3, y AP-1 no han sido plenamente definidos y muy probablemente los efectos pro-tumorigénicas de estos factores de transcripción se ejercen a través de múltiples efectores. Algunos objetivos pueden ser controladas por más de un factor de transcripción y pueden ser más importantes en un tipo de célula que en otro. La expresión de las proteínas anti-apoptóticas Bcl-2 y Bcl-X L , por ejemplo, son promovidas por tanto NF-KB y STAT3 como son c-IAP1, c-IAP2, MCL-1, c-FLIP, y survivina ( Karin, 2006 ; . Yu et al, 2007 ). Mientras que Bcl- Lpuede ser el más prominente de genes anti-apoptóticos en los enterocitos ( Greten et al., 2004 ), c-FLIP parece cumplir la misma función en los hepatocitos ( Chang et al., 2006 ). Tanto NF-KB y STAT3 interfieren con la síntesis de p53 y atenúan vigilancia genómica mediada por p53, lo que representa otro potencial mecanismo promotor de tumores ( Colotta et al., 2009 ).
STAT3 controla la expresión de las ciclinas D1, D2 y B, así como el proto-oncogén c-Myc, y a través de ellos que puede estimular la proliferación celular ( Bollrath et al., 2009 ; Yu et al., 2007 ). Aunque la ciclina D y c-Myc también se cree que ser regulada por NF-? B, la inactivación de IKK en los enterocitos no interfiere con la proliferación celular ( Greten et al., 2004 ) y en los queratinocitos Rastransformed ( Zhang et al., 2004 ) o hepatocitos DEN-iniciado ( Maeda et al., 2005 ) la inhibición de NF-? B en realidad aumenta la expresión de la ciclina D y la proliferación celular. La proteína AP-1 c-Jun coopera con STAT3 en la represión de la expresión de Fas por las células tumorales, atenuando de esta manera su sensibilidad a la apoptosis instructivo ( Eferl y Wagner, 2003 ). Adicional de NF-KB y objetivos de STAT3 de control de células y el tejido la resistencia al estrés y lesiones e incluyen proteínas antimicrobianas (RegIIIβ, RegIIIγ, TFF3), proteínas de choque térmico, y antioxidantes, tales como superóxido dismutasa 2 (SOD2) y ferritina pesada cadena (FHC) ( Bollrath et al., 2009 ; Karin, 2006 ).
Por último, otra categoría de genes diana que promueven la tumorigénesis son citocinas y quimiocinas que actúan en modales autocrina o paracrina para asegurar el reclutamiento continuo de células inflamatorias en el microambiente tumoral. La perpetuación de la inflamación crónica se logra en gran medida a través de bucles de retroalimentación positiva, que incluyen células inflamatorias que producen citocinas que inducen la síntesis de quimioquinas en las células malignas y estromales que conducen al reclutamiento prolongada de células inflamatorias en el microambiente del tumor ( Figura 3 ). Células TAMs, MDSCs, Tregs, y Th17 son los subconjuntos de células inmunes más críticos a este respecto. El reclutamiento de células mieloides se rige por múltiples vías, incluyendo CCL2-CCR2, CCL1-CXCR2, S100A proteínas-RAGE, y la IL-1-IL-1R interacciones ( Bonecchi et al., 2009 ). La señalización a través CCR6 es crítica para la infiltración Th17, mientras que las células Treg son atraídos principalmente a través de CCR4 y CCR7 ( Bonecchi et al., 2009 ). En algunos casos, las quimiocinas críticos no son producidas por células cancerosas, pero se inducen en los fibroblastos asociados a tumores tras la interacción con células de carcinoma ( Liao et al., 2009 ; Orimo et al., 2005 ; Orimo y Weinberg, 2006 ).
Ir:
Inflamación y malignidades linfoides
Condiciones inflamatorias crónicas también están asociados con neoplasias linfoides. Un ejemplo excelente es proporcionado por el tejido linfoide asociado a la mucosa (MALT) linfomas, que se producen en el contexto de la inflamación crónica causada por agentes infecciosos, tales como Helicobacter pylori (el linfoma gástrico más comúnmente encontrado), Chlamydia psittacii (adnexal ocular linfoma MALT) y Borrelia burgdorferi (linfoma MALT cutánea) ( Ferreri et al., 2009 ). Otro ejemplo es el virus de Epstein-Barr (EBV), que es responsable de gran linfoma de células B en pacientes inmunocomprometidos, el linfoma de Burkitt y el linfoma de Hodgkin ( Ferreri et al., 2009 ).
Se ha propuesto que la estimulación repetida antigénica, la autoinmunidad y la inflamación son factores de riesgo para la leucemia linfocítica crónica (CLL), la malignidad hematopoyética más común que representa el 30% de todas las leucemias ( Chiorazzi et al., 2005 ). Un mecanismo mediante el cual tales estímulos promover el desarrollo CLL es la inducción de factor de células B de activación (BAFF), un miembro de la familia TNF, ha demostrado recientemente para acelerar el desarrollo de la enfermedad CLL-como en ratones ( Enzler et al., 2009 ). Las citocinas (tales como IL-4 y VEGF), quimioquinas (tales como SDF-1), y las interacciones con las células del estroma de la médula ósea apoyar la expansión CLL y suprimir la apoptosis a través de la regulación positiva de Bcl-2, survivina, y MCL-1 ( Granziero et al ., 2001 ; Pedersen et al., 2002 ). Esto ocurre en pseudofollicles de ganglios linfáticos y los racimos de la médula ósea, donde las células leucémicas interactúan con componentes del microambiente inflamatorio que apoyan su supervivencia. Otro ejemplo para el papel de la inflamación en enfermedades malignas linfoides son los linfomas que aparecen en GM-CSF y ratones IFN-deficientes, que son causadas por infecciones y regresión después del tratamiento con antibióticos ( Enzler et al., 2003 ).
Una situación similar puede producirse en el mieloma múltiple. A través de la secreción de IL-6, IGF-1, VEGF, TNF-α, SDF-1 y BAFF, elementos estromales promover la supervivencia y migración de células plasmáticas neoplásicas y también confieren resistencia a los medicamentos ( Kastritis et al., 2009 ). IL-6 es de particular importancia, ya que actúa tanto en paracrino y autocrino modales y IL-6-ratones deficientes son resistentes a la inducción de mieloma múltiple ( Hodge et al., 2005 ). A pesar de la activación de NF-kappa B constitutiva, mieloma múltiple sigue dependiendo de factores extrínsecos, y las drogas dirigidas a IL-6 se están evaluando en combinación con el inhibidor del proteasoma bortezomib para el tratamiento de esta malignidad ( Kastritis et al., 2009 ).
Ir:
La inflamación y la metástasis
Desde una perspectiva clínica, la metástasis es el aspecto más crítico de la tumorigénesis, ya que más del 90% de la mortalidad por cáncer es causado por la metástasis. Estudios recientes muestran sin ambigüedad que la metástasis requiere una estrecha colaboración entre las células cancerosas, células inmunes e inflamatorias, y los elementos del estroma. El proceso de la metástasis puede dividirse groseramente en cuatro pasos principales. El primer paso está representada por la transición epitelio-mesenquimal, en la que las células cancerosas adquieren características fibroblastoides que aumentan su motilidad y les permiten invadir revestimientos epiteliales / membranas basales y alcanzan los vasos sanguíneos eferentes o linfáticos ( Kalluri y Weinberg, 2009 ). La pérdida de expresión de E-cadherina se concibe como un acontecimiento clave en la transición epitelio-mesenquimal. En la segunda etapa, las células cancerosas intravasate en los vasos sanguíneos y linfáticos. La inflamación puede promover esto a través de la producción de mediadores que aumentan la permeabilidad vascular. Esto es seguido por la tercera etapa en la que la metástasis de células que inician sobrevivir y viajar a través de la circulación. Se ha estimado que sólo el 0,01% de las células cancerosas que entran en la circulación finalmente sobrevivir y dar lugar a micrometástasis ( Joyce y Pollard, 2009 ). A continuación, la detención mediada por la integrina permite la extravasación de células cancerosas circulantes. Finalmente, progenitores metastásicas individuales interactúan con, y células estromales inmunes, inflamatorias y comienzan a proliferar ( Polyak y Weinberg, 2009 ). Algunas de estas células ya pueden ser dirigidos a la nicho pre-metastásico en respuesta a las señales inflamatorias generado tumorales antes de la llegada de las células de cáncer de metástasis iniciadoras ( Kaplan et al., 2005 ). Una de estas señales inflamatorias es la extracelular versicano componente de la matriz, lo que conduce a la activación de macrófagos y la producción de la citoquina promotora de metástasis TNF-α ( Kim et al., 2009 ). Sin embargo, ha sido difícil determinar si la producción versicano por las condiciones células cancerosas metastásicas el futuro lugar de la metástasis antes de su llegada.
TGF es una citoquina anti-inflamatoria producida por células cancerosas, células mieloides y linfocitos T. La señalización de TGF- es un importante regulador de la transición y la metástasis epitelial-mesenquimal, y elevada TGF- se asocia a menudo con un mal pronóstico ( Yang y Weinberg, 2008 ). TGF activa SMAD factores de transcripción y MAPKs, que controlan la expresión de otros reguladores de la transición epitelial-mesenquimal, tales como Slug ( Yang y Weinberg, 2008 ). TGF sin embargo, también suprime la proliferación de células epiteliales y el crecimiento tumoral temprano, haciendo que algunos tumores de adquirir mutaciones inactivantes en los componentes de señalización de TGFß ( Yang y Weinberg, 2008 ). A pesar de los defectos en la señalización de TGF-, tales tumores todavía pueden hacer metástasis. Estos efectos opuestos de TGF- en diferentes etapas de desarrollo de tumores esperan explicación mecanicista. La interrupción de TGF señalización en células de cáncer también se traduce en la regulación positiva de la SDF1 (CXCL12) -CXCR4 y quimioquinas CXCL5-CXCR2: pares de receptores de quimiocinas e induce el reclutamiento rápido de MDSCs que promueven la metástasis y amortiguan las respuestas inmunes anti-tumorales ( Yang et al,. 2008 ). Se propuso la inactivación de la señalización de TGF para dar lugar a elevadas concentraciones locales TGFß que inhiben las respuestas de células T anti-tumorales e inducir la diferenciación de las células Th17 promotores de tumores ( Langowski et al., 2007 ).
Otro regulador crítico de la transición epitelial-mesenquimal es Snail, un represor de la transcripción E-cadherina en células epiteliales. Recientes hallazgos sugieren que Snail se estabiliza en respuesta a la señalización de TNF-α, un proceso que es crítico para la migración de células de cáncer y la metástasis ( Wu et al., 2009b ). Otros mecanismos mediante los cuales las citoquinas pro-inflamatorias pueden afectar a la transición epitelial-mesenquimal es a través de la inducción de STAT3 mediada por la transcripción de la torcedura y la inducción mediada por NF-KB de ambos Twist and Kiss ( Yu et al., 2009 ), Sin embargo, estos mecanismos permanecen ser confirmado in vivo, y un informe reciente sugiere que STAT3 es un regulador negativo de la transición adenoma-carcinoma en el cáncer de colon ( Musteanu et al., 2009 ).
Invasión de células cancerosas requiere una amplia proteólisis de la matriz extracelular en el frente invasivo. Las células inflamatorias son importantes fuentes de proteasas que degradan la matriz extracelular. En un modelo de cáncer invasivo de colon, CCR1 + células mieloides, cuyo reclutamiento es impulsado por el CCL9 quimiocina producido por las células cancerosas, promover la invasividad través de la secreción de la matriz de las metaloproteinasas de MMP2 y MMP9 ( Kitamura et al., 2007 ). IL-1, TNF-α e IL-6 promueven la expresión de MMP, invasividad y metástasis a través de NF-KB y STAT3 ( Yu et al., 2007 ).
Un mecanismo metastásico diferente dependiente de IKK opera en los cánceres de próstata y de mama. Como estos cánceres progresan, sus células malignas progresivamente acumulan activan IKK en sus núcleos ( Luo et al., 2007 ). En el cáncer de próstata, la acumulación de IKK nuclear activado se correlaciona con una expresión reducida de maspin, un inhibidor de la metástasis ( Luo et al., 2007 ). Activación IKK en la próstata metastásico y células de cáncer de mama está mediado por miembros de la familia TNF, es decir, la linfotoxina y RANKL y sus efectos represivos sobre la transcripción maspin son NF-KB independiente ( Luo et al., 2007 ). ¿Cómo estos linfocitos son reclutados en progresar tumores de mama y próstata sigue siendo desconocido. El reclutamiento de tales células puede ser una consecuencia de la necrosis tumoral, pero como se mencionó anteriormente ciertos carcinomas secretar activamente factores que regulan al alza la fibronectina y causar migración de receptor de VEGF 1 (VEGFR1) progenitores hematopoyéticos positivas con el nicho pre-metastásico ( Kaplan et al., 2005 ). Sin embargo, el nicho concepto premetastásico es algo misterioso, ya que no está claro cómo primaria células tumorales células inflamatorias directos a dichos sitios.
Alternativamente, un pequeño número de células metastásicas puede interactuar con y activar diferentes tipos de células mieloides a través de factores secretados como versicano ( Kim et al., 2009 ). Células de cáncer de pecho utilizan CSF-1 y CXCL12 para inducir el reclutamiento de TAM, que a su vez producir ligandos de EGF receptor (EGFR) ( Joyce y Pollard, 2009 ). Estas citoquinas también pueden mediar una interacción física entre TAM y células de carcinoma ( Condeelis y Pollard, 2006 ). TAM puede ser también “programado” por la infiltración de células T, particularmente células Th17 tumor ( Wang et al., 2009 ) y las células Th2 ( DeNardo et al., 2009 ). IL-13 y IL-4 producida por la infiltración de tumor CD4 + células T estimulan la M1 a M2 transición de TAM y por lo tanto soportan la metástasis pulmonar de las células cancerosas mamarias ( DeNardo et al., 2009 ). El agotamiento de TAM ( Joyce y Pollard, 2009 ) o CD4 +células T ( DeNardo et al., 2009 ) se reduce drásticamente la metástasis del cáncer de mama de ratón.
Una vez que las células metastásicas entren en la circulación, que necesitan para sobrevivir en suspensión y resistir la muerte celular inducida por desprendimiento o anoikis. La supervivencia de las células cancerosas en circulación se ve afectada por los mediadores inflamatorios liberados por las células inmunes en respuesta al cáncer derivado o estímulos derivados de patógenos ( Kim et al., 2009 ; Luo et al., 2004 ). Algunos de estos efectos dependen de la activación de NF-KB en células inflamatorias o en las células cancerosas. Una variedad de citoquinas presentes en el microambiente tumoral, incluyendo TNF-α, IL-6, y epirregulina, puede promover la supervivencia de circulación semillas metastásicos ( Nguyen et al., 2009 ). Además de NF-kB y la activación de STAT3, algunas de estas citoquinas pueden unir físicamente las células del cáncer de TAM, que les permite viajar juntos a través de la circulación ( Condeelis y Pollard, 2006 ). Por otro lado, las células metastásicas individuales, que ya no está presente dentro de un entorno inmunosupresor son, se pueden dirigir de nuevo por la inmunovigilancia. De hecho, en algunos casos, la infiltración de tumores por células T activadas disminuye la tasa de metástasis ( Galon et al., 2006 ; . Pages et al, 2005 ). La interacción de las células cancerosas circulantes con plaquetas o macrófagos pueden protegerlos de NK la destrucción mediada por células, superando de este modo la inmunovigilancia ( Palumbo et al., 2007 ).
Intravasación está regulada por las prostaglandinas (que se producen de una manera COX2 dependiente y actuar sobre el epitelio), por las citoquinas (tales como epirregulina, lo que aumenta la supervivencia de células de cáncer), y por MMPs (que despejar el camino para que este último migrar hacia capilares ( Nguyen et al., 2009 )). La migración de la metástasis de iniciar las células no es al azar y es dirigida por gradientes de quimioquinas detectadas a través de CXCR4, CCR4, CCR7, CCR9 y CCR10 ( Bonecchi et al., 2009 ).
El viaje de la semilla metastásico circulante termina momento de la detención dependiente de integrina en el endotelio, seguido por extravasación. Las moléculas como ANGPTL4, que está regulado por TGF, facilitan la extravasación en los pulmones por la mediación de contacto entre células malignas y endoteliales ( Nguyen et al., 2009 ). La inflamación sistémica mejora la unión de las células cancerosas circulantes a sinusoides hepáticos y este proceso se rige por la regulación positiva de neutrófilos dependiente de moléculas de adhesión ( McDonald et al., 2009 ). Varias citoquinas proinflamatorias que están elevados en la circulación de pacientes con cáncer upregulate expresión de moléculas de adhesión en el endotelio o en los órganos diana y por lo tanto aumentan la probabilidad de la unión celular metastásico ( Mantovani et al., 2008 ).
Ir:
La inmunidad y la tumorigénesis
Como se discutió anteriormente, en los tumores que surgen en el contexto de la inflamación subyacente o en tumores avanzados que contienen infiltrados inflamatorios, el efecto neto del sistema inmune (tanto innata y adaptativa) es la estimulación del crecimiento del tumor y la progresión. Sin embargo, las células cancerosas representan un “auto alterado” y expresan antígenos “no propias” en el contexto de señales de estrés y de peligro que pueden promover la presentación de antígenos. Por lo tanto, los tumores incluso en crecimiento pueden estar sujetos a la inmunovigilancia y la destrucción por las células T y NK activadas ( Dunn et al., 2004 ). Es probable que la inmunovigilancia y la inflamación promotor de tumores pueden coexistir incluso en el mismo tumor ( Bui y Schreiber, 2007 )
Según la hipótesis de la inmunovigilancia, células NK y CTLs se involucran en el asesinato tumor (a través de perforina, granzima B, TRAIL o FasL mecanismos dependientes), mientras Th1 (en virtud de la producción de IFN) y en algunos casos las células Th17 (a través de la producción de IL-17A ) proporcionar una ayuda importante que aumenta la inmunidad citotóxica ( Dunn et al., 2006 ; Dunn et al., 2004 ; Martin-Orozco et al., 2009 ). Por otro lado, las células T reguladoras suprimen las respuestas inmunitarias antitumorales y por lo tanto son pro-tumorigénicos ( Dunn et al., 2004 ). Células NKT también pueden estar involucrados en la vigilancia de tumores hematopoyéticos y químicamente inducidos ( Crowe et al., 2005 ; Smyth et al., 2000 ; Swann et al., 2009 ). Otros componentes críticos de este sistema son las células dendríticas y los macrófagos, que antígenos presentes y responden a las señales de peligro y el estrés, así como inmunorreguladores y citotóxicos citoquinas, tales como IFN tipo I, IFN, FasL, TRAIL, GM-CSF e IL-12 ( Palucka et al., 2007 ; Smyth et al., 2006 ; Swann y Smyth, 2007 ).
La primera demostración experimental de la inmunovigilancia tumor llegó a partir del análisis de los ratones RAG2 deficientes, que carecen de linfocitos maduros. Estos ratones muestran una mayor desarrollo de una variedad de cánceres espontáneos por 14-16 meses de edad ( Shankaran et al., 2001 ). Sin embargo, incluso en ratones inmunocomprometidos, el desarrollo de tumores se produce en el período de post-reproductiva, lo que sugiere que el sistema inmune de los mamíferos no se somete a presión evolutiva sustancial para mejorar el reconocimiento del tumor y la eliminación. Sin embargo, en virallyor por bacterias promovido cánceres, el sistema inmune proporciona protección considerable a través de su capacidad para reconocer y eliminar microbios ( Smyth et al., 2006 ). La inactivación de diversos componentes del sistema de inmunovigilancia, tales como perforina, granzima, y la señalización de interferón, hace ratones susceptibles a la tumorigénesis ( Bui y Schreiber, 2007 ; Dunn et al., 2004 ). Los ratones que carecen citoquinas citotóxicas, tales como las formas unidas a la membrana de FasL o TRAIL muestran también una mayor desarrollo de sarcomas y otros tumores ( O’ Reilly et al., 2009 ; . Smyth et al, 2003 ).
Más evidencia de la inmunovigilancia de tumores y inmunoedición proviene de la presencia de linfocitos infiltrantes de tumores (tanto de linfocitos T y B) que reconocen antígenos tumorales y el pronóstico favorable para algunos pacientes cuyos tumores mostrar aumento de la infiltración con células T activadas ( Dunn et al., 2004 ) . Tal infiltración es aún más notable en tumores que se desarrollan inestabilidad de microsatélites o que tienen un fenotipo “mutator” y por lo tanto expresar antígenos tumorales que presentan mayores diferencias de homólogos normales ( Buckowitz et al., 2005 ; Guidoboni et al., 2001 ). La evidencia adicional pero indirecto para la inmunidad anti-tumor incluye varios casos de regresión espontánea de tumores acompañados de aumento de la infiltración de células citotóxicas activadas y presencia de anticuerpos y las células T que reconocen antígenos tumorales ( Swann y Smyth, 2007 ). Este último sugiere que los linfocitos B y T se han activado por antígenos específicos de tumores, pero no significa necesariamente que estas células son responsables de la regresión del tumor. Evidencia adicional es proporcionado por el aumento del riesgo de linfomas (de etiología viral y no viral) y algunos tumores sólidos en pacientes inmunosuprimidos ( Swann y Smyth, 2007 ).
Sin embargo, en la gran mayoría de tumores establecidos la presencia de linfocitos infiltrantes de tumor es insuficiente para restringir el crecimiento tumoral. Tales consideraciones han dado lugar a una versión revisada de la teoría de la vigilancia inmunológica llamada inmunoedición ( Dunn et al., 2004 ; . Smyth et al, 2006 ). Según este concepto, las células cancerosas editar constantemente y modulan la anti-tumor respuesta inmune del huésped y el anfitrión respuesta inmune da forma a la inmunogenicidad del tumor y la selección clonal. Durante este proceso el equilibrio entre anti-tumor y la inmunidad promotor de tumores se puede inclinar en favor del crecimiento tumoral. Antes de que un tumor se somete a escape inmune, que puede mantenerse a un “equilibrio” entre el crecimiento tumoral y la destrucción inmune, y esto puede dar cuenta de décadas de latencia del tumor ( Koebel et al., 2007 ). Para inclinar el equilibrio en su favor, se propone que la célula de cáncer edita su repertorio de antígenos tumorales hacia inmunogenicidad más baja y también re-moldea el microambiente tumoral para convertirse inmunosupresor. Consistente con esta hipótesis, los cánceres que se han desarrollado en ratones alymphocytic son más inmunogénicos que los tipos de cáncer cultivadas en ratones inmunocompetentes ( Shankaran et al., 2001 ).
Ir:
La terapia induce la inflamación – amigo o enemigo?
La cirugía, la quimioterapia y la radiación son actualmente las principales opciones para el tratamiento del cáncer. Los tres inducir inflamación local o sistémica provocada por la lesión tisular y la muerte de las células cancerosas. Resultados de la cirugía en la activación de vías de estrés de detección infectionor, mientras que las células de cáncer de kill quimio y radioterapia principalmente a través de necrosis, una forma pro-inflamatoria de la muerte celular ( Vakkila y Lotze, 2004 ). Los mediadores inflamatorios liberados por las células necróticas incluyen patrones de peligro asociado moleculares (amortigua), tales como ATP, ácidos nucleicos, proteínas de choque térmico (Hsp70), HMGB-1, proteínas de unión S100 calcio, y la citoquina IL-1α. Una cuestión clave es si la inflamación inducida por la terapia estimula el nuevo crecimiento de células malignas residuales o si mejora el resultado terapéutico? ( Figura 4B ). En apoyo de la primera posibilidad, la inhibición de la autofagia en tumores apoptosis deficiente estimula el crecimiento del tumor a través de la inducción de la necrosis y la inflamación estéril asociado a tumor ( Degenhardt et al., 2006 ). El crecimiento del tumor también puede ser estimulada en respuesta a la necrosis inducida por hipoxia en el núcleo del tumor ( Figura 4B ). También se ha encontrado que la muerte inducida por la castración de cáncer de próstata dependiente de andrógenos, a pesar de que resulta en regresión del tumor inicial, desencadena una respuesta inflamatoria que acelera la re-crecimiento de cáncer resistente a la castración ( Ammirante et al., 2010 ). Por lo tanto, la inhibición de la inflamación inducida por el tratamiento puede mejorar el tratamiento de cáncer de próstata y proporcionar al paciente con varios años más de supervivencia libre de tumor.
Sin embargo, en el caso de más quimioterapia convencional, la inflamación inducida por el tratamiento ha sido encontrado para estimular la presentación de antígenos por el tumor infiltración de células dendríticas y para inducir la producción de citoquinas que estimulan la inmunidad anti-tumor de adaptación ( Apetoh et al, 2007a. ; Zhang et al ., 2007 ) ( Figura 4B ). Curiosamente, el gatillo inflamatoria para esta respuesta beneficiosa es también la muerte necrótica de las células cancerosas, lo que resulta en la liberación de HMG-B1 y ATP, que junto activar TLR4 y la inflamasoma para estimular la producción de IL-1β, que es fundamental para la lucha contra adaptativa inmunidad -tumor ( Ghiringhelli et al., 2009 ). Curiosamente, los polimorfismos genéticos en el TLR4 y P2X7 (el receptor de ATP) loci afectan el resultado de la quimioterapia ( Apetoh et al, 2007a. ; Apetoh et al, 2007b. ). Lo que hace de necrosis tumoral o bien inmunoestimulante o inmunosupresor ( Vakkila y Lotze, 2004 ) aún no está claro. Además, la inmunidad anti-tumor inducida por el tratamiento sólo se ve con ciertas drogas, incluyendo el etopósido, oxaliplatino, y doxorubicina, pero no con otros ( Apetoh et al, 2007a. ; Ghiringhelli et al., 2009 ). Como estos fármacos también pueden matar a la infiltración de células madre inmunes y hematopoyéticas, que son necesarias para una respuesta inmune funcional, eficaz inmunidad antitumoral inducida por la terapia requiere el uso de pequeñas dosis de quimioterapia para evitar la inmunosupresión. A la inversa, haciendo que la muerte de tumor promoción de las células inmunes / inflamatorias, quimio y radioterapia puede usarse para destruir el microambiente inflamatorio promotor de tumores.
Ir:
Los fármacos anti-inflamatorios en la terapia del cáncer
Los hallazgos descritos anteriormente proporcionan una mejor comprensión de la etiología molecular de cáncer y sentar las bases para el uso de medicamentos anti-inflamatorios en la prevención y terapia del cáncer. Una ventaja de la orientación del microambiente inflamatorio es que el genoma normal de las células inflamatorias / inmunes, que a diferencia del genoma de la célula de cáncer, no está sujeto a cambios mutacionales y epigenéticos que resultan en resistencia a los medicamentos. Sin embargo, en la mayoría de los casos, la terapia anti-inflamatoria no es citocida por sí mismo y necesita combinarse con terapias más convencionales que matan a las células cancerosas.
A pesar de estas limitaciones, se han encontrado varios fármacos anti-inflamatorios para reducir la incidencia de tumores cuando se utiliza como profilaxis, así como ralentizar la progresión y la reducción de la mortalidad cuando se utiliza como agentes terapéuticos, particularmente en el caso de cáncer de colon esporádico ( Gupta y Dubois, 2001 ) . Tales medicamentos incluyen inhibidores de COX2, aspirina, y esteroides anti-inflamatorios, tales como dexametasona. Además de sus efectos preventivos bien documentadas en el cáncer de colon, la aspirina reduce la incidencia de cáncer de mama ( Gierach et al., 2008 ) y reduce el riesgo de cáncer de próstata, pero sólo en los individuos que llevan un alelo polimórfico particular, en la linfotoxina α locus, que especifica la producción de alta linfotoxina ( Liu et al., 2006 ). Tales hallazgos son de importancia general porque las drogas no esteroides anti-inflamatorios (NSAID), tales como aspirina, no son muy específicos y suelen tener efectos secundarios que impiden su administración a largo plazo, excepto en individuos de alto riesgo. Por lo tanto, antes de la detección de individuos con alto riesgo de cáncer que tienen más probabilidades de beneficiarse de este tipo de estrategias preventivas deben mejorar en gran medida la eficacia y la utilidad de la prevención del cáncer.
La promoción del tumor por la inflamación puede ser dirigida de varias maneras diferentes: 1) la inhibición de transductores de señales y factores de transcripción que median la supervivencia y el crecimiento de células malignas en respuesta a citoquinas inflamatorias; 2) el secuestro de las quimioquinas y citoquinas que reclutan y sostienen las células inflamatorias en el microambiente tumoral; 3) reducir (o aumentar) la inflamación que sigue a la terapia anti-cáncer; 4) el agotamiento de las células inmunes e inflamatorias que promueven el desarrollo y progresión del tumor, mientras que ahorra tipos de células y las funciones efectoras que apoyan respuestas inmunes protectoras; 5) la inhibición selectiva de citoquinas promotores de tumores sin un efecto sobre la expresión de citocinas anti-tumorigénicos.
En unos pocos casos, una terapia de orientación inflamación puede ser eficaz como agente único. Por ejemplo, constitutiva de NF-? B o STAT3 activación en ciertos tumores linfoides sugiere que los inhibidores de estos factores de transcripción se pueden utilizar como agentes citocidas en dichos cánceres. Sin embargo en la mayoría de los casos es probable que sea eficaz únicamente en combinación con enfoques más convencionales tal terapia. Además, como terapias genotóxicos a menudo conducen a la activación de NF-kB en las células malignas restante, tiene sentido para combinar fármacos genotóxicos con inhibidores de NF-? B como una manera de superar la resistencia de drogas. Sin embargo, la inhibición prolongada de NF-? B puede resultar en una deficiencia inmune grave y puede incluso conducir a la neutrofilia y mucho mayor inflamación aguda debido a una mayor secreción de IL-1β ( Greten et al., 2007 ). Tales complicaciones así como una mayor propensión a daños en el hígado han obstaculizado el desarrollo clínico de los inhibidores de NF-KB y IKK. Otro objetivo atractivo es el factor de transcripción STAT3 y la vía de señalización que conduce a su activación ( Kortylewski et al., 2005 ; . Yu et al, 2009 ). Varios inhibidores de STAT3 y JAK2 se han descrito y demostrado que inhibe el crecimiento de varios tipos de cáncer que muestran la activación de STAT3 ( Hedvat et al., 2009 ; Lin et al., 2009 ). Hasta el momento, ninguna de las complicaciones asociadas con la inhibición de NF-kB se han reportado para los inhibidores de JAK2 o STAT3.
Incluso menos complicaciones debería esperarse de fármacos que inhiben la unión de citocinas o quimiocinas pro-tumorigénicos receptor. Varios fármacos anti-citoquinas están ya en uso para el tratamiento de enfermedades inflamatorias crónicas o están bajo desarrollo clínico para tal uso. Aunque los inhibidores de citoquinas solas son poco probable que cause la muerte celular del cáncer, I / II de ensayos clínicos de fase varios evalúan actualmente la eficacia de los fármacos anti-TNF-alfa como agentes individuales en varios tipos de cáncer (anti-IL-6 y Balkwill, 2009 ). Los efectos obtenidos hasta ahora incluyen estabilización de la enfermedad y respuestas parciales, pero por-y-grande los efectos terapéuticos son modestos y ponen de relieve la necesidad de evaluar estos fármacos en combinación con la terapia convencional. Los fármacos anti-quimioquinas también están siendo evaluados, incluyendo antagonistas de los receptores y anticuerpos de bloqueo, destinados a CCR2, CCR4, y CXCR4 ( Balkwill, 2009 ). IL-1 inhibición en el mieloma múltiple ralentiza el crecimiento tumoral y conduce a un estado de enfermedad crónica, evitando de este modo la progresión a mieloma activo ( Lust et al., 2009 ).
Metástasis presenta otra aplicación importante y un reto para los fármacos que se dirigen a la inflamación asociada al tumor. Recientemente, un anticuerpo anti-RANKL, que fue desarrollado para el tratamiento de osteoporosis, se ha encontrado eficaz en la inhibición de la metástasis ósea en el cáncer de próstata ( Hurst et al., 2009 ). Otros experimentos realizados en ratones han demostrado que la inhibición de NF-? B en células de cáncer metastásico o neutralización de TNF-α puede convertir inflamación promovió el crecimiento metastásico a la regresión del tumor inducida por inflamación, depende de la expresión de TRAIL IFN-inducida ( Luo et al., 2004 ) . Tales resultados ilustran cómo la manipulación de la expresión de citoquinas puede ser usado para convertir la inflamación de tumores y la metástasis de promoción a una fuerte respuesta anti-tumor.
Ir:
Cuadro de texto: inflamación y el cáncer-hechos básicos
1. La inflamación crónica aumenta el riesgo de cáncer.
2. Subclínica, a menudo no detectable, la inflamación puede ser tan importante en el aumento del riesgo de cáncer (por ejemplo, la inflamación inducida por la obesidad).
3. Varios tipos de células inmunes e inflamatorias están presentes frecuentemente dentro de los tumores.
4. Las células inmunes afectan a las células malignas a través de la producción de citocinas, quimiocinas, factores de crecimiento, prostaglandinas y especies reactivas de oxígeno y nitrógeno.
5. impactos inflamación cada paso de la tumorigénesis, desde la iniciación a través de la promoción de tumores, todo el camino hasta la progresión metastásica.
6. En los tumores en desarrollo mecanismos inmunes e inflamatorias anti-tumorigénicos y pro-tumorigénicos coexisten, pero si no se rechaza el tumor, el efecto pro-tumorigénico domina.
7. Vías de señalización que median los efectos pro-tumorigénicas de la inflamación son a menudo objeto de un bucle de alimentación hacia adelante (por ejemplo, la activación de NF-kB en las células inmunes induce la producción de citoquinas que activan NF-KB en células de cáncer para inducir quimiocinas que atraen a más células inflamatorias en el tumor).
8. Ciertos componentes inmunes e inflamatorias pueden ser prescindible durante una etapa de la tumorigénesis pero absolutamente crítico en otra etapa.
Esta trabajo esta inspirado en el articulo de:
Immunity, Inflammation, and Cancer
Sergei I. Grivennikov,1 Florian R. Greten,2 and Michael Karin1, * 1Laboratory of Gene Regulation and Signal Transduction, Departments of Pharmacology and Pathology, School of Medicine, University of California, San Diego, 9500 Gilman Drive, La Jolla, CA, 92093, USA 22nd Department of Medicine, Klinikum rechts der Isar, Technical University Munich, 81675 Munich, Germany *Correspondence: karinoffice@ucsd.edu DOI 10.1016/j.cell.2010.01.025 Inflammatory responses play decisi