ANTICUERPOS BIESPECÍFICOS,
Los anticuerpos monoclonales son proteínas del sistema inmunitario que se crean en el laboratorio. Los anticuerpos son producidos naturalmente por el cuerpo y ayudan al sistema inmunitario a reconocer a los gérmenes que causan enfermedades, como las bacterias y los virus, y los marcan para ser destruidos.
El desarrollo de anticuerpos monoclonales de cada cliente es altamente personalizado. Los protocolos de inmunización, las condiciones de detección y los sustratos de detección adicionales son ejemplos de esto. 
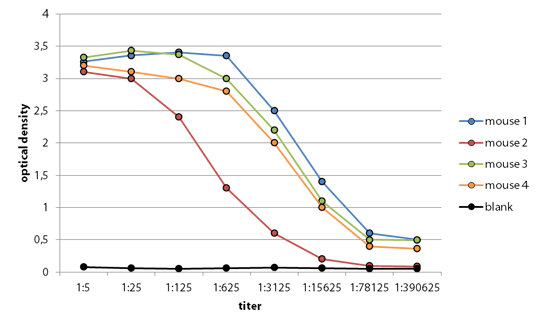
El hibridoma se realiza con la producción de anticuerpos monoclonales utilizando ratones o ratas, así como cualquier antígeno. Se aplican cuatro concentraciones diferentes de antígenos para las vacunas para lograr el mejor efecto. Esto garantiza que el sistema inmunológico responda de manera óptima. Para la fusión, se utilizará el bazo del ratón con el título más alto.  Anticuerpo monoclonal contra Coronavirus.
Anticuerpo monoclonal contra Coronavirus.
Desarrollo de anticuerpos
Davids utilizó con éxito muchos antígenos para desarrollar anticuerpos monoclonales. Las proteínas y péptidos suministrados por el cliente que representan epítopos proteicos son los antígenos más frecuentes para la generación de anticuerpos monoclonales.
PASO 1: Inmunización 2 – 4 meses
 Desde que se aprobó rituximab, muchos otros se han incorporado a los tratamientos oncológicos (medicamentos como bevacizumab, trastuzumab y cetuximab, por citar algunos). Más recientemente, se han sumado a esta familia de ‘mAbs’ (del inglés monoclonal antibody), moléculas dirigidas a los puntos de control (los inhibidores de checkpoints pembrolizumab y nivolumab, sin ir más lejos) que frenan la respuesta del sistema inmunitario ante la célula tumoral, inaugurando una nueva era en la inmunoterapia contra el cáncer.
Desde que se aprobó rituximab, muchos otros se han incorporado a los tratamientos oncológicos (medicamentos como bevacizumab, trastuzumab y cetuximab, por citar algunos). Más recientemente, se han sumado a esta familia de ‘mAbs’ (del inglés monoclonal antibody), moléculas dirigidas a los puntos de control (los inhibidores de checkpoints pembrolizumab y nivolumab, sin ir más lejos) que frenan la respuesta del sistema inmunitario ante la célula tumoral, inaugurando una nueva era en la inmunoterapia contra el cáncer. 
Anticuerpos monoclonales biespecíficos: desarrollo, producción y uso como terapia anticancerígena
Este tipo de fármacos capaz de actuar en dos dianas celulares a la vez está obteniendo resultados esperanzadores en ensayos clínicos de linfomas y mieloma.
Es la penúltima letra del alfabeto; también la forma que tiene el penúltimo cartucho contra el cáncer. Los anticuerpos biespecíficos son una evolución de los anticuerpos monoclonales, fármacos que a su vez se inspiran en los anticuerpos secretados por las células B del sistema inmune. Estas proteínas con forma de ‘Y’ flotan por el organismo en busca del antígeno para el que están destinados, ya sea una molécula en la superficie de una bacteria, un receptor en un virus o una célula tumoral.
En los anticuerpos monoclonales los dos brazos de la ‘Y’ se acoplan a un solo tipo de antígeno, pero los avances biotecnológicos han conseguido un nuevo tipo de anticuerpo, el biespecífico o bifuncional, con el que reconocer y unirse a dos antígenos a la vez, ya sea de dos células diferentes o en la misma célula.
The New England Journal of Medicine (NEJM) dedica un artículo para explicar las peculiaridades de los anticuerpos biespecíficos. Aquí se exponía la existencia de dos grandes tipos: por un lado están los también conocidos por el acrónimo inglés BiTE (bifunctional T-cell engagers o captador funcional de célula T), que con un brazo se unen a un antígeno asociado a tumor y con el otro captan un receptor específico de las células T (como CD3), de forma que atraen la célula inmunitaria hasta la célula tumoral para propiciar la destrucción del cáncer. El BiTE blinatumomab, aprobado por la agencia reguladora estadounidense FDA en leucemia linfoblástica aguda, se dirige al receptor CD3 del linfocito T y al antígeno CD19 presente en las células B malignas.
Otro gran grupo de anticuerpos biespecíficos dirige sus dos brazos a dos dianas en la misma célula tumoral (es el caso de amivantamab que se acopla a EGFR y a la oncoproteína c-MET en el cáncer de pulmón no microcítico).
Si bien el anticuerpo biespecífico blinatumomab ha recibido la aprobación de la FDA, otros fármacos similares en el campo del cáncer, especialmente en enfermedad hematológica maligna, todavía están avanzando en su desarrollo clínico. Muestra de ello ha sido la última reunión de la Sociedad Americana de Hematología (ASH), donde se comunicaron resultados con estos tratamientos.
En linfoma difuso agresivo
Un estudio en fase II que reclutó a 154 pacientes con linfoma B difuso de célula grande (LBDCG) refractario o en recaída mostró que el 39% de los pacientes tratados con el anticuerpo biespecífico glofitamab alcanzaban respuesta completa, mantenida en la mayoría de ellos al menos doce meses.
Los datos de ese estudio multicéntrico internacional fueron presentados por el autor principal, Martin Hutchings, oncohematólogo en el Rigshospitalet, en Compenhague, V coincidiendo con su publicación en NEJM.
Entre los investigadores del trabajo se encontraban Anna Sureda del Instituto Catalán de Oncología en L’Hospitalet, y Gloria Iacoboni, del Hospital Universitari Vall d’Hebron, ambos centros de Barcelona.
La hematóloga del Vall d’Hebron Gloria Iacoboni destaca a DM algunas de las conclusiones que pueden extraerse del estudio: “Más de un tercio de los pacientes tratados con glofitamab registraron respuesta completa. El 73% del grupo que lo recibió contaba con un año de seguimiento al menos, estaban ya sin tratamiento activo y la recaída parece infrecuente en los que alcanzaron remisión completa. Además, el ensayo permitió en pacientes que progresaron que se retrataran con el mismo anticuerpo biespecífico y consiguieron entonces una remisión completa.
El perfil de toxicidad también resultó aceptable. “El efecto secundario más frecuente fue el síndrome de liberación de citocinas, en la mayoría de casos en un grado bajo”, comenta. Los efectos secundarios de grado 3 ó 4 se registraron en más de la mitad de los pacientes, y la neutropenia fue el más habitual de todos.
Para mitigar los eventuales efectos secundarios, como la mencionada tormenta de citocinas, se puede recurrir a una dosis de escalada o ascendente con la que se busca habituar el organismo al fármaco; al llegar a la dosis plena, el tratamiento consistía en 12 ciclos (cada 21 días).
Glofitamab tiene una estructura única al ser un anticuerpo biespecífico bivalente, puesto que actúa en dos dominios del antígeno tumoral CD20 de la célula B y a la vez es monovalente para la proteína CD3 del linfocito T. Eso lo diferencia, entre otros, de mosunetuzumab o epcoritamab, ambos biespecíficos para CD20 y CD3. Todavía es pronto para saber si la bivalencia es un punto fuerte, “con ella se busca una mayor eficacia, pero podría conllevar también más toxicidad. De momento, lo que se ha reportado es favorable, pero, de nuevo, falta tiempo de seguimiento para poder asegurarlo”, matiza Gloria Iacoboni.
En mieloma múltiple
Durante la reunión de la ASH se hicieron públicos resultados de un estudio en fase I, que también se publicó en NEJM, con el anticuerpo biespecífico talquetamab en pacientes con mieloma múltiple altamente pretratados. El fármaco actúa promoviendo la acción de los linfocitos T CD3 positivos para que destruyan a las células del mieloma múltiple a través de la diana GPRC5D, presente en este cáncer hematológico.
Paula Rodríguez, especialista en Hematología y Hemoterapia y coordinadora médica de la Unidad Central de Ensayos Clínicos de la Clínica Universidad de Navarra (CUN), expone a DM que “talquetamab es capaz de inducir una tasa de respuestas globales elevadas, con respuestas profundas, incluyendo respuestas completas y con enfermedad mínima residual negativa, que tienden a profundizarse con el tiempo, son rápidas (mediana de tiempo hasta la primera respuesta de un mes) y son duraderas con una mediana de duración de la respuesta de 10,2 meses para la dosis de 400 y de 7,8 meses para la dosis de 800, aunque el seguimiento de esa última dosis es corto”.
Talquetamab es un anticuerpo biespecifico dirigido frente al antígeno GPRC5D “que se expresa de forma preferencial en la superficie de células plasmáticas y en tejidos derivados de los queratinocitos como piel, uñas y anejos, y papilas de la lengua y glándulas salivares menores. La expresión en pacientes con mieloma múltiple es alta, lo que hace de este antígeno una buena diana para el desarrollo farmacológico en esta enfermedad”, afirma.
No se puede pasar por alto que estos estudios, tanto en linfoma como en mieloma múltiple, se llevan a cabo en un nicho de pacientes, en recaída o refractarios tras las primeras líneas terapéuticas, donde se sitúa hoy la terapia con células CAR-T.
“Los anticuerpos biespecíficos son una nueva alternativa  terapéutica que tiene un mecanismo de acción similar a la terapia CAR T en el sentido en que redirige el linfocito T contra la célula tumoral”, indica la hematóloga de la CUN. “La ventaja principal es que no requiere ningún proceso de producción, lo que hace que sea una terapia que está disponible inmediatamente y se pueda emplear en pacientes que no pueden esperar a la terapia CAR T. Esos resultados demuestran que el tratamiento es una nueva alternativa eficaz y segura en pacientes que han agotado los tratamientos disponibles. Hay varios estudios randomizados en marcha buscando confirmar estos resultados en otras poblaciones de pacientes con enfermedad menos avanzada”.
terapéutica que tiene un mecanismo de acción similar a la terapia CAR T en el sentido en que redirige el linfocito T contra la célula tumoral”, indica la hematóloga de la CUN. “La ventaja principal es que no requiere ningún proceso de producción, lo que hace que sea una terapia que está disponible inmediatamente y se pueda emplear en pacientes que no pueden esperar a la terapia CAR T. Esos resultados demuestran que el tratamiento es una nueva alternativa eficaz y segura en pacientes que han agotado los tratamientos disponibles. Hay varios estudios randomizados en marcha buscando confirmar estos resultados en otras poblaciones de pacientes con enfermedad menos avanzada”.
Gloria Iacoboni añade que “uno de los grandes interrogantes al comparar a los anticuerpos biespecíficos -que aún no están aprobados- con las CAR-T es si las respuestas serán igualmente duraderas. Con las células CAR-T tenemos ya datos incluso de cinco años de seguimiento en algunos productos, y se ha confirmado el plateau, con respuestas duraderas en el 30-40% de los pacientes infundidos. La experiencia nos dice que cuando los linfomas agresivos no recaen en los primeros dos a cinco años es raro que lo hagan más adelante. Con los anticuerpos biespecíficos, de momento, hay poco seguimiento; es lo que se está investigando”.
Una opción de rescate tras CAR-T
En el estudio con glofitamab, un 35% de los pacientes incluidos habían recibido terapia CAR-T: “No hubo diferencias significativas en cuanto a la tasa de remisiones completas con respecto a los pacientes que no fueron tratados con CAR-T”, apunta la hematóloga del Vall d’Hebron, quien recuerda que de hecho en su centro los anticuerpos biespecíficos constituyen “una de las principales opciones de rescate en pacientes que tras recibir la terapia CAR-T progresan (alrededor del 60%)”.
Esta especialista reflexiona que “si los resultados que se están obteniendo se mantienen en fases de ensayo más avanzadas y culminan con una aprobación, es de esperar que se sumen como otra opción a la terapia CAR-T”. El hecho de que la administración de los biespecíficos pueda ser inmediata -sin esperar a las semanas de preparación requerida por las CAR-T- es una cualidad importante en pacientes que tienen el tiempo en su contra.
No obstante, “también hay que tener en cuenta que el uso de las CAR-T se va a adelantar. Axi-cel ya está aprobado por la EMA en segunda línea para pacientes refractarios o en recaída precoz en los primeros 12 meses desde la primera línea, y en Estados Unidos ya están poniendo en marcha esa estrategia. En definitiva, no creo que un tratamiento acabe desbancando a otro. Lo positivo es contar con más opciones para los pacientes y valorar cuál es la mejor en cada uno de ellos”.
Mutaciones en el ‘guardián del genoma’, nuevo factor de riesgo de patología aterosclerótica
Las mutaciones adquiridas en el oncosupresor p53 se convierten en un elemento independiente que puede jugar, en el futuro, un papel diagnóstico y preventivo.
Combinando experimentos en modelos murinos de aterosclerosis y análisis de más de 50.000 secuencias de ADN humano, un equipo del Centro Nacional de Investigaciones Cardiovasculares (CNIC), en colaboración con instituciones estadounidenses, demuestra el papel de las mutaciones adquiridas en el gen p53 en el desarrollo de la enfermedad cardiovascular aterosclerótica, según publican en Nature Cardiovascular Research.
En este trabajo, «demostramos que la presencia en células sanguíneas de mutaciones adquiridas en el oncosupresor p53 no sólo aumenta el riesgo de neoplasias hematológicas, sino que también aumenta el riesgo de desarrollar enfermedad cardiovascular aterosclerótica, tanto a nivel coronario como a nivel de arterias periféricas. Estos resultados aumentan nuestro conocimiento de la hematopoyesis clonal, un fenómeno inducido por mutaciones adquiridas en células sanguíneas, como un nuevo factor de riesgo cardiovascular, completamente independiente de los factores de riesgo tradicionales», señala a DM, José Javier Fuster, investigador del CNIC, y uno de los autores de la nueva investigación.
Conocida como el ‘guardián del genoma’, la proteína codificada por el gen p53 contribuye a mantener la integridad del material hereditario de las células, regulando múltiples funciones celulares en respuesta a diferentes formas de estrés.
Factor independiente
Se sabe que la presencia de mutaciones adquiridas en el gen p53 en las células sanguíneas aumenta el riesgo de desarrollar distintos tipos de cáncer, incluyendo cánceres sanguíneos. Pero, lo novedoso es que en el nuevo trabajo se demuestra que dichas mutaciones aceleran también el desarrollo de la aterosclerosis, la causa subyacente a la mayor parte de las enfermedades cardiovasculares, la primera causa de mortalidad en el mundo y uno de las mayores cargas económicas para los sistemas sanitarios.
En colaboración con los grupos de Derek Klarin, de la Universidad de Stanford; Pradeep Natarajan, del Hospital General de Massachusetts, y Alexander Bick, de la Universidad de Vanderbilt, los investigadores analizaron datos de secuenciación de células sanguíneas de más de 50.000 personas, concluyendo que los portadores de mutaciones adquiridas en p53 presentan un mayor riesgo de desarrollar enfermedad coronaria y enfermedad arterial periférica, de forma completamente independiente de los factores de riesgo cardiovascular tradicionales, como la hipertensión o los niveles elevados de colesterol en sangre.
Los investigadores del CNIC realizaron estudios funcionales en modelos animales de aterosclerosis en los que se introdujeron células mutantes en p53. Los resultados mostraron que los ratones portadores de dichas mutaciones desarrollaron aterosclerosis de forma acelerada, debido principalmente a una proliferación anormalmente elevada de células inmunes en la pared de las arterias.
Estudios anteriores de este mismo grupo ya habían demostrado en un artículo publicado en 2021 en The Journal of the American College of Cardiology (JACC) que varias de estas mutaciones, por ejemplo las que afectan al gen TET2, contribuyen al desarrollo de enfermedades cardiovasculares, como la aterosclerosis o la insuficiencia cardiaca.
Aplicaciones clínicas
Sobre qué potenciales aplicaciones pueden beneficiar a los pacientes, mayoritariamente de edad avanzada, José Javier Fuster, señala que a medio plazo, detectar mutaciones adquiridas en p53 o en otros genes ligados a hematopoyesis clonal podría contribuir a la identificación de pacientes de alto riesgo, tanto en lo relativo a enfermedad cardiovascular como a neoplasias hematológicas.
«Los portadores de estas mutaciones podrían beneficiarse de un seguimiento más exhaustivo de su estado de salud. La asociación entre estas mutaciones y el desarrollo de enfermedad cardiovascular es independiente de los factores de riesgo tradicionales, por lo que sería un abordaje complementario al basado en la determinación de niveles de colesterol, presión arterial».
Este concepto, indica el investigador, está siendo ya aplicado en algunos hospitales en Estados Unidos, que han establecido unidades de hematopoyesis clonal para el seguimiento y el asesoramiento de pacientes que se identifican como portadores de estas mutaciones.
A más largo plazo, identificar estas mutaciones «nos ayudará a diseñar estrategias personalizadas de prevención de riesgo cardiovascular, dirigidas a prevenir los efectos específicos de estas mutaciones. Sin embargo, esto requerirá todavía años de investigación y nuevos ensayos clínicos», explica José Javier Fuster.
Los investigadores destacan que los mecanismos por los que mutaciones en diferentes genes contribuyen a la enfermedad cardiovascular son diferentes, «lo que puede en el futuro abrir la puerta a estrategias personalizadas de prevención de la enfermedad cardiovascular dirigidas a los efectos específicos de las distintas mutaciones», indica Nuria Matesanz, investigadora del CNIC y coprimera autora del artículo.
Biografía
El autor principal del trabajo es Ajai Chari, del Instituto del Cáncer Tisch del Hospital Mount Sinai, en Nueva York. Entre los investigadores del estudio estaban Alberto Oriol, del Instituto Catalán de Oncología (ICO) en Badalona (Barcelona); Paula RodríguezOtero, de la Clínica Universidad de Navarra, en Pamplona; Elham Askari, del Hospital Universitario Fundación Jiménez Díaz, en Madrid, y María Victoria Mateos, del Hospital Universitario de Salamanca.
Valentín Fuster y Andrés Hidalgo. En los últimos 10 años, la investigación dedicada a los anticuerpos biespecíficos ha aumentado significativamente.
Sonia Moreno. Madrid Anna Sureda del Instituto Catalán de Oncología en L’Hospitalet, y Gloria Iacoboni, del Hospital Universitari Vall d’Hebron, ambos centros de Barcelona.
Lun, 16/01/2023 – 09:21
José Javier Fuster, Marta Amorós Pérez, Nuria Matesanz, María Ángeles Zuriaga y Alejandra Aroca Crevillén. Foto: CNIC
Raquel Serrano. Madrid Lun, 16/01/2023 – 17:28