 Modular los receptores de membrana
Modular los receptores de membrana
La complejidad del tema y su desconocimiento por la mayoría de los profesionales de la medicina practica, me llevan a comentar, con una introduccion al tema, «De Molecular Cell. Mario Mellado, director del trabajo e investigador del CNB-CSIC».
Impedir la agregación de los receptores de membrana podría utilizarse como base para nuevas estrategias terapéuticas contra procesos como la metástasis tumoral, enfermedades autoinmunes o el VIH.
Los receptores de membranas son las proteínas o glicoproteínas que permiten la interacción de determinadas sustancias con los mecanismos del metabolismo celular. Están presentes en varios lugares, la membrana plasmática, las membranas de los orgánulos, en el citosol celular o en el núcleo celular, a las que se unen específicamente otras sustancias químicas llamadas moléculas señalizadoras, como las hormonas y los neurotransmisores.
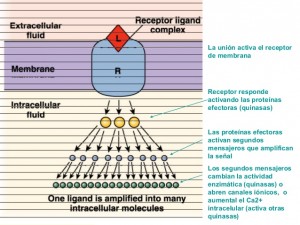
La unión de una molécula señalizadora a sus receptores específicos, desencadena una serie de reacciones en el interior de las células , se llaman transducción de señal), los estímulos recibidos sobre las dianas celulares y modulado por el ambiente , la presencia de patógenos, el estado metabólico de la célula, et
Los receptores se acoplan de forma de forma diversa a diversas proteinas, una proteína se une al receptor y genera una cascada de señales (transducción de señales) que deriva en un comportamiento biológico concreto.
Los acoplados a proteínas a proteínas G, suponen el 40% de la transducción de señales: Existen 6 subtipos de receptores acoplados a proteínas G que se distinguen por la similitud proteica, su mecanismo o su función.
Esquema de receptor transmembrana
E: espacio extracelular; I: espacio intracelular; P: membrana plasmática.
Similares a la rodopsina. Engloba un conjunto amplio de subfamilias de receptores, como la subfamilia de receptores de dopamina, esenciales para la supervivencia por su implicación primordial en el mecanismo de recompensa, o la subfamilia de receptores de histamina, que tienen implicación en el sistema inmune.
Familia de receptores de Secretina. Engloba un conjunto importante de subfamilias de receptores.
Familia de receptores metabotrópicos de Glutamato y feromonas. Engloba un conjunto de receptores basados en mensajeros secundarios y otros receptores relacionados con el gusto.
Receptores de feromonas de apareamiento por hongos.
Receptores de AMP Cíclico.
Frizzled’ / Smoothened’
Receptores basados en la apertura de un canal iónico que basan su modelo funcional en la apertura de un canal iónico de sodio (Na+), calcio (Ca2+) o cloro (Cl-). Una proteína se une a un receptor y provoca la apertura de un canal iónico por donde discurren ciertos iones, positivos o negativos, que provocan una respuesta biológica concreta.
Factor Neurotrófico Derivado de la Línea Celular Glial (GFRa).
Receptor de péptidos natriuréticos (NPR).
Receptor de neurotrofinas (TRK).
Receptor de tipo Toll.
Receptores transmembrana
Los receptores transmembrana son proteínas que se extienden por todo el espesor de la membrana plasmática de la célula, proteínas transmembranales, con un extremo del receptor fuera de la célula (dominio extracelular) y otro extremo del receptor dentro (dominio intracelular). Cuando el dominio extracelular reconoce a una hormona, la totalidad del receptor sufre un cambio en su conformación estructural que afecta al dominio intracelular, confiriéndole una nueva acción. En este caso, la hormona (u otro ligando) no atraviesa la membrana plasmática para penetrar en la célula. Aunque un receptor sencillo puede transducir alguna señal tras la unión del ligando, lo más frecuente es que la unión del ligando provoque la asociación de varias moléculas receptoras. Los principales tipos de receptores transmembrana son los siguientes:1
Receptores con actividad tirosina quinasa intrínseca.
Dentro de este grupo están los receptores de la mayor parte de los factores de crecimiento, como EGF, TGF-alfa, HGF, PDGF, VEGF, FGF, y el receptor de la insulina. Los receptores de esta familia tienen un dominio extracelular de unión al ligando, un dominio transmembrana, y un dominio intracelular con actividad tirosina quinasa intrínseca. Cuando se une el ligando, el receptor se dimeriza, lo que induce la autofosforilación de las tirosinas del dominio intracelular y activa la tirosina quinasa, que fosforila (y por tanto activa) muchas moléculas efectoras en cascada, de forma directa o mediante proteínas adaptadoras. En muchos tipos de cáncer se han detectado alteraciones en la actividad tirosina quinasa del receptor y mutaciones, por lo que estas moléculas son dianas terapéuticas muy importantes.
Receptores que carecen de actividad intrínseca y reclutan quinasas
En este grupo se incluyen los receptores de muchas citoquinas, como IL-2, IL-3, interferón α, β y γ, eritropoyetina (EPO), hormona del crecimiento y prolactina. La transmisión de la señal de estos receptores provoca la activación de miembros de la familia de quinasas denominadas JAK (Janus quinasas). Estas quinasas activan factores de transcripción citoplásmicos llamados STATs (por signal transducers and activation of transcription), que se translocan al núcleo y activan la transcripción de genes específicos. En otros casos, estos receptores activan la cascada de las MAP-quinasas.
Receptores acoplados a proteínas G
En este caso, la transducción de la señal se realiza a través de proteínas triméricas de unión a GTP (proteínas G), que constan de 7 hélices transmembrana y constituyen la mayor familia de proteínas receptoras (1% del genoma humano). Hay un gran número de ligandos que utilizan estos receptores, como las quimiokinas, vasopresina, serotonina, histamina, adrenalina, noradrenalina, calcitonina, glucagón y hormona paratiroidea, entre otros. Muchas drogas farmacéuticas comunes tienen como diana estos receptores. La unión del ligando provoca cambio de conformación y activación del receptor, que puede interaccionar con otras muchas proteínas G. La forma inactiva une GDP, mientras que la forma activa une GTP. En algunos casos, esta vía de señalización incluye AMPc como segundo mensajero.
El reconocimiento de la estructura química de una hormona por el receptor de la hormona utiliza los mismos mecanismos de enlace no covalente como los puentes de hidrógeno, fuerzas electrostáticas, fuerzas hidrófobas y de Van der Waals.
La equivalencia entre la unión hormona-receptor y la hormona libre es igual a:
[H] + [R] <-> [HR], con
[R]=receptor; [H]=hormona libre; [HR]=receptor unido a la hormona
Lo importante de la fuerza de la señal transmitida por el receptor es la concentración de complejos hormona-receptor, que es definida por la afinidad que existe entre la hormona con su receptor, por la concentración de la hormona y por la concentración del receptor. La concentración de hormona circulante es el punto principal de la fuerza de la señal, siempre que los otros dos valores sean constantes. En reacciones rápidas, la producción de hormonas por las células puede almacenarse en forma de prohormonas, y rápidamente transformarse y liberarse cuando sea necesario.
También la célula puede modificar la sensibilidad del receptor, por ejemplo por la fosforilación. También por la variación del número de receptores que pueden modificar la fuerza total de señalización en el interior de la célula.
Receptores nucleares
Los receptores nucleares o citoplasmáticos son proteínas solubles localizadas en el citoplasma o en el núcleo celular. La hormona que pasa a través de la membrana plasmática, normalmente por difusión pasiva, alcanza el receptor e inicia la cascada de señales. Los receptores nucleares son activadores de la transcripción activados por ligandos, que se transportan con el ligando u hormona, que pasan a través de la membrana nuclear al interior del núcleo celular y activan la transcripción de ciertos genes y por lo tanto la producción de una proteína.
Los ligandos típicos de los receptores nucleares son hormonas lipofílicas como las hormonas esteroideas, por ejemplo la testosterona, la progesterona y el cortisol, derivados de la vitamina A y vitamina D. Estas hormonas desempeñan una función muy importante en la regulación del metabolismo, en las funciones de muchos órganos, en el proceso de desarrollo y crecimiento de los organismos y en la diferenciación celular. La importancia de la fuerza de la señal es la concentración de hormona, que está regulada por:
Los órganos dianas reciben estimulación tanto eléctrica como química. En el caso mas típico, El hipotálamo produce factores liberadores de hormonas que actúan sobre la hipófisis y activa la producción de hormonas hipofisarias, las cuales activan los órganos endocrinos que finalmente producen las hormonas para los tejidos diana. Este sistema jerarquizado permite la amplificación de la señal original que procede del hipotálamo. La liberación de hormonas enlentece la producción de estas hormonas por medio de una inhibición reactiva (feedback), para evitar una producción aumentada.
Disponibilidad de la hormona en el citoplasma: Muchas hormonas pueden ser convertidas en formas de depósito por la célula diana para su posterior uso. Este reduce la cantidad de hormona disponible.
Modificación de las hormonas en el tejido diana: Algunas hormonas pueden ser modificadas por la célula diana, de modo que no activan el receptor hormonal y así reducen la cantidad de hormonas disponibles.
Los receptores nucleares que son activados por hormonas activan receptores específicos del ADN llamados elementos sensibles a hormonas (HREs, del inglés Hormone Responsive Elements), que son secuencias de ADN que están situados en la región promotora de los genes que son activados por el complejo hormona receptor. Como este complejo activa la transcripción de determinados genes, estas hormonas también se llaman inductores de la expresión genética. La activación de la transcripción de genes es mucho más lenta que las señales que directamente afectan a proteínas ya existentes. Como consecuencia, los efectos de hormonas que se unen a receptores nucleares se producen a largo plazo. Sin embargo la señal de transducción a través de receptores solubles afecta sólo a algunas proteínas. Los detalles de la regulación genética todavía no son del todo conocidos. Todos los receptores nucleares tienen una estructura modular similar:
Receptores esteroideos son un subtipo de receptores nucleares localizados permanentemente en el citoplasma. En ausencia de hormona esteroidea, los receptores están unidos en un complejo denominado complejo aporreceptor, que contiene proteínas chaperonas o carabina, también conocidas como proteínas de choque térmico o de calor (HSPs del inglés Heat Shock Proteins). Las HSPs son necesarias en la activación del receptor porque ayuda a cambiar su conformación que le permite unirse a la secuencia de bases del ADN.
Los receptores esteroides también pueden tener un efecto represivo sobre la expresión genética cuando el dominio de transactivación esté escondido, por lo que no se puede activar la transcripción. como resultado de otras formas de señal de transducción, por ejemplo como por un factor de crecimiento. Este comportamiento es llamado crosstalk.
RXS y receptores huérfanos. Estos receptores moleculares pueden ser activados por: hormonas que entran en el interior de la célula de diferentes maneras
Una hormona clásica que entra en la célula por difusión.
Una hormona que fue sintetizada en la célula, de un precursor o prohormona, que puede ser transportada hacia la célula a través del torrente sanguíneo, como por ejemplo retinol
Una hormona que fue completamente sintetizada en el interior de la célula, las prostaglandinas.
Estos receptores están localizados en el núcleo y no están acompañados de proteínas carabina. En ausencia de hormona, se une a su secuencia específica de ADN inactivando un gen. Cuando se activan por las hormonas, se activa la transcripción de genes que estaban reprimidos.
La complejidad del tema y el desconocimiento del tema en medicina por la mayoría de los profesionales, me llevan a copiar el articulo .
Impedir la agregación de los receptores de membrana podría utilizarse como base para nuevas estrategias terapéuticas contra procesos como la metástasis tumoral, enfermedades autoinmunes o el VIH, según publica Molecular Cell.
Mario Mellado, director del trabajo e investigador del CNB-CSIC.
Los receptores de quimiocinas son proteínas de la membrana celular clave en muchos procesos biológicos porque orientan y dirigen el movimiento de la célula. No actúan de manera individual, ni tampoco en parejas, como se pensaba hasta ahora, sino que forman agregados de hasta diez unidades para llevar a cabo su función de una manera más eficiente. Es lo que indica un estudio publicado en Molecular Cell que analiza la dinámica y la disposición de CXCR4 en la membrana celular. Los autores sugieren que impedir la agregación de estos receptores podría utilizarse como base para nuevas estrategias terapéuticas contra enfermedades en las que CXCR4 juega un papel importante como la metástasis tumoral, enfermedades autoinmunes o el Sida (CXCR4 es uno de los receptores usado por algunas cepas de VIH para infectar las células).
El trabajo, llevado a cabo por investigadores del Centro Nacional de Biotecnología del CSIC (CNB-CSIC) en colaboración con el ICFO (Instituto de Ciencias Fotónicas) de Barcelona y el CNIC (Centro Nacional de Investigaciones Cardiovasculares Carlos III) de Madrid, demuestra que la asociación de estos receptores en grupos posibilita la activación completa de la maquinaria de señalización celular necesaria para que la célula se oriente y desplace correctamente.
«Estos agregados son más activos que los receptores individuales o en pareja, asegura Mario Mellado, director del trabajo e investigador del CNB-CSIC, quien señala además que es un mecanismo que permite a la célula adaptarse muy rápidamente a cambios en el ambiente en que vive y responder de manera muy efectiva».
Lo más importante del trabajo , es que se han han identificado pequeños péptidos capaces de impedir la formación de estos agregados, bloqueando así la función celular. «Estos resultados posibilitan el desarrollo de nuevas terapias basadas en compuestos que interfieren en la formación de agregados de receptores de quimiocinas específicos. Es una estrategia que podría ser utilizada para atajar enfermedades como el cáncer, la infección por VIH o enfermedades autoinmunes», explica Mellado
Este proceso de agregación también se ve influido por la actina, una proteína que forma parte del esqueleto de la célula. Todos estos factores regulan y controlan la formación de agrupaciones de CXCR4 en la superficie celular y, como consecuencia, la activación de la maquinaria de señalización necesaria para promover una función completa en la célula. «Ya estamos comenzando a trabajar en la búsqueda de compuestos pequeños capaces de intervenir en el proceso de agregación de CXCR4, y sean prometedores candidatos para el desarrollo de nuevos tratamientos clínicos», concluye Mellado.
Referencias
Kumar, MBBS, MD, FRCPath, V.; Abul K. Abbas, MBBS, Nelson Fausto, MD and Jon Aster, MD (2009). «Ch3-Tissue Renewal, Regeneration and Repair». En Saunders (Elsevier). Robbins & Cotran Pathologic Basis of Disease (8th edición).