LA INFLAMACIÓN ATACA O DEFIENDE
Es la inflamación un sistema reparador de la infección o por el contrario es un sistema destructivo.
A medida que avanzan nuestros conocimientos, podemos ver fenómenos contradictorios, como es la repacion por inflamación o por el contrario su efecto destructivos y perpetuaste.
Según esto, habría que incluir a la arteriosclerosis dentro de la enfermedad degenerativa.
La inflamación es en sí un proceso reactivo, complejo, inespecífico, que se caracteriza por modificaciones locales y coordinadas a nivel de los vasos sanguíneos (endotelio) y el tejido conectivo subyacente. Puede alterar la homeostasis general y su función es localizar, eliminar, o al menos aislar el agente o cuerpo extraño. 
Un algoritmo de aprendizaje automático que utiliza datos genéticos de muestras de sangre de pacientes puede predecir y explicar la progresión de enfermedades neurodegenerativas como el Alzheimer y el Huntington.
La inflamación es inicialmente un proceso beneficioso con sistemas de control muy estrictos que permiten su resolución una vez cumplida su función. De ahí que se haya conservado a lo largo de la evolución como un sistema de alarma y defensa. La pregunta que cabe siempre es si la reparación del sistema inflamatorio es también lesiva
Muchos autores se han preocupado de este tema pero es el Dr. Moir muerto recientemente con un tumor cerebral el que al identificar la función biológica normal de Aβ y de los depósitos de β-amiloide insolubles que el péptido puede generar: Resulta que éste péptido antimicrobiano del sistema inmunitario innato, atrapa y mata a los patógenos que invaden el cerebro. Este nuevo descubrimiento sugiere que la EA puede ser una respuesta inapropiada a una infección real o falsamente percibida en el cerebro. Este hallazgo también puede arrojar luz sobre los mecanismos patológicos asociados con otras enfermedades principales asociadas con amiloides, como la diabetes y la arteriolosclerosis.
Hortolano en su artículo sobre síndrome de Inflamación y macrófagos si estos dos elementos procesos actúan como: amigos o enemigos.
Los datos clínicos de la inflamación se han conocido desde la antigüedad Los principales signos de la inflamación en su fase aguda son: calor (a nivel local), enrojecimiento, hinchazón y en algunos casos formación de exudaciones y finalmente presión y dolor en las terminaciones nerviosas.
No cabe duda de la función de los macrófagos en este proceso. Estas son células residentes en los tejidos, que se originan a partir de los monocitos del plasma. Recientemente se ha identificado que los macrófagos, agentes del sistema inmune de mayor relevancia nivel tisular, presentan dos fenotipos, con funciones literalmente opuestas; M1 – inflamatorio y M2 – anti inflamatorio.
Ambos fenotipos son esenciales para la homeostasis del organismo, sin embargo, un desbalance de estos fenotipos se ha identificado en condiciones patológicas como la obesidad mórbida, donde se presenta prevalencia del fenotipo M1, asociado con los niveles elevados de la citoquina llamada TNF-alfa y que es una de la moléculas responsables de promover el que estos pacientes desarrollen resistencia a insulina. Esta alteración se conoce como diabetes tipo II.
En diversas enfermedades auto-inmunes como enfermedad de Chrohn, artritis reumatoide o esclerosis múltiple, entre otras, también se encuentran asociadas a una prevalencia del fenotipo M1 .
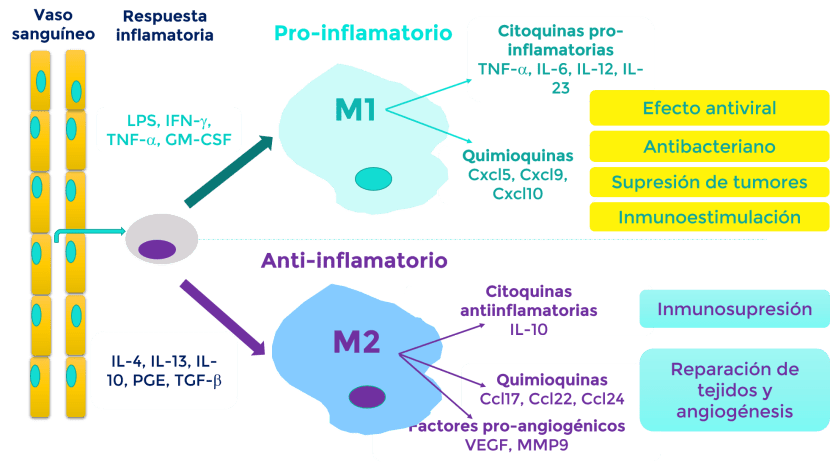
Figura 1. Fenotipos M1-inflamatorio y M2-anti-inflamatorio.
En la inflamación en su etapa aguda, justo se manifiesta cuando ocurre o se presenta la alteración o daño del tejido; las moléculas que liberan macrófagos activados en su fenotipo M1 están orientados a eliminar microbios e iniciar el proceso de reparación tisular (figura 1). Sin embargo, si esos mismos macrófagos permanecen activados por tiempos prolongados en un tejido, conservando este fenotipo M1, se les atribuye la responsabilidad de la mayor parte de los daños tisulares que se presentan en los tejidos y esa condición ya se define como inflamación crónica.
Casi dos tercios de las patologías humanas presentan alteraciones en la respuesta inflamatoria, incluyendo enfermedades como el Alzheimer, que tradicionalmente se consideraba una enfermedad degenerativa, o el cáncer, en la que el componente inflamatorio está adquiriendo cada vez mayor relevancia [1]. Incluso en la osteoporosis surgen evidencias de que esta patología también se debe posiblemente a desbalance de tipo inflamatorio, por la desregulación de los macrófagos a consecuencia de la ausencia de estrógenos, en este caso ya se acuña el término, inmunoporosis [2,3].
Estos macrófagos presentan una alta heterogeneidad y, dependiendo del microambiente que les rodee, pueden adoptar distintos estados de activación, que difieren en la expresión de receptores, funciones y producción de citoquinas y quimioquinas, lo que les permite adaptarse al medio adecuadamente.
En estas patologías cada día crecen las evidencias de la efectividad del uso de la terapia celular con células madre mesenquimales (MSCs, pos sus siglas en inglés). La terapia celular empleando MSCs o derivados de estas (medio condicionado o exosomas) demuestran un potente efecto inmunomodulador, con especial énfasis en la capacidad de estas células en promover el cambio de polarización del fenotipo M1 al M2 [4, 5].
No creo que este articulo aclare el gran problema de infección e inflamación amigos o enemigos. Pero si que están relacionados y contribuyen en la patología degenerativa
Bibliografía:
[1] Hortolano S. Inflamación y macrófagos: amigos o enemigos https://www.sebbm.es/web/images/archivos/archivos_tinymce/sonsoleshortelano_enero2014.pdf Consultado el 23/01/2020
[2] Yang, D. H., & Yang, M. Y. (2019). The Role of Macrophage in the Pathogenesis of Osteoporosis. International journal of molecular sciences, 20(9), 2093.
[3] Srivastava, R. K., Dar, H. Y., & Mishra, P. K. (2018). immunoporosis: immunology of Osteoporosis—Role of T Cells. Frontiers in immunology, 9, 657.
[4] Zhang, Q. Z., Su, W. R., Shi, S. H., Wilder‐Smith, P., Xiang, A. P., Wong, A., … & Le, A. D. (2010). Human gingiva‐derived mesenchymal stem cells elicit polarization of m2 macrophages and enhance cutaneous wound healing. Stem cells, 28(10), 1856-1868.
[5] Sicco, C. L., Reverberi, D., Balbi, C., Ulivi, V., Principi, E., Pascucci, L., … & Pozzobon, M. (2017). Mesenchymal stem cell‐derived extracellular vesicles as mediators of anti‐inflammatory effects: Endorsement of macrophage polarization. Stem cells translational medicine, 6(3), 1018-1028.