ENFERMEDAD DE ALZHEIMER SIN PLACAS AMILOIDE<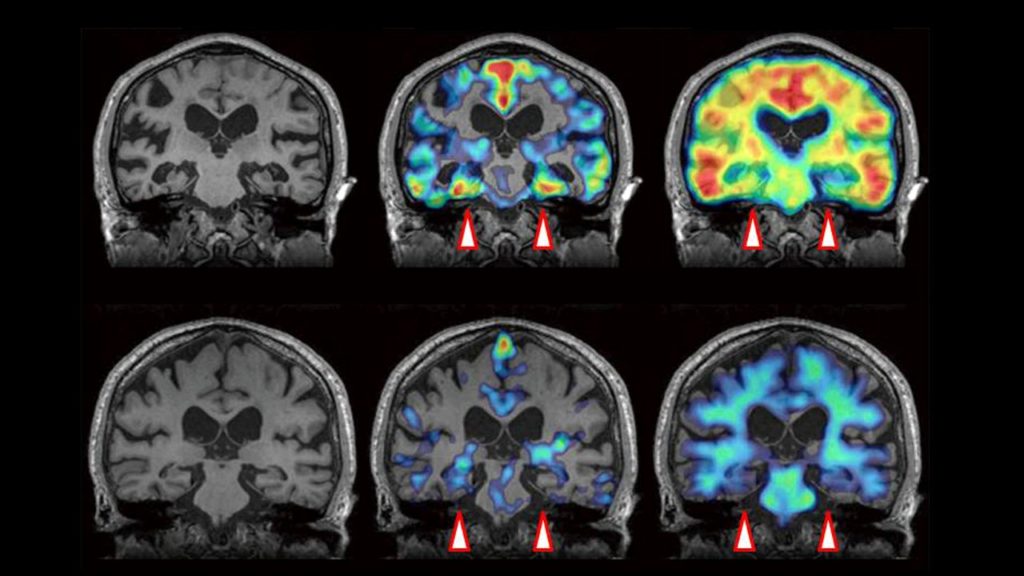
Un nuevo estudio cuestiona que los niveles anómalos de placa de amiloide en el cerebro aparezcan antes que la pérdida de memoria en la enfermedad de Alzheimer.
Una hipótesis prevalente entre la comunidad científica es que la proteína beta-amiloide constituye el primer signo de la enfermedad de Alzheimer. La acumulación anómala de esta proteína conduce, entre otras alteraciones cerebrales, a la neurodegeneración y, finalmente, a problemas de razonamiento y memoria. Pero un nuevo estudio desafía esa teoría: sugiere que los trastornos sutiles de pensamiento y memoria pueden aparecer antes o incluso junto con el desarrollo de placas beta-amiloides del cerebro. El trabajo se acaba de publicar en el último número de Neurology, la revista de la Academia Estadounidense de Neurología.
Mediante el estudio con escáner, se comprobó que “el amiloide no es necesariamente lo primero en el proceso de la enfermedad de Alzheimer”, afirma el autor del trabajo Kelsey R. Thomas, médico del Sistema de Salud de los Veteranos de San Diego. “Gran parte de la investigación que explora posibles tratamientos para la enfermedad de Alzheimer se ha centrado en destruir la placa de beta-amiloide, pero, según nuestros hallazgos, tal vez ese enfoque debe cambiar a otros objetivos”.
El estudio incluyó a 747 personas con una edad media de 72 años. Los investigadores analizaron a los participantes con pruebas neuropsicológicas y de imagen al comienzo del estudio, que cotejaron con otras realizadas durante la investigación. Sobre esos resultados los dividieron en tres grupos: 305 personas con habilidades de razonamiento y memoria normales; 153 con sutiles diferencias, y 289 personas con deterioro cognitivo leve. Las exploraciones de imagen se realizaron anualmente durante cuatro años.
Acumulación más rápida
Tras ajustar la edad, la educación, el sexo, el riesgo genético de la enfermedad de Alzheimer y el nivel de amiloide al comienzo del estudio, los investigadores descubrieron que las personas con diferencias sutiles de razonamiento y memoria tenían una acumulación más rápida de amiloide en comparación con las personas con esas capacidades normales. Al medir los niveles de amiloide, se obtuvo nivel medio de 1,16 entre los participantes con dificultades sutiles de razonamiento y memoria; ese nivel aumentó 0,03 en este grupo, pero entre los que tenían capacidades normales, lo hizo aún más. Las personas con diferencias sutiles presentaron además un adelgazamiento más rápido de la corteza entorrinal, una región del cerebro que se ve afectada muy temprano en la enfermedad de Alzheimer.
Por otro lado, si bien las personas con deterioro cognitivo leve tenían más cantidad de amiloide en sus cerebros al comienzo del estudio, no experimentaron una acumulación más rápida de amiloide en comparación con aquellos con habilidades cognitivas normales. Sin embargo, sí tuvieron un adelgazamiento más rápido de la corteza entorrinal, así como una contracción cerebral del hipocampo.
Proteína tau
“De investigaciones anteriores, sabemos que otro biomarcador de la enfermedad de Alzheimer, la proteína tau, muestra una relación constante con los síntomas cognitivos. Por lo tanto, se necesita más investigación para determinar si la tau ya está presente en el cerebro cuando empiezan a aparecer sutiles alteraciones en el pensamiento y la memoria”, destaca Thomas.
El investigador concluye que el trabajo demostró un método para detectar alteraciones cognitivas sutiles antes o durante la fase en la que la placa de amiloide se acumula a un ritmo más rápido: “Esto podría justificar la realización de exámenes no invasivos que podrían detectar muy temprano quién está en riesgo de desarrollar la enfermedad de Alzheimer”.
De este trabajo se puede deducir que la proteína beta amiloide no es fundamental para la enfermedad de Parkinson y como algunos autores han propuesto los gérmenes tendrían un lugar en esta patología
Los gérmenes llegarían primero, posiblemente como consecuencia de la ruptura de la microbiota, y se depositarían de forma plural en distintos parénquimas, desencadenando después una reacción inmunitaria de tal forma que los macrófagos tales como la beta amiloide y tau entre otras se precipitarían sobre los gérmenes.
La clínica se iniciaría por los gérmenes y el sistema inmunitario y sus proteínas agravarían el conflicto.
¿Podrían las placas y la neuroinflamación en el Alzheimer ser en realidad una respuesta inmune a un verdadero desafío inmunitario de los microbios en el cerebro?
Robert Blair y Alonso, ya hace algún tiempo descubrieron gérmenes bajo las placas beta amiloide. De distintas enfermedades neurodegenerativas
Este esquema parece sencillo pero no lo es más que el admitido hasta ahora.
El algoritmo: que se puede idealizar es como sigue
Rotura de la microbiota
Invasión de gérmenes
Lesión del parénquima,
Precipitación de macrófagos
Desarrollo y evolución de la enfermedad
Biografía una guapa
Neurology, Kelsey R. Thomas, médico del Sistema de Salud de los Veteranos de San Diego.
ELA Y HONGOS. Alonso 1 , Pisa D 1 , Fernández-Fernández AM 1 , Rábano A 2 , Carrasco L 3 .
. Robert Blair