Β-AMILOIDE Y ALZHEIMER
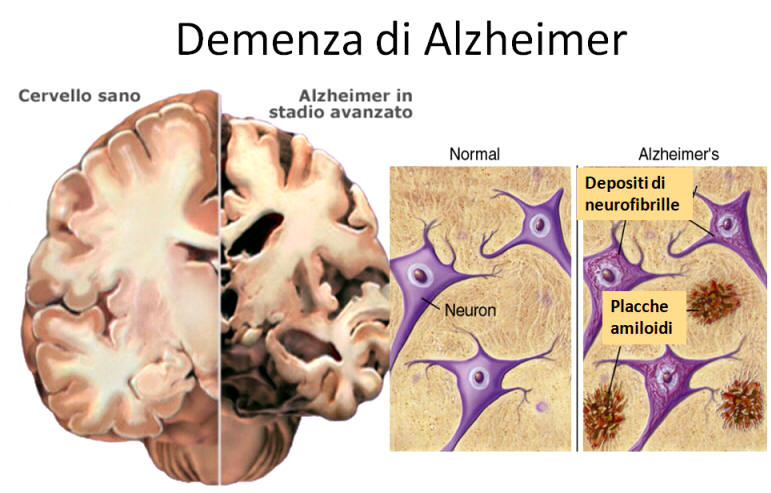
Cada vez se acepta más que la enfermedad de Alzheimer es un síndrome, más que una enfermedad unívoca, y que hay muchos factores a tener en cuenta.
Fraude sobre el alzhéimer:
Esto asusta o por lo menos sorprende, que unos sabios mientan.
Pero el problema que supone esta enfermedad y el poco remedio que tenemos hace que la avidez por una terapia eficaz se desea tanto que se falseen las conclusiones.
La revista Science ha publicado un reportaje en el que se revelan múltiples indicios de fraude en una de las publicaciones más citadas sobre el alzhéimer.
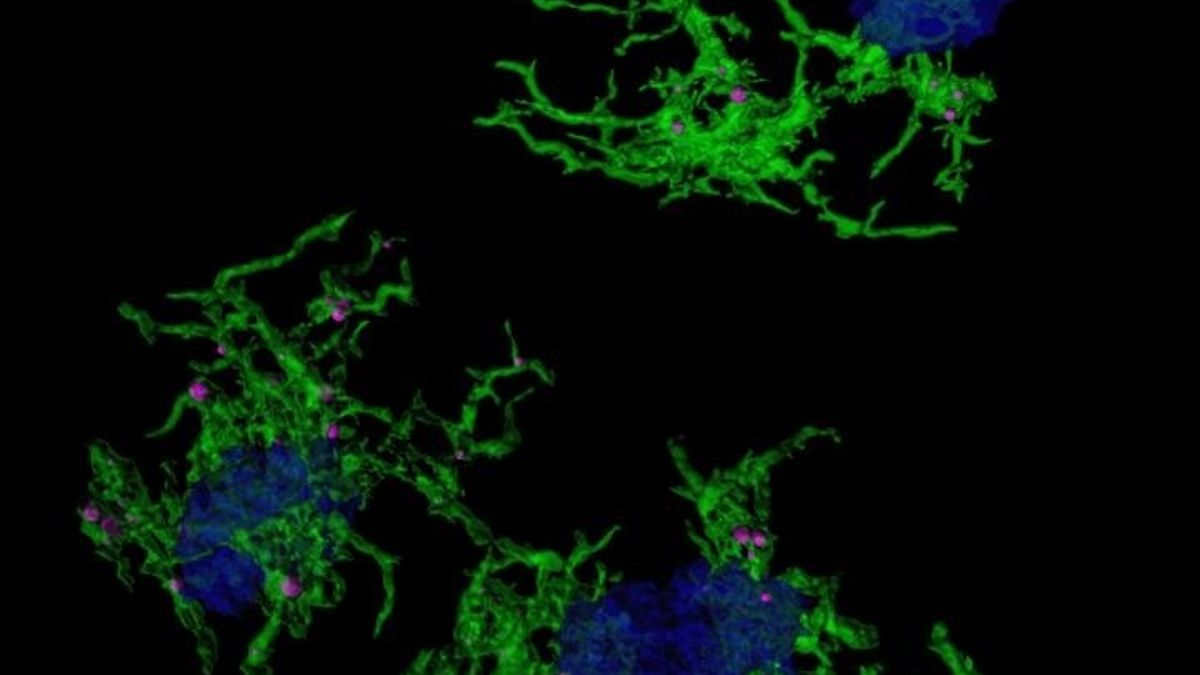 Imagen microscópica con microglia verde envuelve placas amiloide azul
Imagen microscópica con microglia verde envuelve placas amiloide azul
Cronología de algunos hallazgos en Alzheimer
Entre 1906 y 1911, Alois Alzheimer (y Oskar Fischer) empiezan a describir las placas características de los enfermos.
En 1984 se establece que la proteína β-amiloide es el principal componente de las placas.
En 1991 empieza a publicarse que varias mutaciones que aumentan la cantidad de proteína precursora del amiloide provocan indefectiblemente la enfermedad en quienes las portan. Se asume que es la causa del alzhéimer y la teoría se convierte en dominante Una publicación en la revista Science ha destapado un posible caso de fraude en una importante línea de investigación contra el alzhéimer. La señal de alarma la hizo sonar Matthew Schrag, neurólogo y neurocientífico de la Universidad de Vanderbilt, y la propia revista continuó el análisis.
Identificaron que había todo tipo de manipulaciones de imágenes en al menos diez artículos sobre el llamado péptido Aβ*56. Todos ellos incluían la firma del neurocientífico Sylvain Lesné.
El Aβ*56 es una forma en la que se puede presentar la proteína beta-amiloide, la sustancia que se encuentra formando placas en los cerebros de los enfermos de alzhéimer y que, según la teoría dominante en las últimas décadas, es la responsable de iniciar la enfermedad.
Nature en 2006, aseguraba que al inyectar la forma Aβ*56 en ratas sanas, estas desarrollaban pérdidas de memoria. Era la primera vez que se demostraba que una sustancia, teóricamente presente en los cerebros de personas enfermas de alzhéimer, causaba directamente esos síntomas. Supuso un espaldarazo a la hipótesis del amiloide.
Schrag evita el término “fraude” en sus críticas y describe sus hallazgos como una “señal de alerta”. Otros expertos consultados por la revista Science los califican como “ejemplos sorprendentes de manipulación de imágenes”. También se dice que muchos otros grupos intentaron sin éxito reproducir los resultados, pero muy pocos lo comunicaron. Aunque un resultado irreproducible no implica necesariamente un fraude, en el artículo se reconoce que existe muy poco interés por los resultados negativos y es difícil contradecir a investigadores con autoridad.
En redes sociales afirmaron que toda la investigación sobre el alzhéimer se basaba en un fraude y que se habían dilapidado cientos de millones de euros y décadas de esfuerzos. Sin embargo, muchos expertos han tratado de desmentir esas conclusiones y de contextualizar sus repercusiones. Todo gira alrededor de la proteína beta-amiloide.
β- amiloide 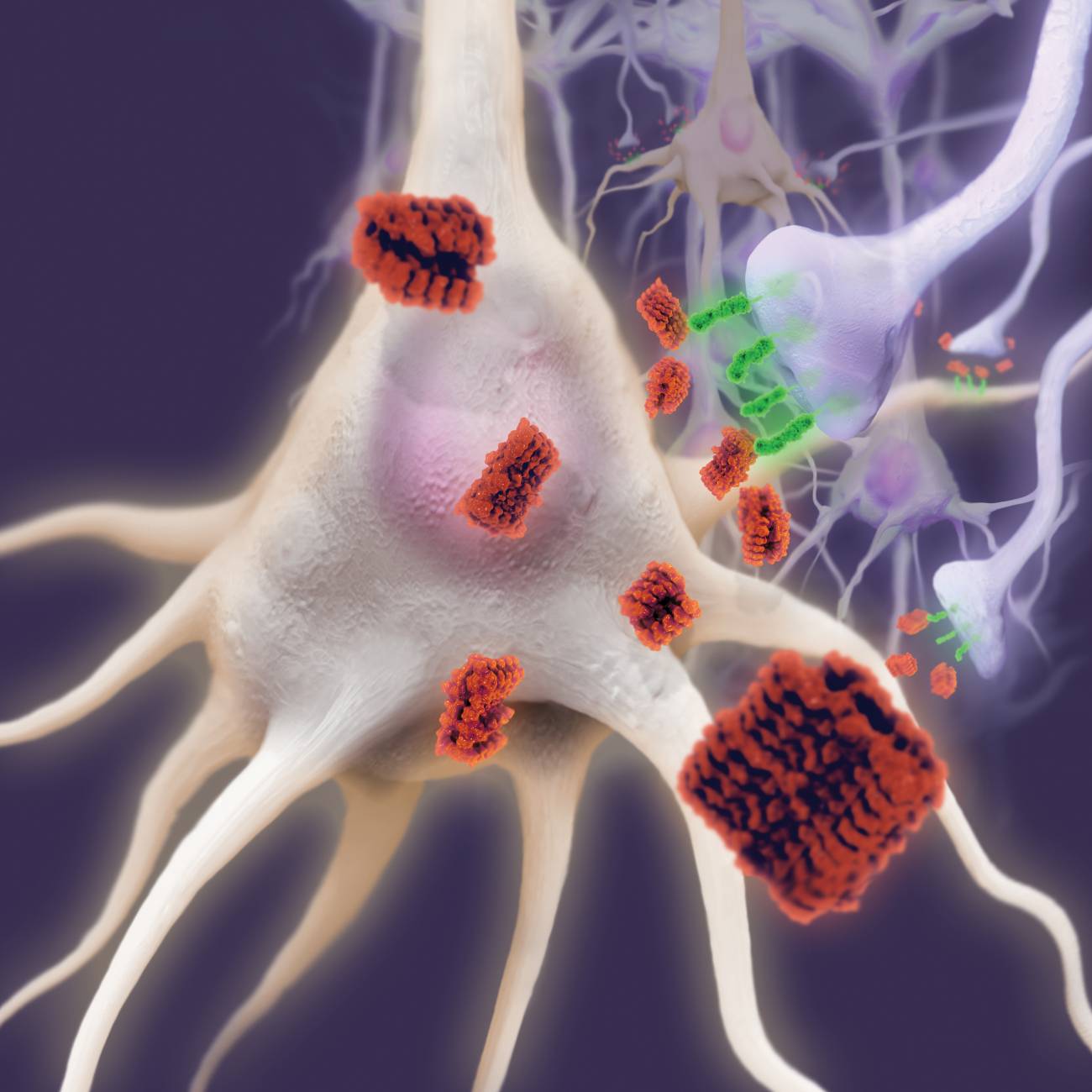
Son pequeños fragmentos que proceden de la llamada proteína precursora del amiloide. Existen múltiples formas diferentes que tienden a agregarse y que acaban formando las placas características de la enfermedad de Alzheimer. En el caso del Aβ*56, se trataría de lo que se llama un oligómero soluble, sería una forma presuntamente tóxica pero que no se encuentra formando parte de las placas.
¿Desmonta el posible fraude la teoría del amiloide y el alzhéimer?
El investigador en alzhéimer Karl Herrup, afirma “la magnitud del fraude es espeluznante, pero la importancia para el campo del alzhéimer se ha exagerado gravemente”.
Según Derek Lowe, ex investigador del alzhéimer y responsable de un blog en la revista Science, “ciertamente, aumentó el entusiasmo y los niveles de financiación en el área y dio a la gente más razones para creer”. Sin embargo, los trabajos sobre el Aβ*56 ahora en cuestión “no condujeron directamente a ningún ensayo clínico sobre esa forma en concreto”.
Estos trabajos supusieron un espaldarazo, pero son solo una rama en todo el árbol de la teoría. También en Twitter, el investigador Samuel Marsh explicaba que “el trabajo principal en cuestión no estableció el modelo de la placa amiloide. Hablaba de un oligómero específico denominado AB*56. Hay muchos otros artículos en este campo que muestran la importancia y los efectos de los oligómeros y las placas”. Y seguía: “Sinceramente, dudo que la ausencia de este artículo en particular y del AB*56 en los registros científicos históricos hubieran cambiado significativamente los últimos 20 años de desarrollo de fármacos para la enfermedad de Alzheimer. Esto se debe a que existen sólidas pruebas genéticas y de otro tipo sobre el papel del amiloide en la enfermedad”.
Para John Hardy, descubridor de una de las mutaciones que llevan indefectiblemente a la enfermedad, “es una vergüenza que estos trabajos impliquen un engaño, y las revistas e instituciones deben tomar medidas contra el fraude cuando se descubre”. Sin embargo, “nunca he pensado que este artículo fuera importante, y creo que nunca me he referido a él en mi propio trabajo”. 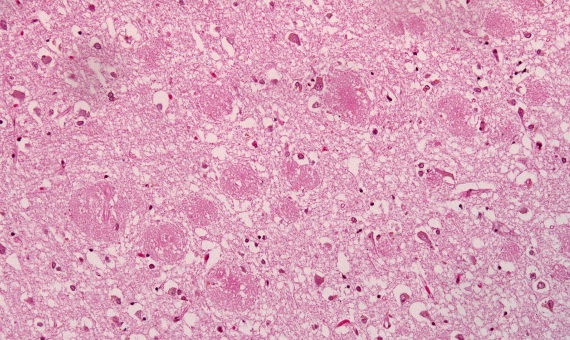
Autopsia cerebral de un paciente diagnosticado con Alzheimer. En la mancha HE numerosas placas amiloides.
En los últimos años ha habido un debate intenso sobre la relevancia del amiloide en la enfermedad de Alzheimer. Una razón es que bastantes personas ancianas presentan placas de amiloide, pero no tienen síntomas, por lo que este podría no ser suficiente para desarrollar la enfermedad. Por otro, y esta es la razón principal, aunque los ensayos clínicos diseñados para reducir las placas han conseguido disminuirlas en varias ocasiones, han fracasado invariablemente a la hora de mejorar los síntomas.
Incluso aquellos ensayos realizados de forma precoz y en personas portadoras de mutaciones que les hacen en el futuro desarrollar la enfermedad no han demostrado ninguna mejoría.
Actualmente solo hay un fármaco antiamiloideo aprobado para el alzhéimer, el ADUCANUMAB. Se le dio luz verde en Estados Unidos en medio de una enorme controversia, tanto por el extraño desarrollo de los ensayos clínicos como por la decisión final. En Europa, la Agencia Europea del Medicamento rechazó aprobarlo, aludiendo a que no había demostrado beneficio clínico y no era suficientemente seguro.
Qué podría explicar el fracaso de los ensayos clínicos
Aunque por lógica y por los estudios genéticos sea difícil de aceptar, es posible que el amiloide sea lo que se conoce como un epifenómeno, algo que acompaña a la verdadera causa pero que no actúe como tal.
Podría ser que los tratamientos incluidos en los ensayos no estuvieran llegando a tiempo. El daño producido por el amiloide podría ser muy precoz, y disminuirlo una vez ha desencadenado la agresión quizá no sea suficiente. Aunque algunos ensayos se han hecho en personas todavía sin síntomas, quizá sea aun así demasiado tarde.
Otra opción es que los anticuerpos utilizados para disminuir el amiloide no lo redujeran lo suficiente o que estuvieran actuando contra ciertas formas de este que fueran las realmente tóxicas. En este caso se estaría reduciendo la cantidad total, pero no aquello que está produciendo realmente el daño.
Y cada vez se acepta más que la enfermedad de Alzheimer es un síndrome, más que una enfermedad unívoca, y que hay muchos factores a tener en cuenta.
Sobre este caso en concreto, así acababa su explicación Samuel Marsh: “Bien, eso es todo por ahora. Una conducta horrible, sí. La razón por la que el campo de la enfermedad de Alzheimer se ha centrado en el amiloide durante los últimos 16 años: absolutamente no. Esta es una gran noticia de por sí, pero la información hiperbólica y poco exacta empeora las cosas”.
El control de la inflamación mejora la enfermedad de Alzhéimer
Otro trabajo sobre Alzheimer EL CURRY 
Un estudio muestra que un componente químico del curry podría utilizarse para el desarrollo de nuevos tratamientos de la enfermedad de Alzheimer. El componente ayuda a la liberación a la sangre de las placas del cerebro típicas de la enfermedad.
Un equipo de investigadores de la Universidad de California han estudiado unos aceites llamados curcominoides, que se encuentran en la curcuma. Han encontrado un componente químico llamado bisdemetoxicurcumina, que al mezclarlo con la proteína beta amiloide y muestras de sangre procedentes de pacientes con y sin Alzheimer ha producido este efecto.
Los macrófagos del sistema inmune en los enfermos de Alzheimer tienen dificultades para eliminar de las placas beta amiloides, causantes de la enfermedad. El componente químico del curry interviene en este proceso, ya que los macrófagos de la sangre de los enfermos de Alzheimer son capaces de eliminar más eficientemente la proteína beta amiloide cuando este compuesto del curry está presente.
En estudio en animales confirma el papel de determinados receptores en la limpieza del cerebro
Controlar la inflamación del cerebro podría ser una vía para mejorar la enfermedad de Alzheimer, asegura un estudio publicado en «The Journal of Experimental Medicine».
El alzhéimer se caracteriza por la acumulación tóxica de una proteína del cerebro llamada beta-amiloide y que la limpieza de estas ‘placas’ de proteínas reduce la enfermedad. Se sabe además que las células inmunes llamadas macrófagos se infiltran en el cerebro ayudan a limpiar estas proteínas tóxicas, con la ayuda de las células del cerebro llamadas microglia residentes. Ambos, macrófagos y microglia, expresan un receptor de superficie llamado TREM2, y aunque las mutaciones en TREM2 han sido asociadas con A el alzhéimer, la función del receptor es incierto.
Limpieza más eficiente 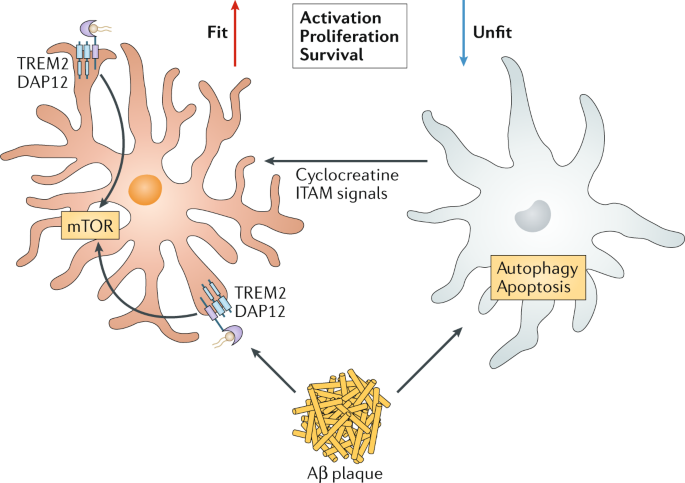
La TREM2, una proteína presente en la microglía, puede conseguir ralentizar el deterioro cerebral en el Alzheimer, según ha demostrado un estudio, publicado en The Lancet Neurology, desarrollado por investigadores de la Unidad de Trastornos Cognitivos del Servicio de Neurología del Hospital Universitario 12 de Octubre. Este hallazgo puede convertirse en el origen de nuevas opciones terapéuticas capaces de potenciar esta proteína y aplicarla como tratamiento preventivo para retrasar el inicio de los primeros síntomas en personas con riesgo de padecer Alzheimer.
Para descifrar el papel de TREM2 en la enfermedad, el equipo de Bruce Cordero, del Instituto de Investigación Lerner de la Clínica Cleveland (EE.UU.) eliminaron el receptor en ratones que desarrollan una enfermedad similar a AD. La eliminación de TREM2 disminuyó la formación de placa, la reducción de la inflamación del cerebro y mejoró la supervivencia de las neuronas. Esta protección se asoció con un menor número de macrófagos infiltrantes. Los investigadores vieron que los macrófagos que carecían de TREM2 eran más eficientes en la limpieza de beta-amiloide, lo que sugiere que podrían ayudar en la tarea de limpieza del cerebro.
Aunque se necesitan más estudios para aclarar el mecanismo exacto de la acción de TREM2 en el alzhéimer, estos resultados sugieren que bajar el tono de la actividad del receptor puede ayudar a poner fin a la neurodegeneración en pacientes con esta enfermedad tan discapacitante.
Bibliografia
Alois Alzheimer (y Oskar Fischer)
Matthew Schrag, neurólogo y neurocientífico de la Universidad de Vanderbilt
Europa Press Science Media Centre 5 de agosto de 2022 14:38h
Sylvain Lesné.
Karl Herrup, “la magnitud del fraude es espeluznante, pero para el campo del alzhéimer se ha exagerado gravemente”.
John Hardy, descubridor de una de las mutaciones que llevan indefectiblemente a la enfermedad,
«The Journal of Experimental Medicine». Controlar la inflamación del cerebro podría ser una vía para mejorar la enfermedad de Alzheimer,
Bruce Cordero, del Instituto de Investigación Lerner de la Clínica Cleveland (EE.UU.)
La TREM2, proteína presente en la microglía, puede conseguir ralentizar el deterioro cerebral en el Alzheimer, The Lancet Neurology,