Illustration showing the multiple sclerosis
Era de esperar que las enfermedades degenerativas y concretamente las neurodegenerativas, tuvieran un patron microbiano y desarrollaran autoinmunidad, que resultaba letal y que estaba en relación con múltiples procesos biologicos
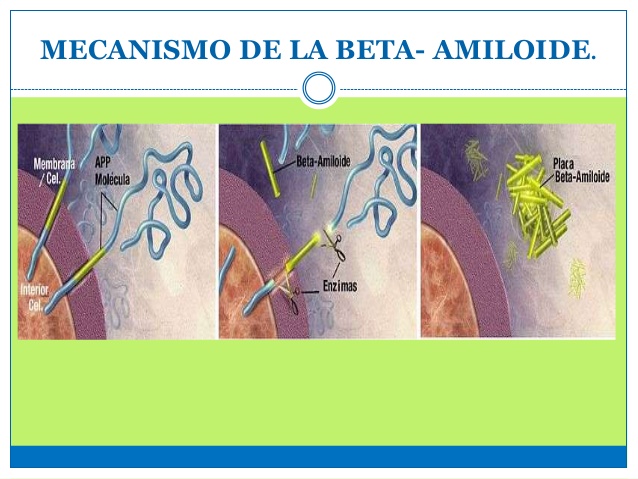
El Alzheimer (AL) es una enfermedad neurodegenerativa, y la causa principal y más conocida Enfermedades demenciales, cuya característica principal es la pérdida de memoria. Su relación
con la proteína amiloide y tau es indiscutible. Su acumulo en el lóbulo temporal entre otras zonas del cerebro mutila la funciones cognoscitiva y produce demencia.
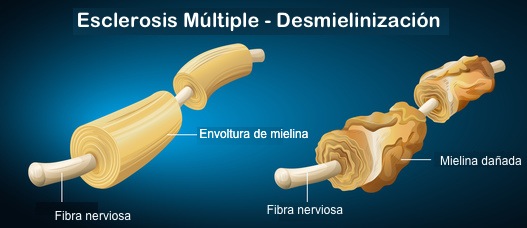
La Esclerosis Múltiple, (EM) también es una enfermedad neurodegenerativa, y afecta a los nervios, destruye la mielina que es su aislante Los nervios están envueltos en mielina que los aisla y permite su función. Cuando se desmielinizan, y este aislante se rompe o desaparece, las señales nerviosas no llegan correctamente, y poco a poco impiden la conducción nerviosa.
Que relación existe entre AL y AM ? Aparentemente ninguna, pero ahora se ha descubierto que la molécula causante de la enfermedad de AL, una proteína llamada beta-amiloide, causante de la degeneración neuronal, es capaz de curar e incluso revertir los efectos de la EM.
Esto supone un nuevo y alentador método de tratamiento, según afirman , en la Universidad de Stanford, en California, cuyo trabajo ha sido publicado en la revista Science Traslational Medicine. Como ellos mismos dicen, esta molécula debería agravar los daños en la mielina, ya que es tóxica para las neuronas. Sin embargo, cuando realizaron un experimento inyectando la proteína beta-amiloide en las cavidades corporales de ratones con EM , esta molecula consiguió retrasar el inicio de la parálisis típica de esta enfermedad, e incluso se llego a revertir.
La beta-amiloide sería capaz de luchar contra la reacción inflamatoria autoinmune que causa la EM.
Lo más raro del asunto es que en otras investigaciones anteriores a esta se había descubierto que la proteína beta-amiloide y su precursor se encuentran en las lesiones de la EM . De hecho, la proteína se identificaba como un marcador de daño en la mielina, por eso en la investigación se pensaba que la molécula dañaría más a la mielina, y no al contrario.
Lawrence Steinman, ya había usado ratones en otros estudios para desarrollar fármacos contra la EM, como el natalizumab, un potente medicamento que modifica la activación y proliferación de células inmunes externas al sistema nervioso central, impidiendo que estas afecten a las células nerviosas, ya que la EM, al ser autoinmune, lo que provoca es que el mismo sistema inmunitario ataque a las células del sistema nervoso.
Por ello, sabiendo esto sobre las células inmunes externas, analizaron que pasaría con la administración de la proteína beta-amiloide fuera del cerebro, concretamente se inyectó en el vientre de los ratones y no en el cerebro. Aunque los sistemas inmunes de estos ratones estaban preparados para atacar al aislante nervioso o mielina, con la administración de la beta-amiloide se produjo todo lo contrario. Así lo expresa Steinman: “Esta es la primera vez que la beta amiloide demuestra tener propiedades antiinflamatorias”
En definitiva, la beta-amiloide fuera del sistema nervioso central tendría propiedades como antiinflamatorio, todo lo contrario a lo que produce cuando se encuentra dentro del mismo cerebro o de los nervios.
El juego inflamatorio en enfermedades degenerativas, llegan siempre a las misma situaciones, un problema de inflamación y reparación complejo e imbricado.
No es la primera vez que se analizan las propiedades de la beta amiloide, El Hospital General de Massachusetts (MGH,), evidencio que la proteína beta-amiloide se deposita en forma de placas en el cerebro de pacientes con enfermedad de AL y se la considera una parte normal del sistema inmune innato, primera línea de defensa del cuerpo contra la infección.
Su estudio, publicado en ‘Science Translational Medicine’, concluye que la expresión de beta-amiloide humana resulta protectora contra las infecciones potencialmente letales en ratones, en el C elegans y en células cerebrales humanas en cultivo. “Se ha pensado que la neurodegeneración en la enfermedad de AlL es causada por el comportamiento anormal de moléculas de beta-amiloide, que son conocidas por reunirse en resistentes estructuras de fibrillas llamadas placas amiloides en el cerebro de los pacientes
En 2010 , Moir y Rudolph Tanzi, director del MGH-MIND y concluyeron que la beta-amiloide tenía muchas de las cualidades de un péptido antimicrobiano (AMP) y se trata de una pequeña proteína innata del sistema inmune que protege contra una amplia gama de patógenos.
En ese estudio se compararon formas sintéticas de A-beta con un conocido AMP llamado LL-37 y se encontró que la beta inhibe el crecimiento de varios patógenos importantes, a veces igual de bien o mejor que LL-37. La beta amiloide de los cerebros de los pacientes de AL también suprimió el crecimiento del hongo ‘Candida’ cultivado para esa investigación y, posteriormente, otros grupos han documentado la acción de A-beta sintético contra los virus de influenza y herpes.
En este nuevo trabajo, los investigadores encontraron que los ratones transgénicos que expresan A-beta humano sobrevivieron significativamente más tiempo después de inducir la infección por ‘Salmonella’ en sus cerebros frente a los ratones sin alteración genética. Los ratones que carecen de la proteína precursora de amiloide murieron incluso más rápidamente.
La expresión de la beta transgénica parece proteger a los gusanos ‘C.elegans’ de cualquier infección por ‘Candida’ o ‘Salmonella’. Del mismo modo, la expresión de beta humana protegio las células neuronales cultivadas de ‘Candida’. De hecho, la beta amiloide humano expresado por células vivas parece ser mil veces más potente contra la infección que el beta amiloide sintético utilizado en estudios previos.
Esa superioridad parece referirse a propiedades de beta amiloides que se han considerado parte de la patología en la enfermedad AL, la propensión de moléculas pequeñas a combinarse en lo que se denominan oligómeros y luego se agregan en placas de beta-amiloide.
Las preparaciones sintéticas de beta amiloide utilizadas en los estudios anteriores no inclujeron oligómeros; pero en el actual estudio, el oligómero de beta amiloide humano no sólo mostró una actividad antimicrobiana aún más fuerte, sino que también se observó su agregación en los tipos de fibrillas que forman las placas de beta-amiloide para atrapar los microbios en los modelos de ratones y gusanos redondos.
Tanzi explica que “se sabe que AMP juega un papel en las patologías de una amplia gama de enfermedades inflamatorias”. “Por ejemplo, LL-37, que ha sido nuestro modelo para la actividad antimicrobiana de beta amiloide, ha sido implicado en varias enfermedades al final de la vida, incluyendo artritis reumatoide, lupus y aterosclerosis. El tipo de desregulación de la actividad de AMP que puede causar inflamación mantenida en esos trastornos podría contribuir a las acciones neurodegenerativas de beta amiloide en la enfermedad de AL.
Moir añade: “Nuestros resultados plantean la intrigante posibilidad de que puede surgir la patología de AL, cuando el cerebro se percibe a sí mismo como bajo el ataque de los patógenos invasores, aunque se necesitan estudios adicionales. No parece probable que las vías inflamatorias del sistema inmune innato puedan ser posibles dianas de tratamiento. Si se validan, nuestros datos también justifican la necesidad de tener precaución con terapias dirigidas a la eliminación total de las placas de beta-amiloide. Las terapias basadas en la disminución de amiloides, pero no en la eliminación de beta amiloide en el cerebro podría ser una estrategia mejor”.
El siguiente paso es la búsqueda de microbios en los cerebros de pacientes de AL y enfermedades degenerativas en general, que puedan haber desencadenado la deposición de amiloide como una respuesta protectora, llevando más tarde a la muerte de las células nerviosas. “Si podemos identificar a los culpables –ya sean bacterias, virus u hongos– podemos ser capaces de dirigirnos a ellos terapéuticamente para la prevención primaria de la enfermedad”.