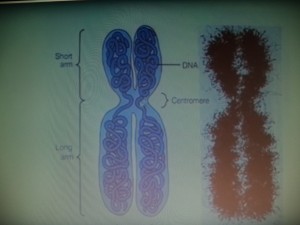
 El estudio de las alteraciones genéticas de la artrosis es un tema debatido y hasta ahora no ha tenido una conclusión lo suficientemente clara como para creer que la enfermedad tenga una participación genetica. La mayoria de las alteraciones geneticas en esta enfermedad, concluyen que se encuentra alguna vez en los genes que promocionan la vitamina D
El estudio de las alteraciones genéticas de la artrosis es un tema debatido y hasta ahora no ha tenido una conclusión lo suficientemente clara como para creer que la enfermedad tenga una participación genetica. La mayoria de las alteraciones geneticas en esta enfermedad, concluyen que se encuentra alguna vez en los genes que promocionan la vitamina D
Estudio aquí un trabajo amplio sobre alteraciones genéticas RAQUIDEA en la artrosis de los autores Cristina Rodriguez-Fontenla∗ y Antonio Gonzalez Laboratorio de Investigación 10, Rheumatology Unit, Instituto de Investigación Sanitaria Hospital Clínico Universitario de Santiago, Santiago de Compostela, La Coruña, España, publicado en Julio de 2014.
Este trabajo es complejo y muy específico y si no se conoce la función de los genes y su terminología, será difícil entenderlo, no obstante es exhaustivo aunque no concluyente
Empieza estudiando esta patología en gemelos :
Los estudios en gemelos nos han dado luz sobre el comportamiento de los genes en la artrosis RAQUIDEA. También llamada osteoartritis (OA). La herencia de esta enfermedad oscila con los distintos autores. En la de rodilla la herencia se localiza en el 40%, lo hace en el 65% en los casos de OA de cadera y en lo que respecta a la columna vertebral sufren la herencia en la OA el 70%.
Los primeros estudios se hicieron en ligamentos por estar estos ampliamente distribuidos en las articulaciones. Los genes de la 4-R y en el cluster IL-1 (2-4). posiblemente implicados, se vio posteriormente que esto locus no se habían confirmado.
Hay que partir de la base que un factor genético no tiene igual efecto en la susceptibilidad a la enfermedad en distintas poblaciones. Esto se refleja claramente en los estudios genéticos realizados en poblaciones europeas y asiática
Se eligieron para estudio genes funciónantes y relevantes en la enfermedad, es decir genes que codifican proteínas reguladoras del anabolismo y catabolismo en la matriz extracelular y para moderar la inflamación. Se obtuvieron muestras relativamente grandes. Y sólo se confirmó como posible gene lesionado el GDF-5 (8-5).
La GWAS es un sistema que permiten estudiar toda la variabilidad genética del genoma sin hipótesis previa . La organización del genoma en bloques de LD permite obtener una representación de una región genómica seleccionando algunos SNPs informativos (tagSNPs). Los tagSNPs característicos de una región se conocen gracias al proyecto Hap-Map que estudió gran número de SNPs en diferentes poblaciones.
Basándose en esta información, los arrays de genotipado de alta densidad proporcionan una cobertura casi completa de la variabilidad del genoma. Los arrays utilizados en la mayoría de los GWAS de OA contienen 500.000 SNPs y en el caso del estudio arcOGEN, el más potente realizado en OA, se utilizó un array que cubre 610.000 SNPs10,11. Una de las características principales de los GWAS es el umbral de significación considerado tras corregir por test múltiples (p < 5× 10−8). Este umbral viene dado por la estimación de que existen aproximadamente 106 SNPs independientes en el genoma humano, (0,05/106 = 5 × 10−8, y tiene la ventaja de reducir la tasa de falsos positivos. Gracias a los GWAS y a los metaanálisis de GWAS se han ido descubriendo genes de susceptibilidad a OA, aunque el número de loci es relativamente bajo en comparación con otras enfermedades complejas. Los primeros hallazgos sólidos fueron el gen GDF-5, el locus 7q22 y MCF2L9,12,13. Más recientemente se han incorporado los loci descubiertos en el estudio arcOGEN (GNL3, GLT8D1, ASTN2, FILIP1-SENP6, KLHDC-5-PTHLH, CHST11, TP63 y SUPT3H-CDC5L) y otros loci como DOT1L, NCOA3 y ALDH1A211,14-16.
En resumen, se pueden considerar 2 grandes grupos de loci asociados con OA:
1 Loci posiblemente asociados con OA pero que no han alcanzado el nivel de asociación requerido en los GWAS
2 Loci que han alcanzado el nivel de asociación de los GWAS (p < 5 ×10−8 y que, por lo tanto, son los más consistentemente asociados con OA
Dos son las alteracuiones geneticas mas frecuentemente encontradas en la OA
GDF-5 fue el primer locus asociado a nivel de GWAS en europeos y asiáticos. Un estudio en población japonesa descubrió la asociación de un SNPs (rs143383, C/T) en la región 5_UTR del gen. Esta asociación se observó con OA de cadera (p = 1,8 × 10−13) y con menor magnitud con OA de rodilla8
El locus del cromosoma 7q22 con sus 6 genes El segundo locus que se encontró asociado a nivel de GWAS
en europeos es el locus del cromosoma 7q22. Es un locus muy extenso que ocupa unas 500 kb, y contiene 400 SNPs y 6 genes diferentes: PRKAR2B, HBP1, COG5, GPR22, DUS4L y BCAP29. La asociación de este locus con OA de rodilla se descubrió en un GWAS que después de diferentes fases de estudio de 500.000 SNPs llevó a solo un SNPs, rs3815148, con asociación a nivel de GWAS mayor (OR = 1,14, p = 8 ×10−8)10.
El proyecto arcOGEN es el más ambicioso realizado hasta el momento en el campo y constituye un gran esfuerzo para el esclarecimiento de las bases genéticas de susceptibilidad a la OA.
En contraste con otras enfermedades complejas en las que muchos polimorfismos con pequeño efecto se
encuentran junto a unos pocos de efecto marcado, en la OA no se ha encontrado ninguna evidencia de polimorfismos de gran efecto.
Los 2 SNPs más asociados, rs6976 y rs11177, representan una única señal que está asociada con OA y reemplazamiento articular tanto de la rodilla como de la cadera. Uno de estos SNPs, rs6976, está situado en la región 3_UTR de GLT8D1, y el otro, rs11177, es un SNPs no sinónimo localizado en el exón 3 de GNL3, por lo que cualquiera
de estos genes podría ser el responsable de la asociación 3 loci que mostraron asociación cerca del umbral de p < 5
debe se˜nalar que, al igual que en la primera fase de arcOGEN, no se replica la asociación de GDF-5 ni del locus 7q22 a nivel de GWAS, a pesar de que, como se ha se˜nalado, se trata de asociaciones sólidas. Esta falta de replicación se ha atribuido a una combinación de diferentes factores: insuficiente poder estadístico dado el tamaño de la muestra en la fase de descubrimiento y las frecuencias alélicas
El papel del ADN mitocondrial en la artrosis
Además del genoma nuclear también se ha estudiado el posible papel de los haplogrupos del ADNmt en OA. Cada
haplogrupo mitocondrial está definido por una combinación particular de variantes genéticas. En concreto, los haplogrupos J (m.4216T > C, m.10398ª > G) y JT (m.4216T > C) se encontraron asociados con un menor riesgo de padecer OA de rodilla y los haplogrupos relacionados J y J1c (m.14798T > C) con un menor riesgo de OA de cadera en espa˜noles50,51. En población asiática también se encontró asociación de otros 2 haplogrupos mitocondriales,
G y B/B4, que mostraron un efecto de susceptibilidad y protección, respectivamente52. Sin embargo, en el estudio arcOGEN de un tama˜no muestral mayor (7.393 casos y 5.122 controles del Reino Unido) no se encontró asociación con ningún haplogrupo de ADNmt53.
La artrosis (OA) es una enfermedad compleja en la que diferentes factores ambientales interactúan con múltiples factores genéticos. Esta revisión se centra en los estudios que han contribuido a descubrir los factores genéticos de susceptibilidad a la OA. También se tratan con detalle los loci más relevantes en la actualidad, como GDF-5, el locus en el cromosoma 7q22, MCF2L, DOT1L, NCOA3 y los provenientes del estudio arcOGEN. Además, se discuten las diferentes aproximaciones que pueden servir para minimizar
los problemas específicos del estudio de la genética de la OA..
El complicado y minucioso estudio de las alteraciones genómica en la OA, está muy parcialmente estudiado y aún no se ha llegado a conclusiones válidas, queremos pensar que nuevos estudios nos darán una luz más acertada.
Bibiografia
1.-Lymph and blood supply of the human intervertebral disc. Cadaver study of correlations to discitis.
Rudert M1, Tillmann B. Acta Orthop Scand. 1993 Feb;64(1):37-40. Ann Anat. 1993 Jun;175(3):237-42.
2. – Detection of lymph and blood vessels in the human intervertebral disc by histochemical and immunohistochemical methods.Rudert M1, Tillmann B. Ann Anat. 1993 Jun;175(3):237-42
3. – Evolution of disc degeneration in lumbar spine: a comparative histological study between herniated and postmortem retrieved disc specimens.Repanti M1, Korovessis PG, Stamatakis MV, Spastris P, Kosti P. J Spinal Disord. 1998 Feb;11(1):41-5.
4. Wiltse LL: El tratamiento de la espondilolistesis y la espondilolisis en los niños. Clin.Orthop., 117:92-100,
1976.
5. Michelli LJ: lesiones de la espalda en la gimnasia. Clin Sports Med.., 4:85-93, 1985.
Peter N. Fysh, D.C., B. Aplicación., Sc. Sunnyvale, California,
6. Los gérmenes anaerobios de la piel en la Artrosis raquidea E. Rubio @ 15:0716 Marzo 2016. enriquerubio.net
7. Enrique Rubio, del Centro Médico Delfos y uno de los ponentes que ha tratado sobre las nuevas teorías de la etiopatogenia de la artrosis vertebral en el V Congreso Nacional de Neuro Raquis, celebrado en Gerona.
8. Stirling A, Worthington T, Rafi M, Lambert PA, Elliott TSJ. Association between sciatica and Propionibacterium acnes. Lancet 2001;357:2024-2025
LOS GENES EN LA ARTROSIS RAQUIDEA.
El estudio de las alteraciones genéticas de la artrosis es un tema debatido y hasta ahora no ha tenido una conclusión lo suficientemente clara como para creer que la enfermedad tenga una participación genetica. La mayoria de las alteraciones geneticas en esta enfermedad, concluyen que se encuentra alguna vez en los genes que promocionan la vitamina D
Los estudios en gemelos no han dado luz sobre el comportamiento de los genes en la artrosis RAQUIDEA. La herencia de esta enfermedad oscila con los distintos autores. En la de rodilla la herencia se localiza en el 40%, lo hace en el 65% en los casos de OA de cadera y en lo que respecta a la columna vertebral sufren la herencia en la OA el 70%.
Hay que partir de la base que un factor genético no tiene igual efecto en la susceptibilidad a la enfermedad en distintas poblaciones. Esto se refleja claramente en los estudios genéticos realizados en poblaciones europeas y asiática
Se eligieron para estudio genes funciónantes y relevantes en la enfermedad, es decir genes que codifican proteínas reguladoras del anabolismo y catabolismo en la matriz extracelular y para moderar la inflamación. Se obtuvieron muestras relativamente grandes. Y sólo se confirmó como posible gene lesionado el GDF-5 (8-5).
La GWAS es un sistema que permiten estudiar toda la variabilidad genética del genoma sin hipótesis previa . La organización del genoma en bloques de LD permite obtener una representación de una región genómica seleccionando algunos SNPs informativos (tagSNPs). Los tagSNPs característicos de una región se conocen gracias al proyecto Hap-Map que estudió gran número de SNPs en diferentes poblaciones.
Se pueden considerar 2 grandes grupos de loci asociados con OA:
1 Loci posiblemente asociados con OA pero que no han alcanzado el nivel de asociación requerido en los GWAS
2 Loci que han alcanzado el nivel de asociación de los GWAS (p < 5 ×10−8 y que, por lo tanto, son los más consistentemente asociados con OA
Dos son las alteracuiones geneticas mas frecuentemente encontradas en la OA
GDF-5 fue el primer locus asociado a nivel de GWAS en europeos y asiáticos. Un estudio en población japonesa descubrió la asociación de un SNPs (rs143383, C/T) en la región 5_UTR del gen. Esta asociación se observó con OA de cadera (p = 1,8 × 10−13) y con menor magnitud con OA de rodilla8
El locus del cromosoma 7q22 con sus 6 genes El segundo locus que se encontró asociado a nivel de GWAS
en europeos es el locus del cromosoma 7q22. Es un locus muy extenso que ocupa unas 500 kb, y contiene 400 SNPs y 6 genes diferentes: PRKAR2B, HBP1, COG5, GPR22, DUS4L y BCAP29. La asociación de este locus con OA de rodilla se descubrió en un GWAS que después de diferentes fases de estudio de 500.000 SNPs llevó a solo un SNPs, rs3815148, con asociación a nivel de GWAS mayor (OR = 1,14, p = 8 ×10−8)10.
El proyecto ARCOGEN es el más ambicioso realizado hasta el momento en el campo y constituye un gran esfuerzo para el esclarecimiento de las bases genéticas de susceptibilidad a la OA.
En contraste con otras enfermedades complejas en las que muchos polimorfismos con pequeño efecto se encuentran junto a unos pocos de efecto marcado, en la OA no se ha encontrado ninguna evidencia de polimorfismos de gran efecto.
Los 2 SNPs más asociados, rs6976 y rs11177, representan una única señal que está asociada con OA y reemplazamiento articular tanto de la rodilla como de la cadera. Uno de estos SNPs, rs6976, está situado en la región 3_UTR de GLT8D1, y el otro, rs11177, es un SNPs no sinónimo localizado en el exón 3 de GNL3, por lo que cualquiera
de estos genes podría ser el responsable de la asociación 3 loci que mostraron asociación cerca del umbral de p < 5
debe señalar que, al igual que en la primera fase de arcOGEN, no se replica la asociación de GDF-5 ni del locus 7q22 a nivel de GWAS, a pesar de que, como se ha se˜nalado, se trata de asociaciones sólidas. Esta falta de replicación se ha atribuido a una combinación de diferentes factores: insuficiente poder estadístico dado el tamaño de la muestra en la fase de descubrimiento y las frecuencias alélicas
El papel del ADN mitocondrial en la artrosis .Además del genoma nuclear también se ha estudiado el posible papel de los haplogrupos del ADNmt en OA. Cada haplogrupo mitocondrial está definido por una combinación particular de variantes genéticas. En concreto, los haplogrupos J (m.4216T > C, m.10398ª > G) y JT (m.4216T > C) se encontraron asociados con un menor riesgo de padecer OA de rodilla y los haplogrupos relacionados J y J1c (m.14798T > C) con un menor riesgo de OA de cadera en espa˜noles50,51. En población asiática también se encontró asociación de otros 2 haplogrupos mitocondriales, G y B/B4, que mostraron un efecto de susceptibilidad y protección, respectivamente52. Sin embargo, en el estudio arcOGEN de un tama˜no muestral mayor (7.393 casos y 5.122 controles del Reino Unido) no se encontró asociación con ningún haplogrupo de ADNmt53.
La artrosis (OA) es una enfermedad compleja en la que diferentes factores ambientales interactúan con múltiples factores genéticos. Esta revisión se centra en los estudios que han contribuido a descubrir los factores genéticos de susceptibilidad a la OA. También se tratan con detalle los loci más relevantes en la actualidad, como GDF-5, el locus en el cromosoma 7q22, MCF2L, DOT1L, NCOA3 y los provenientes del estudio arcOGEN. Además, se discuten las diferentes aproximaciones que pueden servir para minimizar los problemas específicos del estudio de la genética de la OA..
El complicado y minucioso estudio de las alteraciones genómica en la OA, está muy parcialmente estudiado y aún no se ha llegado a conclusiones válidas, queremos pensar que nuevos estudios nos darán una luz más acertada.
Bibliografía
1. Spector TD, MacGregor AJ. Risk factors for osteoarthritis: Genetics. Osteoarthritis Cartilage. 2004;12 Suppl A:S39–44.
2. Stefánsson SE, Jónsson H, Ingvarsson T, Manolescu I, Jónsson HH, Olafsdóttir G, et al. Genomewide scan for hand osteoarthritis: A novel mutation in matrilin-3. Am J Hum Genet. 2003;72:1448–59.
3. Forster T, Chapman K, Loughlin J. Common variants within the interleukin 4 receptor alpha gene (IL4R) are associated with susceptibility to osteoarthritis. Hum Genet. 2004;114:391–5.
4. Leppävuori J, Kujala U, Kinnunen J, Kaprio J, Nissilä M, Heliövaara M, et al. Genome scan for predisposing loci for distal interphalangeal joint osteoarthritis: Evidence for a locus on 2q. Am J Hum Genet. 1999;65:1060–7.
5. Valdes AM, Loughlin J, Timms KM, Meurs JJB, van Southam L, Wilson SG, et al. Genome-wide association scan identifies a prostaglandin-endoperoxide synthase 2 variant involved in risk of knee osteoarthritis. Am J Hum Genet. 2008;82:1231–40.
6. Meulenbelt I, Min JL, Bos S, Riyazi N, Houwing-Duistermaat JJ, van der Wijk H-J, et al. Identification of DIO2 as a new susceptibility locus for symptomatic osteoarthritis. Hum Mol Genet. 2008;17:1867–75.
7. Loughlin J, Dowling B, Chapman K, Marcelline L, Mustafa Z, Southam L, et al. Functional variants within the secreted frizzled-related protein 3 gene are associated with hip osteoarthritis in females. Proc Natl Acad Sci. 2004;101:9757–62.
8. Miyamoto Y, Mabuchi A, Shi D, Kubo T, Takatori Y, Saito S, et al. A functional polymorphism in the 5_ UTR of GDF5 is associated with susceptibility to
osteoarthritis. Nat Genet. 2007;39:529–33.
9. Valdes AM, Evangelou E, Kerkhof HJM, Tamm AA, Doherty SA, Kisand K, et al. The GDF5 rs143383 polymorphism is associated with osteoarthritis of the knee with genome-wide statistical significance. Ann Rheum Dis. 2011;70:873–5.
10. Kerkhof HJM, Lories RJ, Meulenbelt I, Jonsdottir I, Valdes AM, Arp P, et al. A genome-wide association study identifies an osteoarthritis susceptibility locus on chromosome 7q22. Arthritis Rheum. 2010;62:499–510.
11. Zeggini E, Panoutsopoulou K, Southam L, Rayner NW, Day-Williams AG, Lopes MC, et al. Identification of new susceptibility loci for osteoarthritis (arcOGEN): A genome-wide association study. Lancet. 2012;6736:1–9.
12. Evangelou E, Valdes AM, Kerkhof HJM, Styrkarsdottir U, Zhu YY, Meulenbelt I, et al. Meta-analysis of genome-wide association studies confirms a susceptibility locus for knee osteoarthritis on chromosome 7q22. Ann Rheum Dis. 2011;70:349. Documento descargado de http://www.reumatologiaclinica.org el 30/04/2016. Copia para uso personal, se prohíbe la transmisión de este documento por cualquier medio o formato.
40 C. Rodriguez-Fontenla, A. Gonzalez / Reumatol Clin. 2015;11(1):33–40
13. Day-Williams AG, Southam L, Panoutsopoulou K, Rayner NW, Esko T, Estrada K, et al. A variant in MCF2L is associated with osteoarthritis. Am J Hum Genet. 2011;89:446–50.
14. Castano MC, Cailotto F, Kerkhof HJ, Cornelis FMF, Casta˜no Betancourt MC, Doherty SA, et al. Genome-wide association and functional studies identify the DOT1L gene to be involved in cartilage thickness and hip osteoarthritis. Proc Natl Acad Sci. 2012;109:1–6.
15. Evangelou E, Kerkhof HJ, Styrkarsdottir U, Ntzani EE, Bos SD, Esko T, et al. A metaanalsis of genome-wide association studies identifies novel variants associated with osteoarthritis of the hip. Ann Rheum Dis. 2013;0:1–7.
16. Styrkarsdottir U, Thorleifsson G, Helgadottir HT, Bomer N, Metrustry S, Bierma-Zeinstra S, et al. Severe osteoarthritis of the hand associates with common ariants within the ALDH1A2 gene and with rare variants at 1p31. Nat Genet. 2014;46:498–502.
17. Kerkhof HJM, Meulenbelt I, Akune T, Arden NK, Aromaa A, Bierma-Zeinstra SMA, et al. Recommendations for standardization and phenotype definitions in genetic studies of osteoarthritis: The TREAT-OA consortium. Osteoarthritis Cartilage. 2011;19:254–64.
18. Malfait A-M, Seymour AB, Gao F, Tortorella MD, Graverand-Gastineau MPH, Le Wood LS, et al. A role for PACE4 in osteoarthritis pain: Evidence
from human genetic association and null mutant phenotype. Ann Rheum Dis. 2012;71:1042–8.
19. Valdes AM, de Wilde G, Doherty SA, Lories RJ, Vaughn FL, Laslett LL, et al. The 585Val TRPV1 variant is involved in risk of painful knee osteoarthritis. Ann Rheum Dis. 2011;70:1556–61.
20. Panoutsopoulou K, Southam L, Elliott KS, Wrayner N, Zhai G, Beazley C, et al. Insights into the genetic architecture of osteoarthritis from stage 1 of the arcOGEN study. Ann Rheum Dis. 2011;70:864–7.
21. Gibson G. Rare and common variants: Twenty arguments. Nat Rev Genet. 2011;13:135–45.
22. Dunham I, Kundaje A, Aldred SF, Collins PJ, Davis CA, Doyle F, et al. An integrated encyclopedia of DNA elements in the human genome. Nature. 2012;489: 57–74.
23. Southam L, Rodriguez-Lopez J, Wilkins JM, Pombo-Suarez M, Snelling S, Gomez- Reino JJ, et al. An SNP in the 5_-UTR of GDF5 is associated with osteoarthritis susceptibility in Europeans and with in vivo differences in allelic expression in articular cartilage. Hum Mol Genet. 2007;16:2226–32.
24. Vaes RBA, Rivadeneira F, Kerkhof JM, Hofman A, Pols HAP, Uitterlinden AG, et al. Genetic variation in the GDF5 region is associated with osteoarthritis, height, hip axis length and fracture risk: The Rotterdam study. Ann Rheum Dis. 2009;68:1754–60.
25. Sanna S, Jackson AU, Nagaraja R, Willer CJ, Chen W-M, Bonnycastle LL, et al. Common variants in the GDF5-UQCC region are associated with variation in human height. Nat Genet. 2008;40:198–203.
26. Storm EE, Kingsley DM. GDF5 coordinates bone and joint formation during digit development. Dev Biol. 1999;209:11–27.
27. Tsumaki N, Tanaka K, Arikawa-Hirasawa E, Nakase T, Kimura T, Thomas JT, et al. Role of CDMP-1 in skeletal morphogenesis: promotion of mesenchymal cell recruitment and chondrocyte differentiation. J Cell Biol. 1999;144:161–73.
28. Syddall CM, Reynard LN, Young DA, Loughlin J. The identification of trans-acting factors that regulate the expression of GDF5 via the osteoarthritis susceptibility SNP rs143383. PLoS Genet. 2013;9:e1003557.
29. Reynard LN, Bui C, Canty-Laird EG, Young DA, Loughlin J. Expression of the osteoarthritis-associated gene GDF5 is modulated epigenetically by DNA methylation. Hum Mol Genet. 2011;20:3450–60.
30. Evangelou E, Valdes AM, Kerkhof HJM, Styrkarsdottir U, Zhu Y, Meulenbelt I, et al. Meta-analysis of genome-wide association studies confirms a susceptibility locus for knee osteoarthritis on chromosome 7q22. Ann Rheum Dis. 2011;70:349–55.
31. Guns L-A, Cailotto F, Lories RJ. A5.6 Cholecystokinin and purinoreceptor antagonists modulate OA-associated GPR22 signalling. Ann Rheum Dis. 2014;73 Suppl 1:A65.
32. Raine EVA, Wreglesworth N, Dodd AW, Reynard LN, Loughlin J. Gene expression analysis reveals HBP1 as a key target for the osteoarthritis susceptibility locus that maps to chromosome 7q22. Ann Rheum Dis. 2012;71:2020–7.
33. Verbruggen G. Chondroprotective drugs in degenerative joint diseases. Rheumatology. 2006;45:129–38.
34. Liu F, Lijn F, van der Schurmann C, Zhu G, Chakravarty MM, Hysi PG, et al. A genome-wide association study identifies five loci influencing facial morphology in Europeans. PLoS Genet. 2012;8:e1002932.
35. Elliott KS, Chapman K, Day-Williams A, Panoutsopoulou K, Southam L, Lindgren CM, et al. Evaluation of the genetic overlap between osteoarthritis with body mass index and height using genome-wide association scan data. Ann Rheum Dis. 2012;72:935–41.
36. Eyre D. Collagen of articular cartilage. Arthritis Res. 2002;4:30–5.
37. Jakkula E, Melkoniemi M, Kiviranta I, Lohiniva J, Räinä SS, Perälä M, et al. The role of sequence variations within the genes encoding collagen II, IX
and XI in non-syndromic, early-onset osteoarthritis. Osteoarthritis Cartilage. 2005;13:497–507.
38. Mio F, Chiba K, Hirose Y, Kawaguchi Y, Mikami Y, Oya T, et al. A functional polymorphism in COL11A1, which encodes the alpha 1 chain of type XI collagen, is associated with susceptibility to lumbar disc herniation. Am J Hum Genet. 2007;81:1271–7.
39. Raine EVA, Dodd AW, Reynard LN, Loughlin J. Allelic expression analysis of the osteoarthritis susceptibility gene COL11A1 in human joint tissues. BMC Musculoskelet Disord. 2013;14:85.
40. Rodriguez-Fontenla C, Calaza M, Evangelou E, Valdes AM, Arden N, Blanco FJ, et al. Assessment of osteoarthritis candidate genes in a meta-analysis of 9 genome-wide association studies. Arthritis Rheumatol. 2014;66:940–9.
41. Miyamoto Y, Shi D, Nakajima M, Ozaki K, Sudo A, Kotani A, et al. Common variants in DVWA on chromosome 3p24.3 are associated with susceptibility to knee osteoarthritis. Nat Genet. 2008;40:994–8.
42. Meulenbelt I, Chapman K, Dieguez-Gonzalez R, Shi D, Tsezou A, Dai J, et al. Large replication study and meta-analyses of DVWA as an osteoarthritis susceptibility locus in European and Asian populations. Hum Mol Genet. 2009;18:1518–23.
43. Valdes AM, Spector TD, Doherty S, Wheeler M, Hart DJ, Doherty M. Association of the DVWA and GDF5 polymorphisms with osteoarthritis in UK populations. Ann Rheum Dis. 2009;68:1916–20.
44. Wagener R, Gara SK, Kobbe B, Paulsson M, Zaucke F. The knee osteoarthritis susceptibility locus DVWA on chromosome 3p24.3 is the 5_ part of the split COL6A4 gene. Matrix Biol. 2009;28:307–10.
45. Nakajima M, Miyamoto Y, Ikegawa S. Cloning and characterization of the osteoarthritis-associated gene DVWA. J Bone Miner Metab. 2011;29:300–8.
46. Nakajima M, Takahashi A, Kou I, Rodriguez-Fontenla C, Gomez-Reino JJ, Furuichi T, et al. New sequence variants in HLA class II/III region associated with susceptibility to knee osteoarthritis identified by Genome-Wide Association Study. PLoS One. 2010;5:e9723.
47. Shi D, Zheng Q, Chen D, Zhu L, Qin A, Fan J, et al. Association of single-nucleotide polymorphisms in HLA class II/III region with knee osteoarthritis. Osteoarthritis Cartilage. 2010;18:1454–7.
48. Valdes AM, Styrkarsdottir U, Doherty M, Morris DL, Mangino M, Tamm AA, et al. Large scale replication study of the association between HLA II/BTNL2 variants and osteoarthritis of the knee in European-descent populations. PLoS One. 2011;6:e23371.
49. Zhai G, Meurs JBJ, van Livshits G, Meulenbelt I, Valdes AM, Soranzo N, et al. A genome-wide association study suggests that a locus within the ataxin 2 binding protein 1 gene is associated with hand osteoarthritis: The Treat-OA consortium. J Med Genet. 2009;46:614–6.
50. Rego-Pérez I, Fernández-Moreno M, Fernández-López C, Arenas J, Blanco FJ. Mitochondrial DNA haplogroups: Role in the prevalence and severity of knee osteoarthritis. Arthritis Rheum. 2008;58:2387–96.
51. Rego I, Fernández-Moreno M, Fernández-López C, Gómez-Reino JJ, González A, Arenas J, et al. Role of European mitochondrial DNA haplogroups in the prevalence of hip osteoarthritis in Galicia, Northern Spain. Ann Rheum Dis. 2010;69:210–3.
52. Fang H, Liu X, Shen L, Li F, Liu Y, Chi H, et al. Role of mtDNA haplogroups in the prevalence of knee osteoarthritis in a southern Chinese population. Int J Mol Sci. 2014;15:2646–59.
53. Hudson G, Panoutsopoulou K, Wilson I, Southam L, Rayner NW, Arden N, et al. No evidence of an association between mitochondrial DNA variants and osteoarthritis in 7393 cases and 5122 controls. Ann Rheum Dis. 2013;72:136–9.
54. Soto-Hermida A, Fernández-Moreno M, Oreiro N, Fernández-López C, Rego- Pérez I, Blanco FJ. mtDNA haplogroups and osteoarthritis in different geographic populations. Mitochondrion. 2014;15:18–23.
55. Cillero-Pastor B, Rego-Pérez I, Oreiro N, Fernandez-Lopez C, Blanco FJ. Mitochondrial respiratory chain dysfunction modulates metalloproteases -1, -3 and -13 in human normal chondrocytes in culture. BMC Musculoskelet Disord. 2013;14:235.
56. Dodd AW, Rodriguez-Fontenla C, Calaza M, Carr A, Gomez-Reino JJ, Tsezou A, et al. Deep sequencing of GDF5 reveals the absence of rare variants at this important osteoarthritis susceptibility locus. Osteoarthritis Cartilage. 2011;19:430–4.
57. Kizawa H, Kou I, Iida A, Sudo A, Miyamoto Y, Fukuda A, et al. An aspartic acid repeat polymorphism in asporin inhibits chondrogenesis and increases susceptibility to osteoarthritis. Nat Genet. 2005;37:138–44.
58. Wilkins JM, Southam L, Mustafa Z, Chapman K, Loughlin J. Association of a functional microsatellite within intron 1 of the BMP5 gene with susceptibility to osteoarthritis. BMC Med Genet. 2009;10:141.
59. Rodriguez-Fontenla C, Carr A, Gomez-Reino JJ, Tsezou A, Loughlin J, Gonzalez A. Association of a BMP5 microsatellite with knee osteoarthritis: case-control study. Arthritis Res Ther. 2012;14:R257.